Do, 29.11.2018 - 09:40 — Francis S. Collins

![]() Weltweit erkranken Millionen Patienten an lebensbedrohenden Infektionen, die sie sich während ihres Aufenthalts im Krankenhaus zuziehen und zig-Tausende sterben daran . Bis jetzt wurden dafür Im wesentlichen unzureichende hygienische Bedingungen in den Spitälern verantwortlich gemacht. Eine neue Studie an Knochenmark-transplantierten und dementsprechend immunsupprimierten Patienten zeigt nun, dass die infektiösen Keime auch aus dem Mikrobiom des Darms der Patienten selbst stammen können und bietet damit neue Ansätze zu Prävention und Therapie derartiger Infektionen [1]. Francis Collins, NIH-Direktor und ehem. Leiter des "Human Genome Project", berichtet über diese wegweisenden Ergebnisse.*
Weltweit erkranken Millionen Patienten an lebensbedrohenden Infektionen, die sie sich während ihres Aufenthalts im Krankenhaus zuziehen und zig-Tausende sterben daran . Bis jetzt wurden dafür Im wesentlichen unzureichende hygienische Bedingungen in den Spitälern verantwortlich gemacht. Eine neue Studie an Knochenmark-transplantierten und dementsprechend immunsupprimierten Patienten zeigt nun, dass die infektiösen Keime auch aus dem Mikrobiom des Darms der Patienten selbst stammen können und bietet damit neue Ansätze zu Prävention und Therapie derartiger Infektionen [1]. Francis Collins, NIH-Direktor und ehem. Leiter des "Human Genome Project", berichtet über diese wegweisenden Ergebnisse.*
Während ihrer Behandlung im Krankenhaus erkranken erschreckend viele Patienten an lebensbedrohender Sepsis - d.i. an Infektionen in der Blutbahn. Man hat angenommen, dass dafür Mikroben verantwortlich sind, die hauptsächlich auf medizinischen Geräten herumsitzen und auf dem Spitalspersonal oder auch auf anderen Patienten und Besuchern auf ihre Opfer lauern. Das ist auch sicherlich oft der Fall. Nun hat ein von den National Institutes of Health (NIH) gefördertes Team herausgefunden, dass ein erheblicher Teil dieser Krankenhausinfektionen tatsächlich aus einer ganz anderen Quelle stammen kann, nämlich aus dem Körper des Patienten selbst.
In einer Studie an 30 Knochenmark-transplantierten Patienten, die an Blutinfektionen litten, wendeten die Forscher ein neu entwickeltes Bioinformatik Tool namens StrainSifter ("Stamm-Prüfer", Anm. Redn) an: in mehr als einem Drittel der Fälle entsprach die DNA-Sequenz der infektiösen Keime jener DNA , die bereits im Dickdarm der Patienten lebende Mikroorganismen aufwiesen [1] . Dafür, dass derartige Keime von Patient zu Patient übertragen werden, fanden die Forscher auf Basis der DNA-Datenaber kaum Hinweise.
Infektionen im Krankenhaus
In den Vereinigten Staaten erleidet etwa einer von 50 Patienten mindestens eine Infektion während seines Krankenhausaufenthalte [2]. Solche Infektionen sind jedes Jahr für Zehntausende von Todesfällen verantwortlich und sind in den Vereinigten Staaten eine der häufigsten Todesursachen [3].
Auch in Europa zählen Infektionen im Krankenhaus zu den häufigen Erkrankungen (Abbildung 1) und fordern auch hier sehr viele Todesopfer. (Text und Bild von der Redn. eingefügt) 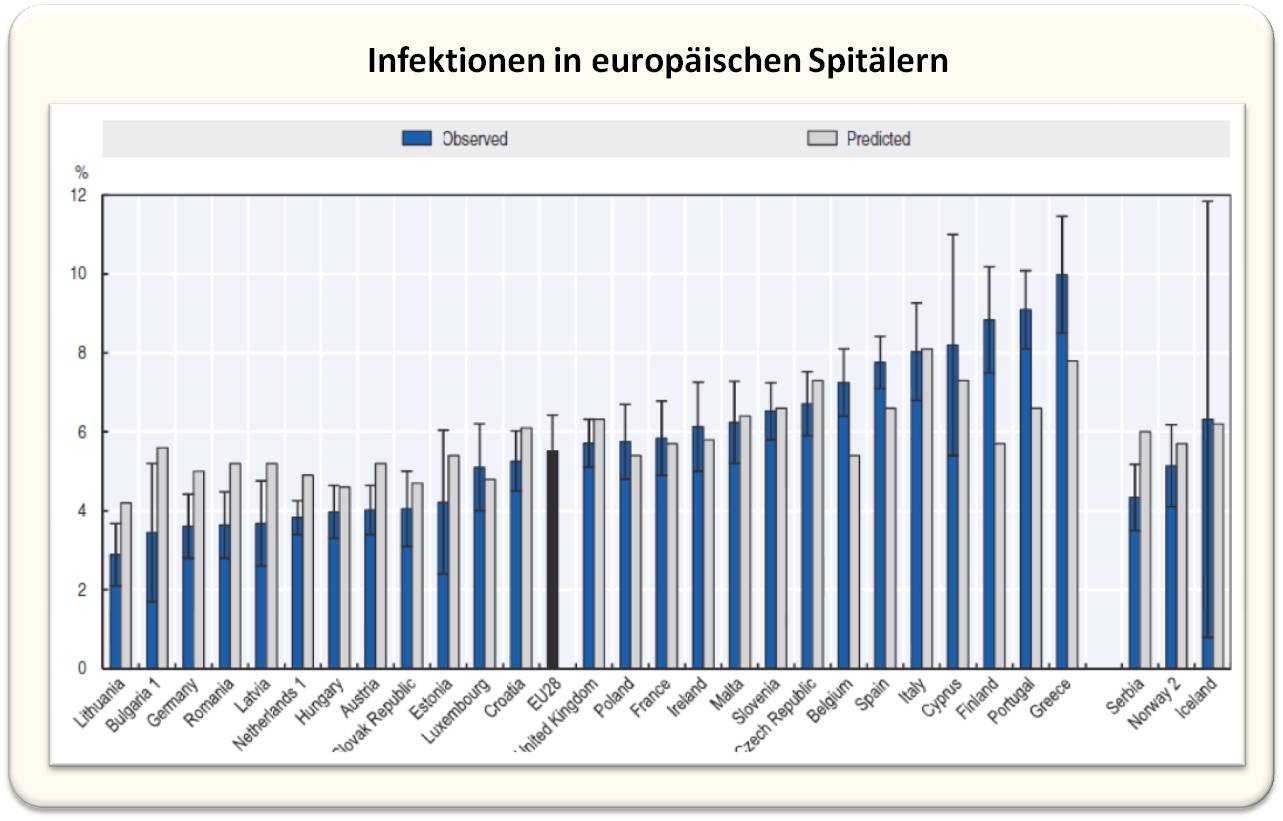
Abbildung 1. Anteil der Patienten, die im Zeitraum 2016 - 2017 zumindest an einer im Spital hervorgerufenen Infektion erkrankt sind. (Bild und Text von der Redaktion eingefügt, Quelle: ECDC 2016-17 Point prevalence survey)
Was ist die Ursache von Krankenhausinfektionen?
Während ihrer Assistenzzeit in der Inneren Medizin erweckten im Krankenhaus erworbene Infektionen das Interesse von Ami Bhatt (Stanford University, Palo Alto, Kalifornien). Als ihre Patienten Sepsis entwickelten, ging Bhatt daran die Ursache dafür festzustellen. Sie erkannte aber bald, dass es kompliziert werden würde den Ursprung der Infektion zu bestimmen.
Als Bhatt über mögliche Quellen der im Krankenhaus erworbenen Infektionen nachdachte, zog sie auch das Mikrobiom in Erwägung - die Tausenden von Mikroben, die auf ganz natürliche Weise in und auf dem menschlichen Körper leben. In zunehmendem Maße werden wir ja vieler wichtiger Funktionen des Mikrobioms gewahr, die es auf unseren Stoffwechsel, unsere Immunität und sogar auf unsere psychische Gesundheit ausübt. Bhatt überlegte nun, ob Keime aus dem Mikrobiom in den Blutkreislauf mancher Patienten gelangen könnten, insbesondere bei Patienten, deren Immunsystem bereits beeinträchtigt ist.
Die Studie an immunsupprimierten Patienten
Mit ihren Kollegen (darunter den Erstautoren der Studie Fiona Tamburini und Tessa Andermann) konzentrierte sich Bhatt auf den Darm, der ja natürlicher Lebensraum für viele Hunderte verschiedene Arten von Mikroben ist. Ihr Team rekrutierte Patienten, die sich im Stanford University Hospital einer Transplantation des Knochenmarks unterzogen und sammelte von ihnen wöchentliche Stuhlproben; jede dieser Proben enthielt eine Fülle mikrobiellen Lebens, das aus dem Darm stammte.
Patienten, die Knochenmark transplantiert bekommen, erhalten Medikamente, um das Immunsystem zu supprimieren, um ihren Organismus davon abzuhalten die kostbaren Spenderzellen zu attackieren. Aufgrund des supprimierten Immunsystems sind solche Patienten aber auch einem erhöhten Infektionsrisiko ausgesetzt.
Erkrankte nun ein Transplantationspatient an einer Sepsis - und zwar innerhalb von 30 Tagen nachdem man die Darmmikroben enthaltenden Stuhlproben gesammelt hatte -, so isolierten die Forscher das verursachende Bakterium aus dem Blut, brachten es Kultur und sequenzierten seine DNA.
Der nächste Schritt bestand dann darin, dass sie untersuchten ob es eine exakte Übereinstimmung zwischen der DNA des Infektionserregers und der DNA eines Bakteriums in der Stuhlprobe des Patienten geben könnte. Dies würde dann darauf hindeuten , dass der Infektionserreger aus dem Mikrobiom des Darms stammte.
Ein überaus schwieriges Unterfangen
Obwohl vom Konzept her simpel, war die Durchführung dieser Untersuchung dann alles andere als einfach. Die Forscher mussten ja die DNA eines einzelnen Infektionserregers mit all den DNA-Sequenzen vergleichen, die man von den Hunderten im Darm ansässigen Mikroben - dem Darmmikrobiom - bestimmt hatte. Es war eine Analyse, die zudem extreme Präzision erforderte. Es war eine Herausforderung, welche die Forscher so beschrieben: Man setzt viele Hunderte verschiedener Fotografien zusammen, die zuvor in kleine Stücke geschnitten, zusammengemischt und aufgeschüttelt worden waren, bevor man dann versucht die wieder hergestellten Fotos mit einem anderen Foto abzugleichen.
Die Forscher schafften diese schwierige Aufgabe mit ihrem Bioinformatik Tool StrainSifter. Sie konnten damit zeigen, dass in mehr als einem Drittel der Stuhlproben genau der gleiche Bakterienstamm enthalten war, der den jeweiligen Patienten krank gemacht hatte. Abbildung 2.
 Abbildung 2. Sepsis im Krankenhaus: Mittels eines neuen Bioinformatik Tools wurde nachgewiesen ob ein, in der Blutbahn entdeckter Infektionserreger aus dem Mikrobiom des Darms stammt. (Credit: Fiona Tamburini, Stanford University, Palo Alto, CA)
Abbildung 2. Sepsis im Krankenhaus: Mittels eines neuen Bioinformatik Tools wurde nachgewiesen ob ein, in der Blutbahn entdeckter Infektionserreger aus dem Mikrobiom des Darms stammt. (Credit: Fiona Tamburini, Stanford University, Palo Alto, CA)
Interessanterweise gab es aber kaum Anzeichen dafür, dass diese Stämme auch im Blut oder im Stuhl anderer Patienten im selben Krankenhaus gefunden wurden. Mit anderen Worten, die Keime schienen sich nicht von Person zu Person auszubreiten.
Die Ergebnisse weisen darauf hin,
dass viele der an Sepsis Erkrankten sich die Infektion nicht aus der Umgebung oder von einer anderen Person zugezogen hatten, sondern vielmehr aufgrund eines mikrobiellen Ungleichgewichts im eigenen Körper. Bhatt merkte an, dass die Studienteilnehmer im Krankenhaus häufig intensiv mit Antibiotika und anderen Medikamenten behandelt wurden. Ohne sorgfältige Behandlung könnten ihre Körper zu Brutstätten für infektiöse und antibiotikaresistente Bakterien werden.
Tatsächlich bestätigten die klinischen Befunde und die DNA-Daten, dass Antibiotika-resistente Stämme von Escherichia coli und Klebsiella-pneumoniae im Verdauungstrakt vorlagen, Keime, die häufige Ursachen für schwere Lungenentzündung, Harnwegsinfektionen und andere möglicherweise schwere Infektionen sind. Darüber hinaus fanden sich im Darm dieser Knochenmark-Empfänger auch andere Krankheitserreger, die man dort nicht vermutet hätte (beispielweise Pseuomonas aeruginosa und Staphylococcus epidermiis; von Rdn. ergänzt).
Fazit
Wenn optimale Hygienepraktiken auch nach wie vor für die Prävention von Krankenhausinfektionen entscheidend sind, so lassen die neuen Ergebnisse darauf schließen, dass diese Prävention komplizierter sein kann als man ursprünglich dachte. Um die Infektionsquelle korrekt zu identifizieren, kann es notwendig sein das individuelle Mikrobiom jedes Patienten in Betracht zu ziehen. Die gute Nachricht: mit den zunehmenden Möglichkeiten die Quelle von Blutinfektionen zu ermitteln, wird dies dem Gesundheitssystem helfen, gezieltere und effektivere Methoden zu entwickeln, um Krankenhausinfektionen künftig zu verhindern und in den Griff zu bekommen.
[1] Precision identification of diverse bloodstream pathogens in the gut microbiome. Tamburini FB, Andermann TM, Tkachenko E, Senchyna F, Banaei N, Bhatt AS. Nat Med. 2018 Oct 15. DOI:10.1038/s41591-018-0202-8.
[2] Health-care Associated Infection Data. Centers for Disease Control and Prevention.
[3] Estimating health care-associated infections and deaths in U.S. hospitals, 2002. Klevens RM, Edwards JR, Richards CL Jr, Horan TC, Gaynes RP, Pollock DA, Cardo DM. Public Health Rep. 2007 Mar-Apr;122(2):160-6.
* Dieser Artikel von NIH Director Francis Collins, M.D., Ph.D. erschien unter dem Titel: " Some ‘Hospital-Acquired’ Infections Traced to Patient’s Own Microbiome" " zuerst (am 23. Oktober 2018) im NIH Director’s Blog. https://directorsblog.nih.gov/2018/10/23/some-hospital-acquired-infections-traced-to-patients-own-microbiome/ Der Artikel wurde von der Redaktion möglichst wortgetreu aus dem Englischen übersetzt und geringfügig (mit Untertiteln) für den Blog adaptiert. Zur Illustration wurden Abbildung 1 (plus Text) von der Redaktion eingefügt. Reprinted (and translated by ScienceBlog) with kind permission from the National Institutes of Health (NIH).
Weiterführende Links
- National Institutes of Health (NIH) in Bethesda (Maryland).
- Bhatt Lab (Stanford University, Palo Alto, CA)
- OECD/EU (2018), Health at a Glance: Europe 2018: State of Health in the EU Cycle,
OECD Publishing, Paris
Artikel zu ähnlichen Themen im ScienceBlog
- Francis Collins, 18.09.2017 Ein erweiterter Blick auf das Mikrobiom des Menschen
- Redaktion, 10.05.2018: Anton Weichselbaum und das menschliche Mikrobiom - ein Vortrag vor 125 Jahren
- Redaktion, 22.11.2018: Eurobarometer 478: zum Wissenstand der EU-Bürger über Antibiotika, deren Anwendung und Vermeidung von Resistenzentstehung
- Inge Schuster, 23.09.2016: Gehen wir auf eine Post-Antibiotika Ära zu?
- Printer-friendly version
- Log in to post comments
