Fr, 27.05.2016 - 15:18 — Francis S. Collins
Lange vor den ersten Anzeichen von Gedächtnisproblemen erfolgen bei Alzheimerkranken bereits Veränderungen im Gehirn. Charakteristisch dafür sind zwei Typen unlöslicher Proteinablagerungen: beta-Amyloid Plaques ausserhalb und verklumpte Tau-Protein Fibrillen innerhalb der Nervenzellen des Gehirns. Francis Collins, Direktor der US National Institutes of Health, weist hier auf eine neue Studie hin, die Kartierungen dieser Ablagerungen mittels bildgebender Verfahren (PET- und MRI-Scans) ausgeführt hat. Die Anreicherung des Tau-Proteins im Schläfenlappen korreliert dabei eng mit den Symptomen des Gedächtnisverlustes. Demnach könnten PET-Scans der Tau-Protein Verteilung bereits frühzeitig Aussagen über das Stadium der Krankheit und Prognosen über deren Fortschreiten erlauben und das Ansprechen auf Therapien kontrollieren.
Viele Jahre bevor noch erste Anzeichen von Gedächtnisproblemen auftreten, setzen bei Menschen mit Alzheimerkrankheit bereits Veränderungen im Gehirn ein. Zu derartigen Veränderungen zählt eine allmähliche Ansammlung von beta-Amyloid Peptiden und Tau-Proteinen, die Plaques (unlöslichen Proteinablagerungen außerhalb der Nervenzellen, Anm. Red.) und verklumpte Tau-Fibrillen (innerhalb der Zellen, Anm. Red.) bilden und allgemein als Erkennungszeichen der Krankheit gelten. Während Amyloid-Plaques breite Aufmerksamkeit als frühe Anzeiger der Erkrankung erlangt haben, gab es bis vor Kurzem keine Möglichkeit die Zunahme von unlöslichem Tau-Protein im Gehirn eines lebenden Menschen zu bestimmen. Dementsprechend weiß man viel weniger über den Zeitablauf und die Verteilung der Tau-Protein Fibrillen und wie dies mit dem Gedächtnisverlust zusammenhängt.
Kartierung von Tau-Protein und beta-Amyloid
In einer eben erschienenen Untersuchung hat ein vom National Institute of Health (NIH) unterstütztes Forscherteam eine Reihe erster Kartierungen erstellt, die zeigen wo sich in frühen Stadien der Alzheimerkrankheit Tau-Proteine in den Gehirnen ansammeln [1]. Abbildung 1. Diese neuen Befunde weisen darauf hin, dass beta-Amyloid zwar ein verlässliches frühes Anzeichen der Alzheimerkrankheit darstellt, dass Tau-Protein aber wesentlich bessere Vorhersagen über das Nachlassen des Gedächtnisses eines Patienten und sein mögliches Ansprechen auf eine Therapie erlauben könnte.
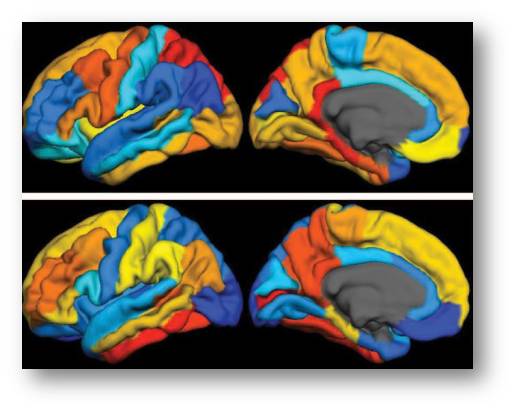 Abbildung 1. Positronen-Emissions-Tomographie (PET) zeigt die Verteilung von Tau-Protein (obere Reihe) und beta-Amyloid (untere Reihe) im Gehirn in einer frühen Phase der Alzheimerkrankheit. Rot: höchste Konzentration von Protein-gebundenem Diagnostikums, blau: niedrigste Konzentration, gelb. orange: mittlere Konzentrationen.(Credit: Brier et al., Sci Transl Med)
Abbildung 1. Positronen-Emissions-Tomographie (PET) zeigt die Verteilung von Tau-Protein (obere Reihe) und beta-Amyloid (untere Reihe) im Gehirn in einer frühen Phase der Alzheimerkrankheit. Rot: höchste Konzentration von Protein-gebundenem Diagnostikums, blau: niedrigste Konzentration, gelb. orange: mittlere Konzentrationen.(Credit: Brier et al., Sci Transl Med)
Ziel der von Beau Ances und Matthew Brier (Washington University, St. Louis) geleiteten Studie war es zu erkunden wie die Anhäufung von Tau-Proteinen und beta-Amyloid Plaques - auch wenn diese mit unterschiedlichen pathologischen Prozessen zusammenhängen - klinisch mit dem Fortschreiten der Alzheimerkrankheit korrelieren. Sie wandten dazu bildgebende Verfahren für beta-Amyloid und Tau-Protein an, wobei sie ein neu erhältliches Diagnostikum für das Tau-Protein anwandten: wenn dieses Diagnostikum intravenös injiziert wird, bindet es an das Tau-Protein und kann mittels Positronen-Emissions-Tomographie (PET) im Gehirn sichtbar gemacht werden.
Die Forscher untersuchten insgesamt 46 Personen mit einem Durchschnittsalter von 75 Jahren - 36 Personen dienten als gesunde Kontrolle, 10 litten laut Diagnose an einer leichten Form der Alzheimerkrankheit. Die Verteilung von beta-Amyloid und Tau-Protein im Gehirn wurde an den Studienteilnehmern jeweils mittels der bildgebenden Verfahren Magnetresonanz-Tomographie (MRI) und Positronen-Emissions-Tomographie visualisiert. Alle Teilnehmer unterzogen sich auch standardisierten Gedächtnistests auf Demenz. Zusätzlich erfolgten bei den meisten Teilnehmern die Bestimmung von beta-Amyloid und Tau-Protein in der Rückenmarksflüssigkeit und eine neuropsychologische Testung.
Verglichen mit den gesunden Kontrollen ließen die Gehirnaufnahmen der Patienten mit leichter Alzheimerkrankheit deutlich gestiegene Gehalte an Tau-Proteinen erkennen. Abbildung 2. Die Unterschiede waren insbesondere im Schläfenlappen zu beobachten, einer Gehirnregion, deren Rolle für das Gedächtnis bekannt ist. Die Forscher beobachteten auch Anstiege des beta-Amyloid an Personen mit Alzheimer, aber ebenso auch in einigen kognitiv nicht beeinträchtigten Personen. Derartige Amyloid-Plaques entwickelten sich besonders ausgeprägt in den Frontal- und Scheitellappen des Gehirns - Regionen, die für die Integration von Sinneswahrnehmungen und höhere kognitive Prozesse von zentraler Bedeutung sind, Gedächtnis und operative Funktionen miteingeschlossen. 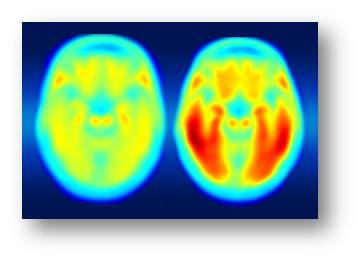
Abbildung 2. Zusammengesetztes PET-Scan Bild. (Zunehmende Intensität der Rotfärbung bedeutet mehr Tau-Protein.) Links: mittlere Tau-Proteinkonzentrationen von Personen mit normalen kognitiven Fähigkeiten, Rechts: gemittelte Tau-Proteinkonzentrationen von Personen mit milden Symptomen der Alzheimerkrankheit. (Credit: Matthew R. Brier, Washington University, St. Louis)
Anreicherung von Tau-Protein korreliert mit Symptomen des Gedächtnisverlustes
Obwohl beta-Amyloid und Tau-Protein tendenziell in unterschiedlichen Regionen des Gehirns akkumulieren, fanden die Forscher, dass die Anreicherung des Tau-Protein im Schläfenlappen eng mit den Symptomen des Gedächtnisverlustes korrelierte, die mit Hilfe standardisierter schriftlicher Tests für kognitive Fähigkeiten erhoben wurden. Die beta-Amyloid Aufnahmen zeigten dagegen nicht dieselbe Aussagekraft für die kognitiven Eigenschaften einer Versuchsperson.
Die auf PET-Imaging basierende Bestimmung der Gesamtbelastung mit Tau-Protein spiegelte genau die auf Grund von Analysen der Rückenmarksflüssigkeit erhaltenen Werte wider. Die Bilder bieten darüber hinaus aber mehr an Information: wo Tau-Protein zu akkumulieren ansetzt, wenn sich das Gedächtnis zu verschlechtern beginnt. Zweifellos sind weitere Untersuchungen an einer größeren Zahl von Probanden über einen größeren Zeitraum nötig.
Auf Grund ihrer Daten vermuten Ances und seine Kollegen, dass beta-Amyloid sich vorerst in diffuser Weise im ganzen Hirn anreichert. Gedächtnisprobleme tauchen erst später auf, dann wenn beide Typen von Ablagerungen - von Amyloid und Tau-Proteinen - in bestimmten Regionen des Gehirns vorliegen.
PET-Verfahren zur Diagnose, Prognose des Krankheitsverlaufs und Kontrolle der Wirksamkeit von Therapien
Die Amyloid-Visualisierung ist ein vielversprechendes Verfahren, um die Alzheimerkrankheit bereits in einer frühen Phase zu diagnostizieren. Menschen suchen den Arzt aber häufig erst dann auf, wenn bereits Probleme mit ihrem Gedächtnis begonnen haben. Hier kann die Visualisierung des Tau-Proteins ein wichtiges Mittel sein, um das Stadium der Erkrankung zu bestimmen. Mit dem Fortschritt in der Entwicklung neuer Alzheimer-Therapien - inklusive solcher, die gegen beta-Amyloid und Tau-Protein gerichtet sind - könnten PET-Verfahren sich sehr nützlich erweisen, um eine für den Patienten möglichst günstige Therapie auszuwählen und deren Wirksamkeit auf den weiteren Verlauf der Erkrankung zu kontrollieren.
Inzwischen unterstützt die Forschungsförderung des NIH gezielt PET-Imaging des Tau-Proteins in klinischen Studien. Ein wichtiges Beispiel dafür ist das Projekt "The Accelerating Medicines Partnership-Alzheimer’s Disease (AMP-AD) Biomarkers Project", das vom National Institute on Aging des NIH überwacht wird. Diese Projekt stellt ein Konsortium von drei klinischen Studien (in Phase II/III) dar, in welchen anti-Amyloid Therapien zur Prävention oder Verzögerung der Alzheimerkrankheit getestet werden. Das Imaging des Tau-Protein ist bereits in diese Studien aufgenommen. Der Fortschritt im Visualisieren von Tau-Protein und Prognostizieren von kognitivem Abbau könnte eine Hilfe für die rund 5 Millionen Amerikaner darstellen, die schon an der Alzheimerkrankheit leiden [2, 3 ]. Darüber hinaus wird diese Entwicklung den Forschern ein wichtiges Instrument in die Hand geben, um eine Reihe neuer präventiver Therapien zu testen, deren Entwicklung höchste Priorität hat.
[1] Tau and Aβ imaging, CSF measures, and cognition in Alzheimer’s disease. Brier MR, Gordon B, Friedrichsen K, McCarthy J, Stern A, Christensen J, Owen C, Aldea P, Su Y, Hassenstab J, Cairns NJ, Holtzman DM, Fagan AM, Morris JC, Benzinger TL, Ances BM. Sci Transl Med. 2016 May 11;8(338):338ra66.
[2] Alzheimer disease in the United States (2010–2050) estimated using the 2010 census. Hebert LE, Weuve J, Scherr PA, Evans DL.Neurology. 2013 May 7;80:1778-1783.
[3] Alzheimer’s Disease. Centers for Disease Control and Prevention. 2016 March 5.
* Dieser Artikel von NIH Director Francis Collins, M.D., Ph.D. erschien zuerst (am. 24. Mai 2016) im NIH Director’s Blog, https://directorsblog.nih.gov/2016/05/24/alzheimers-disease-tau-protein-... . Reprinted (and translated by ScienceBlog) with permission from the National Institutes of Health (NIH).
Im Artikel angeführte Links:
- Alzheimer’s Disease Fact Sheet (National Institute on Aging/NIH) https://www.nia.nih.gov/alzheimers/publication/alzheimers-disease-fact-s...
- Beau Ances (Washington University School of Medicine, St. Louis) https://neuro.wustl.edu/research/research-labs-2/ances-laboratory/
- Accelerating Medicines Partnership (NIH) https://www.nih.gov/research-training/accelerating-medicines-partnership.... NIH Support: National Institute on Aging; National Institute of Neurological Disorders and Stroke; National Center for Advancing Translational Science
Weiterführende Links
National Institutes of Health (NIH). https://www.nih.gov/
Alzheimer: Eine dreidimensionale Entdeckungsreise. Video 6:28 min. https://www.youtube.com/watch?v=paquj8hSdpc
Tau-Protein gegen Gedächtnisverlust (ohne Ton). Max-Planck Film 1:44 min, http://www.mpg.de/4282188/Tau-Protein_gegen_Gedaechtnisverlust
Planet Wissen - Diagnose Alzheimer .Video 58:17 min, https://www.youtube.com/watch?v=mp9A2esKt-A
Francis Collins: Wir brauchen bessere Medikamente – und zwar sofort (TEDMED 2012) Video 14:33 min. https://www.ted.com/talks/francis_collins_we_need_better_drugs_now?langu...
Artikel im ScienceBlog
Gottfried Schatz: 03.07.2015: Die bedrohliche Alzheimerkrankheit — Abschied vom Ich. http://scienceblog.at/die-bedrohliche-alzheimerkrankheit.
- Printer-friendly version
- Log in to post comments

