Do, 24.11.2016 - 14:27 — Francis S. Collins

![]() Wahrscheinlich können Sie sich nicht mehr erinnern, wann Sie als Kind das erste Mal Grippe hatten. Neue Erkenntnisse sprechen dafür, dass das menschliche Immunsystem jedoch seine erste Begegnung mit einem Grippevirus niemals vergisst. Es nützt dieses immunologische "Gedächtnis" möglicherweise sogar, um gegen künftige Infektionen mit neuen Stämmen der Vogelgrippe zu schützen. Diese eben erschienenen, grundlegenden Ergebnisse einer NIH-unterstützten Untersuchung fasst der Chemiker und Mediziner Francis Collins, Direktor der US National Institutes of Health (NIH) und ehem. Leiter des "Human Genome Project" hier zusammen.*
Wahrscheinlich können Sie sich nicht mehr erinnern, wann Sie als Kind das erste Mal Grippe hatten. Neue Erkenntnisse sprechen dafür, dass das menschliche Immunsystem jedoch seine erste Begegnung mit einem Grippevirus niemals vergisst. Es nützt dieses immunologische "Gedächtnis" möglicherweise sogar, um gegen künftige Infektionen mit neuen Stämmen der Vogelgrippe zu schützen. Diese eben erschienenen, grundlegenden Ergebnisse einer NIH-unterstützten Untersuchung fasst der Chemiker und Mediziner Francis Collins, Direktor der US National Institutes of Health (NIH) und ehem. Leiter des "Human Genome Project" hier zusammen.*
Ein NIH-unterstütztes Forschungsteam hat Fälle von Vogelgrippe zwischen 1997 und 2015 in sechs Ländern in Asien und dem mittleren Osten untersucht und gesehen, dass vor 1968 geborene Menschen ein geringeres Risiko hatten an H5N1-Vogelgrippe schwer zu erkranken oder daran zu sterben, als die später geborenen. Genau das Gegenteil war bei dem Vogelgrippestamm H7N9 der Fall: die vor 1968 Geborenen hatten ein wesentlich höheres Risiko, während die später Geborenen häufig besser geschützt waren.
Wie kommt dieser Gegensatz zustande?
Es zeigt sich, dass das H5N1-Vogelgrippevirus (Abbildung 1) näher verwandt ist zu dem Virus der saisonalen Grippe, die vor 1968 dominierte und dass danach zwei saisonale Grippestämme überwogen, die mehr dem H7N9 -Vogelgrippevirus ähnelten. Dies bedeutet, dass die erste Erfahrung mit der Grippe und die sich daraus entwickelnde Immunität Jahrzehnte später über Leben und Tod entscheiden können, wenn der Mensch dann einem völlig neuen Influenzastamm ausgesetzt ist.
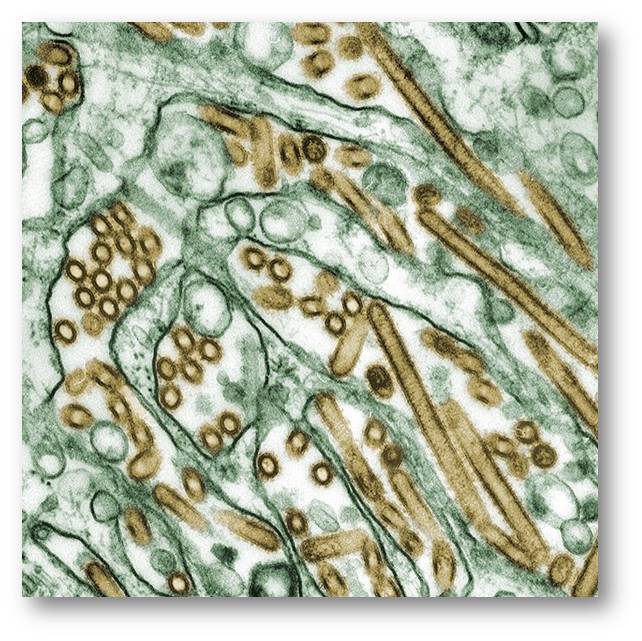 Abbildung 1. Wie H5N1-Vogelgrippeviren aussehen. Die Viren haben sich in einer MDCK Zellkultur (eine Nierenzelllinie des Hundes) vermehrt. Anfärbung: Viren: (goldfarben), MDCK Zellen: grün; Transmissionselektronenmikroskopie. Credit: Cynthia Goldsmith, CDC
Abbildung 1. Wie H5N1-Vogelgrippeviren aussehen. Die Viren haben sich in einer MDCK Zellkultur (eine Nierenzelllinie des Hundes) vermehrt. Anfärbung: Viren: (goldfarben), MDCK Zellen: grün; Transmissionselektronenmikroskopie. Credit: Cynthia Goldsmith, CDC
Diese Ergebnisse haben bedeutende Auswirkungen auf öffentliche Gesundheitsinitiativen, um diejenigen zu schützen, die bei einer künftigen Influenza-Pandemie das höchste Risiko tragen. Die Ergebnisse bieten auch wichtige Einsichten zur Entwicklung universeller Influenzavakzinen, die vor einem weiten Spektrum an Influenzastämmen Schutz bieten könnten.
In welchem Alter sind Menschen am stärksten von Virusgrippe betroffen?
Darüber haben Forscher lange gerätselt. Als das klassische Beispiel, die H1N1-Grippeepidemie im Jahr 1918 Millionen Menschen tötete, waren dies zumeist Erwachsene im Alter von 20 - 30 Jahren. Auch an der H5N1-Vogelgrippe erkrankten mehr Kinder und junge Erwachsene, dagegen betraf H7N9 häufiger ältere Leute.
In einem eben im Journal Science erschienenen Artikel [1] haben James Lloyd-Smith und Kollegen von der University of California, Los Angeles und Michael Worobey von der University of Arizona, Tucson die Vermutung aufgestellt, dass diese eigenartigen Infektionsmuster mehr mit den unterschiedlichen Virusstämmen der Erstinfektion zu tun haben als mit Alter der Menschen. Um diese Möglichkeit zu prüfen, haben die Forscher die Geschichte der saisonalen Grippe in Kambodscha, China, Ägypten, Indonesien, Thailand und Vietnam seit dem Jahr 1918 rekonstruiert. Sodann trugen sie alle bekannt gewordenen Vogelgrippe-Erkrankungen durch H5N1 und H7N9 (1997 erfolgte der Übergang von H5N1 auf den Menschen) zusammen und stellten sie den Geburtsjahren der betroffenen Patienten gegenüber. Abbildung 2.
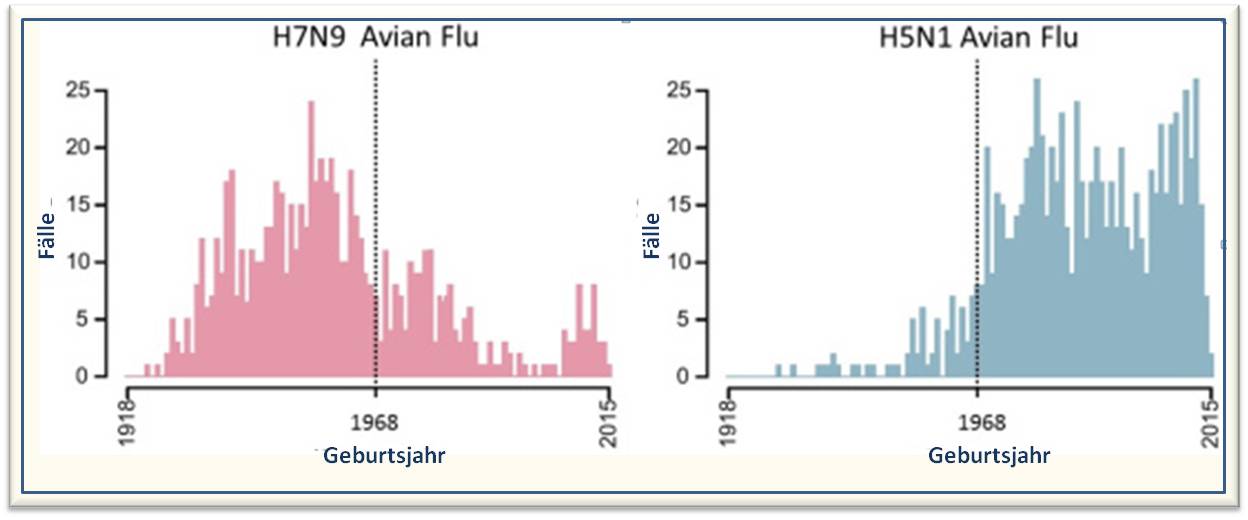 Abbildung 2. Links: Geburtsjahre von in China lebenden Menschen, die zwischen 1997 und 2015 an der H7N9 Vogelgrippe erkrankten. Rechts: Geburtsjahre von Menschen in Kambodscha, China, Ägypten, Indonesien, Thailand und Vietnam, die zwischen 1997 und 2015 an der H5N1 Vogelgrippe erkrankten. (Quelle: adaptiert aus Science. 2016 Nov 11;354(6313):722-726) Die Daten zeigten, dass eine klarer Zusammenhang zwischen der ersten Begegnung einer Person mit Influenza und späteren Infektionen besteht. Der 1968 beobachtete, plötzliche Sprung in der Anfälligkeit für Grippeinfektionen, lässt sich mit einer abrupten Veränderung in der Häufigkeit der saisonalen Influenzastämme erklären. In diesem Jahr hatte eine Pandemie mit dem H3N2-Stamm - die sogenannte Hongkong-Grippe - die saisonalen Grippestämme H2N2 und H1N1 vollständig abgelöst, die vorher im Umlauf waren.
Abbildung 2. Links: Geburtsjahre von in China lebenden Menschen, die zwischen 1997 und 2015 an der H7N9 Vogelgrippe erkrankten. Rechts: Geburtsjahre von Menschen in Kambodscha, China, Ägypten, Indonesien, Thailand und Vietnam, die zwischen 1997 und 2015 an der H5N1 Vogelgrippe erkrankten. (Quelle: adaptiert aus Science. 2016 Nov 11;354(6313):722-726) Die Daten zeigten, dass eine klarer Zusammenhang zwischen der ersten Begegnung einer Person mit Influenza und späteren Infektionen besteht. Der 1968 beobachtete, plötzliche Sprung in der Anfälligkeit für Grippeinfektionen, lässt sich mit einer abrupten Veränderung in der Häufigkeit der saisonalen Influenzastämme erklären. In diesem Jahr hatte eine Pandemie mit dem H3N2-Stamm - die sogenannte Hongkong-Grippe - die saisonalen Grippestämme H2N2 und H1N1 vollständig abgelöst, die vorher im Umlauf waren.
Darüber, wie die erste Infektion zu einer lebenslangen Immunität einer Person führt, müssen noch detaillierte Kenntnisse gesammelt werden. Zweifellos hängt dieser Vorgang mit der unterschiedlichen Art und Weise zusammen, wie menschliche Antikörper ein spezielles, auf der Virusoberfläche sitzendes Protein - Hemagglutinin - erkennen und darauf reagieren. Jedes Influenzavirus träg eines von 18 unterschiedlichen Typen des Hemagglutinin auf seiner Oberfläche (der Buchstabe "H" gefolgt von einer Nummer charakterisiert den Hemagglutinintyp in der Bezeichnung des Virusstammes). Dabei lassen sich alle 18 Hemagglutinintypen in nur zwei größere Gruppen einteilen: die saisonalen Grippeviren H1 und H2 und der Vogelgrippestamm H5 fallen in eine Gruppe, der saisonale H3-Stamm und das Vogelgrippevirus H7 in die andere Gruppe.
Die in den verschiedenen Ländern erhobenen Infektionsmuster zeigen, dass ein früher Kontakt zu einem bestimmten Influenzastamm einigen Schutz gegen andere Stämme bietet, sofern diese in dieselbe Hemagglutinin-Gruppe fallen (ein als Kreuzreaktivität bekanntes Phänomen). Nach Schätzungen der Forscher kann eine korrekte Prägung des Immunsystems auf ein Hemagglutinin der Gruppe 1 oder 2 einen 75 prozentigen Schutz vor einer schweren Infektion mit H5N1 oder H7N9 und 80 % Schutz vor möglichen Todesfolgen bieten.
In vielerlei Hinsicht sind dies gute Nachrichten.
Wenn dieser Effekt auch auf andere Influenzastämme zutrifft, so sollte es keine komplett neue Grippeepidemie geben. Sogar neue Viren, die noch nie Menschen infiziert haben, werden Charakteristika aufweisen, gegen die einige unserer Immunsysteme geprägt worden sind. Dies bedeutet nicht zwangsweise, dass die mit diesen Viren infizierten Menschen nicht erkranken können, die Grippe wird aber bei denen, die einigen Schutz entwickelt haben, voraussichtlich glimpflicher verlaufen.
Weiters zeigen die Daten, dass ein breiter, lang anhaltender immunologischer Schutz erreicht werden kann. Dieser Schutz basiert offensichtlich auf einem bestimmten Abschnitt des Hemagglutininmoleküls , der bereits vielen Forschern als Zielstruktur für eine universell wirkende Vakzine dient (siehe Artikel im ScienceBlog: http://scienceblog.at/influenza-viren-%E2%80%93-pandemien-sind-universel... ; Anm. Red.) Was sich allerdings zeigt: unsere früheste Begegnung mit Grippeviren prägt unser Immunsystem in einer Weise, die kaum ausgeweitet oder überboten werden kann.
Was eine universell wirksame Influenzavakzine betrifft, so wird diese - in Gegenwart eines bereits existierenden Immungedächtnisses - einen breiten Immunschutz stimulieren müssen, der stärker ist, als ihn Influenzainfektionen im späteren Leben bewirken können. Dies wird verständlich, wenn man vor 1968 geborene Personen betrachtet: diese waren zuerst H1 oder H2 Influenzastämmen ausgesetzt und später, über Jahrzehnte hinweg, den dominierenden saisonalen H3-Stämmen. Die spätere H3-Exposition reichte demnach nicht aus, um diese Menschen zu schützen, als H7N9 auftauchte.
Es ist noch nicht klar, was die Ergebnisse für das Risiko des Einzelnen bedeuten, an einer schweren saisonalen Grippe erkranken. Das ist eine sehr wichtige Frage - immerhin sterben weltweit jährlich bis zu 500 000 Menschen an Grippe [2]. Lloyd-Smith und Worobey meinen dazu, dass man in Zukunft die früheste Influenzainfektion einer Person berücksichtigen sollte, um die beste saisonale Influenza-Vakzine zu wählen - eine Vakzine die das Immunsystem in genau den Bereichen stärken sollte, in denen es Schwächen zeigt.
Im Licht der neuen Ergebnisse sind viele neuen Fragen aufgetaucht und viel Forschungsarbeit ist zu tun. Es gibt auch einige offensichtliche Konsequenzen. H5N1 und H7N9 haben weltweit bereits Hunderte Menschen infiziert. Sollte eines der Viren mutieren und leichter vom Vogel auf den Menschen übergehen, könnte dies die nächste Pandemie verursachen. Die beschriebene Untersuchung zeigt, dass eine sorgfältige Analyse von existierenden Gesundheitsdaten der Bevölkerung in Verbindung mit mathematischen Modellierungen der Krankheitsübertragung es bereits möglich macht, bessere Voraussagen zu treffen und Pläne für derartige Risiken zu entwickeln.
*Dieser Artikel von NIH Director Francis Collins, M.D., Ph.D. erschien unter dem Titel:" Birth Year Predicts Bird Flu Risk" zuerst (am 22. Novemberi 2016) im NIH Director’s Blog:. https://directorsblog.nih.gov/2016/11/22/birth-year-predicts-bird-flu-risk/ . Reprinted (and translated by ScienceBlog) with permission from the National Institutes of Health (NIH).
[1] Potent protection against H5N1 and H7N9 influenza via childhood hemagglutinin imprinting. Gostic KM, Ambrose M, Worobey M, Lloyd-Smith JO. Science. 2016 Nov 11;354(6313):722-726. (open access)
[2] Influenza (Seasonal). World Health Organization. March 2014.
Weiterführende Links
- Influenza (National Institute of Allergy and Infectious Diseases, NIH),
- Lloyd-Smith Lab (University of California, Los Angeles)
- Michael Worobey (University of Arizona, Tucson)
- Influenza - Die Angriffstaktik des Virus. Video 1:25 min.
Artikel im ScienceBlog
- Peter Palese, 10.05.2013: Influenza-Viren – Pandemien: sind universell wirksame Impfstoffe in Reichweite?
- Printer-friendly version
- Log in to post comments
