Fr, 03.07.2015 - 09:49 — Gottfried Schatz 
![]()
Unser Gehirn droht im Alter zu versagen. Die häufigste Form von geistigem Verfall ist die Alzheimerkrankheit, die wegen der Überalterung der Bevölkerung immer häufiger wird. Ihre Ursache ist noch unbekannt. Der renommierte Biochemiker Gottfried Schatz beschreibt die aktuellen Ansätze, welche das Krankheitsbild auf molekularem Niveau zu erklären versuchen, um auf dieser Basis therapeutische Strategien zu entwickeln.
«Ich beginne nun die Reise, die mich zum Sonnenuntergang meines Lebens führt, in der Gewissheit, dass über Amerika immer wieder ein strahlender Morgen heraufdämmern wird.» Mit diesen bewegenden Worten gestand der dreiundachtzigjährige ehemalige US-Präsident Ronald Reagan der amerikanischen Öffentlichkeit seine Alzheimer-Erkrankung, an deren Folgen er zehn Jahre später sterben sollte. Auf seiner tragischen Reise war er nicht allein; zeitgleich mit ihm litten mindestens zwanzig Millionen Menschen an dieser Krankheit.
Der junge Münchner Psychiater Alois Alzheimer beschrieb sie zum ersten Mal am 3. November 1906 vor einer Versammlung südwestdeutscher Irrenärzte und veröffentlichte dann seine Befunde in einem kurzen Artikel mit dem Titel «Über eine eigenartige Erkrankung der Hirnrinde». Der Artikel schloss mit den prophetischen Worten: «Es gibt ganz zweifelsfrei viel mehr psychische Krankheiten, als sie unsere Lehrbücher aufführen.»
Eiweissablagerungen
Die Alzheimerkrankheit lässt sich heute weder heilen noch wirksam behandeln. Versuche, ihr Fortschreiten wesentlich zu verlangsamen, hatten bisher nur mässigen Erfolg. Nach der ersten Diagnose sterben die Patienten im Durchschnitt nach sechs bis zehn Jahren, meist an infizierten Liegewunden oder einer Lungenentzündung. Ihr Gehirn ist durch das massive Absterben von Nervenzellen deutlich geschrumpft. Dies erklärt den geistigen Verfall, der sich gewöhnlich mit einem Verlust des Gedächtnisses und anderer Hirnleistungen ankündigt und schliesslich zu völliger Teilnahmslosigkeit führt. 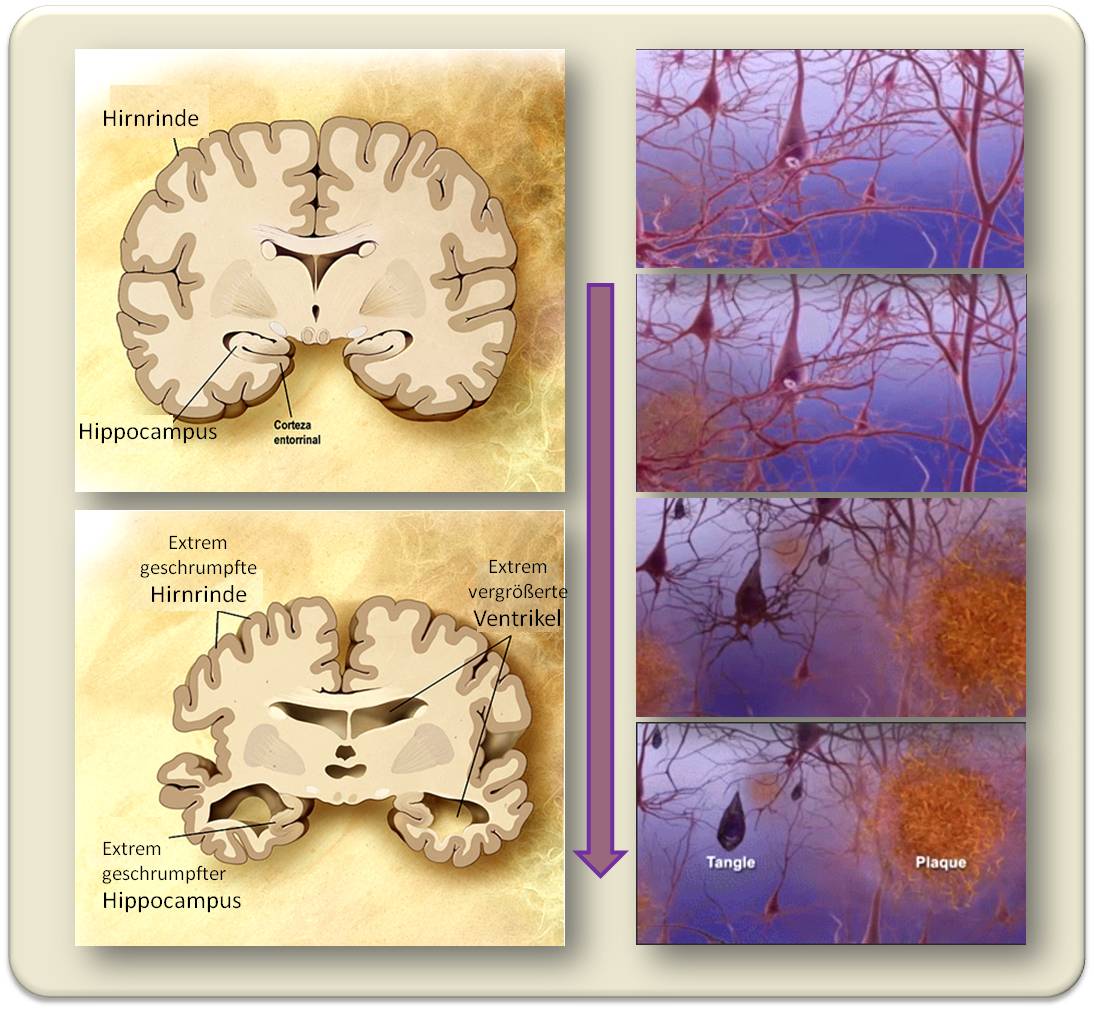
Abbildung 1. Das Gehirn schrumpft durch das massive Absterben von Nervenzellen (links). Rechts: Unlösliche Proteinablagerungen außerhalb der Nervenzellen – Plaques – und Bildung von verklumpten Tau-Fibrillen in den Zellen (siehe auch Abb. 2), die zu deren Absterben führen. (Bild: modifiziert nach Wikipedia)
Charakteristisch für die Krankheit sind zwei Typen von unlöslichen Proteinablagerungen, eine ausserhalb und eine innerhalb der Nervenzellen des Gehirns. Die äusseren Ablagerungen – die «Plaques» – sind verklumpte, abnormale Spaltprodukte eines Proteins, das fest in der Oberflächenmembran der Nervenzellen verankert ist und wie eine Mobilfunkantenne aus dieser herausragt. Wir wissen noch nicht mit Sicherheit, welche Funktion dieses Protein im gesunden Gehirn erfüllt, vermuten aber, dass es die Vernetzung von Gehirnzellen fördert. Sein offizieller Name ist «Amyloid-Precursor-Protein» – oder kurz «APP». Wie fast jedes Protein wird APP laufend abgebaut und neu gebildet. Der normale Abbau liefert lösliche Spaltprodukte, die von der Zelle schnell entsorgt werden und unschädlich sind. Bei Alzheimerkranken führt der Abbau jedoch zu einem abnormalen Spaltprodukt, dem Beta-Amyloid, das sich zu unlöslichen Plaques zusammenklumpt, die von der Zelle nicht weiter abgebaut werden können und diese schliesslich töten.
Die Proteinablagerungen innerhalb der Gehirnzellen bestehen aus einem Protein, das normalerweise das innere Stützgerüst der Nervenzellen festigt und es den Zellen ermöglicht, lange Ausstülpungen zu bilden und über diese mit anderen Nervenzellen elektrische Kontakte auszubilden. Dieses stützende «Tau-Protein» ist bei Alzheimerkranken chemisch verändert, so dass es sich nicht mehr an das innere Stützgerüst der Zellen anlagert, sondern unlösliche Neurofibrillen im Inneren der Zellen bildet und so deren elektrische Vernetzung verhindert. 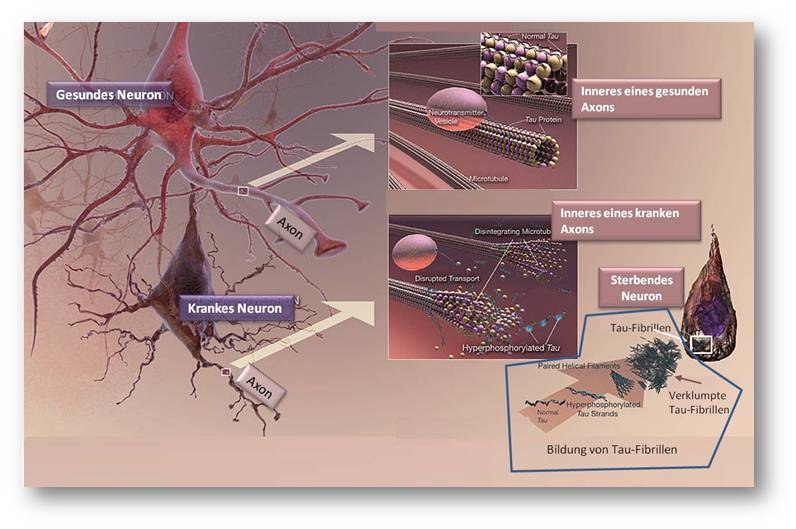 Abbildung 2. Das Tau-Proteins festigt normalerweise das Stützgerüst (Mikrotubuli) der Nervenzelle (Neuron). Veränderungen im Tau-Protein führen zur Bildung von verklumpten Fibrillen im Zellinneren (Ausschnitte aus dem Axon rechts vergrößert), zum Zerfall der Mikrotubuli, das Neuron stirbt (ganz rechts). (Quelle: http://www.nia.nih.gov/alzheimers/publication/alzheimers-disease-unravel..., gemeinfrei).
Abbildung 2. Das Tau-Proteins festigt normalerweise das Stützgerüst (Mikrotubuli) der Nervenzelle (Neuron). Veränderungen im Tau-Protein führen zur Bildung von verklumpten Fibrillen im Zellinneren (Ausschnitte aus dem Axon rechts vergrößert), zum Zerfall der Mikrotubuli, das Neuron stirbt (ganz rechts). (Quelle: http://www.nia.nih.gov/alzheimers/publication/alzheimers-disease-unravel..., gemeinfrei).
Die Ursachen all dieser Veränderungen und des damit verbundenen geistigen Verfalls sind noch nicht mit Sicherheit bekannt. Es mehren sich jedoch die Hinweise, dass die Krankheit von einer Veränderung – einer Mutation – gewisser Gene begleitet ist. Gene sind meist Baupläne für bestimmte Proteine. In Familien, in denen die Alzheimerkrankheit ungewöhnlich häufig und typischerweise bereits im Alter von vierzig bis fünfzig Jahren auftritt, ist mindestens eines von drei Genen mutiert. Eines von ihnen trägt den Bauplan für das erwähnte APP, so dass eine Mutation in diesem Gen zu einem abnormalen APP führt, das offenbar nicht zu harmlosen Spaltprodukten, sondern zu unlöslichen Plaques abgebaut wird. Tatsächlich entwickelt eine Maus, der man dies mutierte menschliche APP-Gen mit gentechnischen Methoden einpflanzt, Lerndefizite und Plaques im Gehirn.
Das Gen für APP befindet sich auf Chromosom 21, von dem etwa 0,1 Prozent aller Menschen nicht die üblichen zwei, sondern drei Exemplare besitzen. Diese Trisomie 21 (auch «Down-Syndrom» genannt) führt wahrscheinlich zu einer Überproduktion und, als Folge davon, zu einem abnormalen Abbau von APP, so dass fast alle vom Down-Syndrom Betroffenen vor ihrem vierzigsten Lebensjahr Alzheimerdemenz entwickeln. Die beiden anderen Gene, die in Familien mit gehäufter und früh einsetzender Alzheimerkrankheit mutiert sind, tragen die Namen «Präsenilin-1» und «Präsenilin-2». Sie bestimmen die Struktur von Proteinen, die im Verein mit anderen Proteinen normales APP abbauen. Wenn sie durch eine Mutation verändert sind, spalten sie APP an den falschen Stellen, so dass die Spaltprodukte wiederum unlösliche Plaques bilden. Plaques können sich also als Folge einer veränderten APP-Struktur, einer Überproduktion von APP oder einer veränderten Abbaumaschine bilden. Derart klare genetische Korrelationen finden sich jedoch nur bei einer sehr kleinen Minderheit von Alzheimerpatienten. In den meisten Fällen sind wahrscheinlich andere Gene, Krankheiten wie Bluthochdruck sowie Lebensstil und Umweltfaktoren beteiligt.
Warum hat die Evolution die Gene, welche Alzheimerkrankheit verursachen oder das Risiko für sie erhöhen, nicht völlig ausgemerzt? Ein Grund ist wahrscheinlich, dass diese Gene in früheren Zeiten ihre Wirkung nur sehr selten entfalten konnten, weil die meisten ihrer Träger vor Ausbruch der Krankheit starben – und heute zeigt sich die Wirkung dieser Gene in den meisten Fällen erst in einem Lebensabschnitt, in dem die Betroffenen keine Kinder mehr zeugen. Damit schlagen diese Gene der biologischen Selektion ein Schnippchen. Ein zweiter Grund könnte sein, dass einige dieser Gene unserem Körper auch nützen können. Die Spaltprodukte von APP zerstören die Zellmembran von Bakterien und wirken deshalb bakterizid. Wahrscheinlich trifft dies nicht nur für die normalen, sondern auch für die abnormalen APP-Spaltprodukte zu. Diese Abbauprodukte könnten also ein Verteidigungssystem sein, mit dem unser Gehirn eindringende Bakterien bekämpft. Sollte diese Vermutung zutreffen, dann wäre eine Alzheimer-Erkrankung die Entgleisung einer Verteidigungsstrategie unseres Körpers, die uns schweren Schaden zufügt. Ähnliches gilt auch für das Immunsystem, das sich gelegentlich nicht nur gegen eindringende Viren und Bakterien, sondern auch gegen uns selbst richtet und lebensbedrohende Autoimmunerkrankungen auslösen kann.
Die abnormalen APP-Abbauprodukte bilden aber nicht nur unlösliche Plaques ausserhalb der Nervenzellen, sondern können vielleicht sogar in diese eindringen und die Funktion der Mitochondrien stören. Mitochondrien sind die Organe der Zellatmung, die unseren Zellen die lebensnotwendige Energie liefern. Ist ihre Funktion beeinträchtigt, kommt es nicht nur zu einer Energiekrise, sondern auch zur Freisetzung stark oxidierender Nebenprodukte der Atmung, die den Zellstoffwechsel hemmen und die Zellen abtöten. Eine solche Störung der Mitochondrien ist aber noch nicht gesichert, und wir wissen auch nicht, ob sie Ursache oder Folge der Alzheimerkrankheit wäre.
Eine eindeutige Früherkennung der Krankheit ist selbst heute noch schwierig. Sie stützt sich auf Auffälligkeiten in neuropsychologischen Tests oder einen verringerten Zuckerverbrauch bestimmter Gehirnregionen. Zunehmend wichtig werden auch der Nachweis abnormaler APP-Spaltprodukte oder veränderter Tau-Proteine im Nervenwasser sowie bildgebende Verfahren, welche die Plaques im Patientengehirn sichtbar machen. Allerdings ist die Frühdiagnose einer unheilbaren Krankheit, deren Verlauf sich nicht wesentlich beeinflussen lässt, grundsätzlich fragwürdig. Eine eindeutige Diagnose ist erst nach dem Tod der Patienten durch eine histologische Untersuchung des Gehirns möglich.
Beunruhigende Fragen
In Europa und den USA ist Alzheimerdemenz eine der kostspieligsten Krankheiten. Die USA geben gegenwärtig für die Betreuung von Alzheimerpatienten jährlich etwa hundert Milliarden Dollar aus. Wenn die Überalterung der amerikanischen Gesellschaft wie erwartet weiter zunimmt und es nicht bald wirksame Waffen gegen Alzheimerdemenz gibt, dürfte diese Summe bis zum Jahr 2050 etwa zehnmal höher sein. Im Durchschnitt litte dann jeder hundertste Amerikaner an Alzheimerdemenz. Rund zwei Drittel der medizinischen Kosten entfallen auf die langfristige Pflege, die das Pflegepersonal bis an seine physischen und psychischen Grenzen belastet. Die psychische Belastung der Pfleger ist bei der Betreuung von Alzheimerpatienten in der letzten Krankheitsphase wahrscheinlich noch höher als bei Patienten, die ohne Hoffnung auf Gesundung völlig gelähmt oder jahrelang bewusstlos sind. In Japan mit seiner stark überalterten Bevölkerung ist die Betreuung von Alzheimerkranken besonders prekär, weil das Land den Mangel an eigenen Pflegern nur ungern durch Fachkräfte aus dem Ausland ausgleicht. Japanische Firmen entwickeln deshalb Pflegeroboter, die in Gestalt eines putzigen Bären oder eines anderen Kuscheltieres Kranke aus ihrem Bett heben und in dieses zurücklegen und auch andere Tätigkeiten menschlicher Pfleger wahrnehmen.
Was aber ist der angemessene Umgang mit Menschen, die ihre Funktionen, welche das Menschsein ausmachen, verloren haben? Worin besteht dieses Menschsein? Und wann hört ein Mensch auf, Mensch zu sein? Diese Fragen führen unmittelbar zu jener nach dem würdigen Ende unseres Lebens und – zumindest für mich persönlich und mit aller Vorsicht gesagt – zu der Möglichkeit, dieses Leben freiwillig beenden zu dürfen. Ich wage es kaum, diese beunruhigenden Fragen zu denken, doch unseren Kindern und Enkelkindern wird es wohl nicht erspart bleiben, sie zu beantworten.
Weiterführende Links
Alzheimer: Eine dreidimensionale Entdeckungsreise. Video 6:28 min. https://www.youtube.com/watch?v=paquj8hSdpc
Tau-Protein gegen Gedächtnisverlust (ohne Ton). Max-Planck Film 1:44 min, http://www.mpg.de/4282188/Tau-Protein_gegen_Gedaechtnisverlust
Planet Wissen - Diagnose Alzheimer .Video 58:17 min, https://www.youtube.com/watch?v=mp9A2esKt-A
- Printer-friendly version
- Log in to post comments
