Do, 06.02.2020 — Redaktion
Die Blut-Hirn-Schranke ist eine hoch entwickelte Barriere aus verschiedenen Zelltypen, die den Durchtritt von Molekülen - beispielsweise von Arzneimitteln gegen neurodegenerative Erkrankungen oder Hirnverletzungen - vom Blut ins Gehirn stoppen. Mit dem Ziel diese Barriere für bestimmte Substanzen selektiv durchlässig zu machen, laufen zwei EU-Projekte: i) es soll ein in vitro-Modell der Blut-Hirn-Schranke aufgebaut werden, das verlässlichere Vorhersagen zur in vivo Wirksamkeit hirnaktiver Substanzen erlaubt, ii) Leuchtende Nanopartikeln sollen als Sonde das Durchqueren der Blut-Hirn-Schranke direkt in Echtzeit sichtbar machen.*
Ein neues Medikament gegen Alzheimer, Schlaganfall oder Hirnverletzungen mag unter Laborbedingungen vielleicht gut funktionieren, entscheidend ist aber die Untersuchung, ob es dort hinkommt, wo es hinkommen muss. (Abbildung 1)
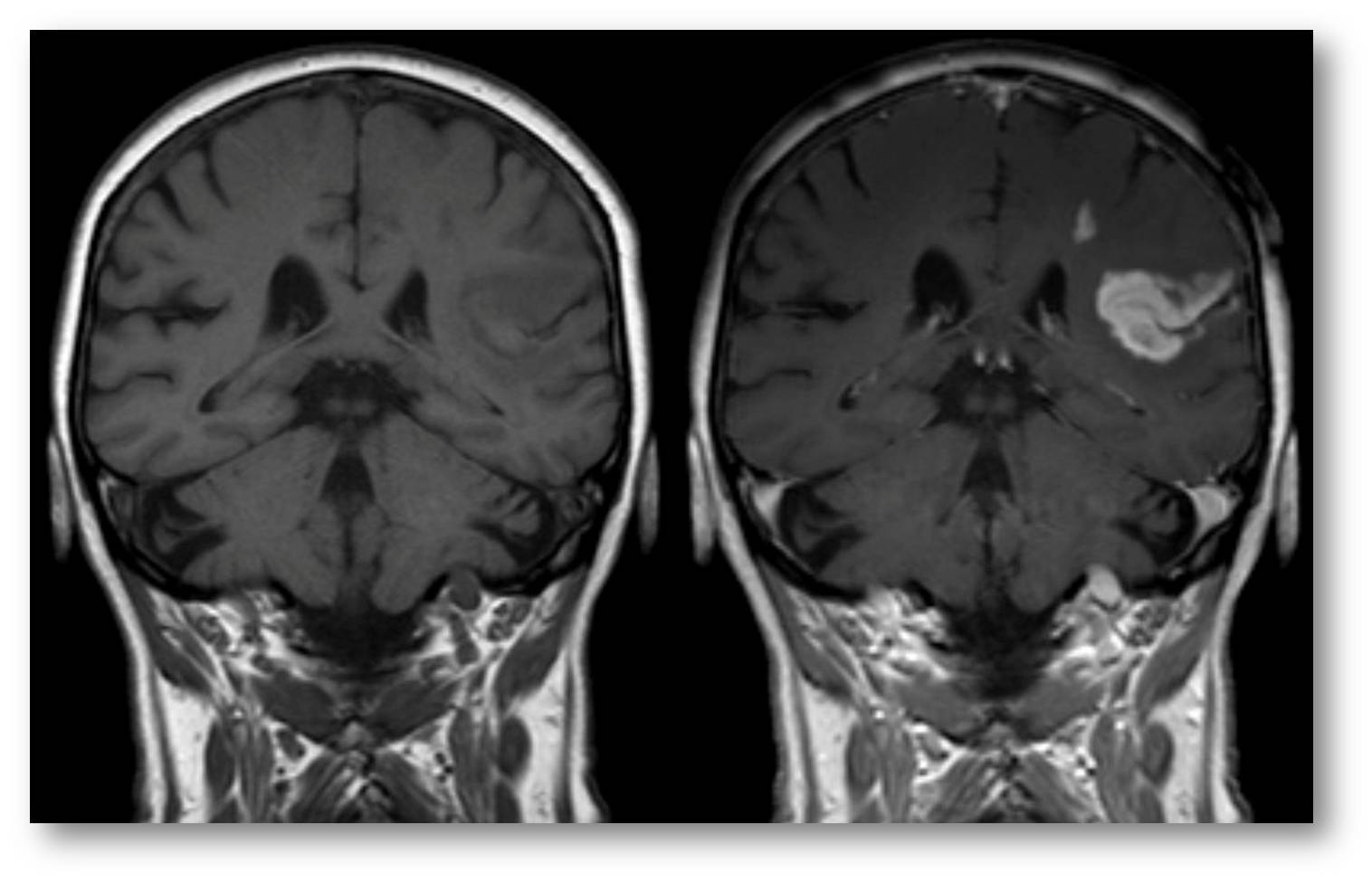 Abbildung 1. Forscher streben an, die schützende Blut-Hirn-Schranke für therapeutisch wirksame Moleküle durchlässig zu machen, um so Erkrankungen und Verletzungen des Gehirns behandeln zu können. (Bild: Hellerhoff, licensed under CC BY-SA 3.0)
Abbildung 1. Forscher streben an, die schützende Blut-Hirn-Schranke für therapeutisch wirksame Moleküle durchlässig zu machen, um so Erkrankungen und Verletzungen des Gehirns behandeln zu können. (Bild: Hellerhoff, licensed under CC BY-SA 3.0)
"Es ist in der Tat eine frustrierende Herausforderung, denn wir haben Entwicklungssubstanzen, die gute Wirkung zeigen könnten, wenn wir sie nur ins Gehirn brächten", sagt Professor Maria Tenje, ausgebildete Physikerin und Ingenieurin an der Universität Uppsala, Schweden.
Das Gehirn besitzt eine schützende Barriere - die sogenannte Blut-Hirn-Schranke -, die so aufgebaut ist, dass sie das Eindringen gefährlicher Moleküle und Zellen verhindert. Diese Schranke wirkt als Filter zwischen dem Gehirn und den Blutgefäßen: sie lässt wichtige Nährstoffe - wie Sauerstoff - passieren, während Moleküle ferngehalten werden, welche die empfindlichen, komplexen Prozesse im Gehirn stören könnten. Nun gut, fast alle.
"Wenn man ein Bier trinkt, kann man die angenehme Wirkung spüren, weil das Ethanol im Gehirn angekommen ist", sagt Prof. Tenje. „Könnte allerdings alles durch die Gefäßwand hindurch ins Gehirn gelangen, so würde das für uns das Ende bedeuten; wir haben ja viele Toxine, Nanopartikel und Chemikalien, die nicht ins Gehirn gelangen sollten.
"Aus der Sicht des Technikers ist es ein interessantes Problem - wie können wir etwas designen, das ausschließlich spezifische Moleküle passieren lässt, und wie können wir dies kontrollieren? Das ist, was wir herauszufinden versuchen.“
Vorhersagen
Im Rahmen eines EU-Projekts namens SONGBIRD [1] nützt Prof. Tenje ihre technische Expertise, um ein Modell der Blut-Hirn-Schranke zu erstellen. Damit sollen andere Forscher bessere Vorhersagen treffen können, welche Medikamente beim Menschen wahrscheinlich wirken. Die Barriere besteht aus vielen verschiedenen, dicht zusammen gepackten Zellen. (Abbildung 2). Modelle wurden dafür bereits in der Vergangenheit designt, die Schwierigkeit besteht aber darin das Gerüst zwischen den Zellen herzustellen.
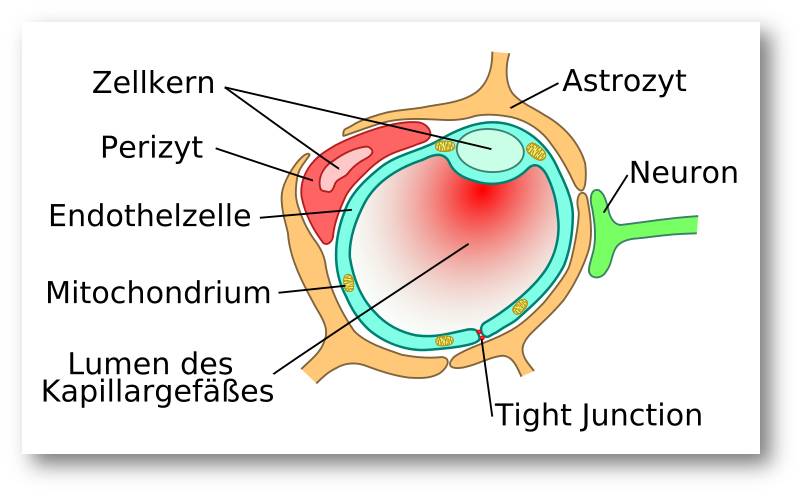 Abbildung 2. Querschnit durch die schützende Barriere um eine zerebrales Blutgefäß. Die Blutkapillare wird von Endothelzellen (türkis) gebildet, die keine Öffnungen haben und miteinander (über Tight Junctions) fest verbunden sind. Astrozyten (Makrogliazellen)bedecken mit ihren Gliederfüßchen (orange) die Endothelzellen, induzieren in diesen die Barrierefunktion und versorgen sie selektiv mit Nährstoffen. Perizyten sind fest an Endothelzellen verankert und weisen u.a. Immunfunktionen auf. (Bild und Text von der Redaktion eingefügt. Das Bild stammt aus Wikipedia: Zerebrale Kapillare; Armin Kübelbeck, Lizenz: cc-by)
Abbildung 2. Querschnit durch die schützende Barriere um eine zerebrales Blutgefäß. Die Blutkapillare wird von Endothelzellen (türkis) gebildet, die keine Öffnungen haben und miteinander (über Tight Junctions) fest verbunden sind. Astrozyten (Makrogliazellen)bedecken mit ihren Gliederfüßchen (orange) die Endothelzellen, induzieren in diesen die Barrierefunktion und versorgen sie selektiv mit Nährstoffen. Perizyten sind fest an Endothelzellen verankert und weisen u.a. Immunfunktionen auf. (Bild und Text von der Redaktion eingefügt. Das Bild stammt aus Wikipedia: Zerebrale Kapillare; Armin Kübelbeck, Lizenz: cc-by)
Dieses Gerüst - die sogenannte extrazelluläre Matrix - ist laut Prof. Tenje ein "klebriges Zeug". Es besteht aus Kollagen und Glykoproteinen um den Zellen strukturelle Stützung zu bieten. Um die extrazelluläre Matrix herzustellen, verwendet Prof. Tenje Hydrogel - ein Material, das zu etwa 90% aus Wasser besteht und durch Ketten von Polymeren zusammengehalten wird, die das Wasser an Ort und Stelle halten. Sie hofft, dass es ihr damit möglich sein wird, ein lebensechteres Modell zu schaffen. Die Herausforderung besteht jedoch darin, aus etwas, das weich ist, eine feste, stabile Struktur zu schaffen. Tenje und ihr Team testen verschiedene Möglichkeiten das Hydrogel zusammenzuhalten, ohne dass die Bewegungsfreiheit der Zellen beeinträchtigt wird.
"Will man diese Art von Material verwenden, um damit etwas zu bauen, so wird man Probleme haben, weil es zusammenfällt." Wir versuchen, die richtigen Methoden für den Bau von Strukturen mit weichem Material zu entwickeln “, sagte sie. Prof. Tenje hofft, dass dieses Modell uns einer zu einer besseren Vorhersage verhelfen könnte, ob ein Medikament die Barriere passieren wird, bevor es in klinischen Studien scheitert. Derzeit sind wir darauf angewiesen die Medikamente an Tieren zu testen, um festzustellen, wie gut sie wirken und ob sie sicher sind, bevor sie an Menschen getestet werden. "Wir sind Ratten zwar ähnlich, aber nicht so ähnlich", sagt sie.
Neues Modell
Dr. Igor Khalin vom Institut für Schlaganfall- und Demenzforschung an der Universität München sieht den erzielbaren Vorteil, den ein neues Modell für die Blut-Hirn-Schranke in der Forschung hat. "Wenn wir zwischen einer einfachen Zellkultur und Tierstudien etwas haben, ein Modell, das die Blut-Hirn-Schranke nachahmt, wird man die Zahl der Moleküle reduzieren, die man an Tieren testen muss", meint er.
„Allerdings kann das Modell nicht alle Probleme lösen. Man kann den Einsatz von Tieren nicht völlig vermeiden, da die nächste Stufe normalerweise die Forschung am Menschen ist. Wenn wir bei Tieren etwas übersehen, kann es für den Menschen böse enden.“
Dr. Khalin versucht besser zu verstehen, was im Gehirn passiert, wenn ein Arzneimittel die Barriere passiert. Im Rahmen eines Projekts namens NEUROTARGET entwickelt er ein System, um ein einzelnes Teilchen im Gehirn in Echtzeit zu verfolgen. „Bisher hat das niemand direkt gezeigt, nur indirekt. Ich möchte das Durchqueren der Blut-Hirn-Schranke direkt messen (sichtbar machen)“, sagt er.
Khalin verwendet Nanopartikel, die ein helles Licht abgeben, das unter dem Mikroskop sichtbar ist. Ein normales Lichtmikroskop kann Zellen sehen, aber keine Details von Objekten, die kleiner als 200 Nanometer sind. Die von Dr. Khalin verwendeten Nanopartikel sind nur 70 nm breit, aber dank des Lichts können sie gesehen werden. Er kombiniert diese Nanopartikel mit einer Technik namens Zwei-Photonen-Mikroskopie, mit der er das Gehirn einer Maus in Echtzeit abbilden kann.
Bei den von ihm verwendeten Nanopartikeln handelt es sich um Material, das von der Europäischen Arzneimittel-Agentur bereits für den Einsatz beim Menschen zugelassen wurde. Es kann die Blut-Hirn-Schranke passieren und zum Transport von Arzneimitteln verwendet werden. Es ist biologisch abbaubar, kann also von Enzymen im Körper abgebaut und absorbiert werden.
Änderungen
Dr. Khalin hofft, dass dieser Ansatz nicht nur zur Behandlung von Krankheiten beiträgt, sondern auch ein tieferes Verständnis dafür vermittelt, wie sich das Gehirn bei Verletzungen verändert.
"Wir können diese Partikel möglicherweise als Sonde verwenden und diese Sonde kann uns Informationen über die Pathophysiologie der Krankheit geben", sagt er. "Ich hoffe, wir können bei Schlaganfall und traumatischer Hirnverletzung helfen (heilen)."
Eines der Probleme bei Hirnverletzungen ist die langfristige Auswirkung kleinerer Stöße auf den Kopf. "Hirntrauma ist eine stille Epidemie", sagt er. 'Wenn jemand beispielsweise einen Zusammenstoß hat, bei dem er am Kopf getroffen wird und meint: "Ich brauche nicht zum Arzt zu gehen, mir geht es gut." Was derjenige nicht weiß, ist, dass viele Prozesse im Gehirn ablaufen. Am Ende wird dies die kognitive Funktion vermindern.
“Sowohl er als auch Prof. Tenje hoffen, dass ihre Forschung zu besseren Ergebnissen für die Patienten führen wird, sie sind sich jedoch bewusst, dass die Forschung noch im Anfangsstadium ist. Sie hoffen, ihre Expertisen so einzusetzen, dass andere darauf aufbauen können.
„Die Blut-Hirn-Schranke ist eine recht komplexe biologische Struktur. Sie besser zu verstehen ist unser Endziel und, um dies zu erreichen, betreiben wir technische Grundlagenforschung“, sagt Prof. Tenje. „Es sind große Herausforderungen, die mit der Biologie allein nicht gelöst werden können. Wir müssen zusammenarbeiten und unsere Anstrengungen bündeln.“
[1] SONGBIRD: SOphisticated 3D cell culture scaffolds for Next Generation Barrier-on-chip In vitro moDels. EU-Projekt (1 January 2018 - 31 December 2022) https://cordis.europa.eu/project/id/757444
[2] NEUROTARGET: Treatment of traumatic brain injury using dye-loaded polymeric nanoparticles. EU-Projekt (1.Dezember 2018 - 30. Novemner 2020) https://cordis.europa.eu/project/id/794094
Dieser Artikel wurde ursprünglich am 30. Jänner 2020 von Ian Le Guillo in Horizon, the EU Research and Innovation Magazine unter dem Titel Our brain has a barrier that stops drugs. How do we get past it? publiziert. Der unter einer cc-by-Lizenz stehende Artikel wurde von der Redaktion möglichst wortgetreu aus dem Englischen übersetzt. Abbildung 2 und Beschriftung wurden von der Redaktion eingefügt.
Weiterführende Links
Blood Brain Barrier on a Chip. (11.07.2019) LabTube Video 1:40 min. Wyss Institute Harvard University. https://www.technologynetworks.com/drug-discovery/videos/blood-brain-barrier-on-a-chip-321662
Auf dem ScienceBlog
Susanne Donner, 08.04.2016: Mikroglia: Gesundheitswächter im Gehirn.
Inge Schuster, 08.12.2016: Wozu braucht unser Gehirn so viel Cholesterin.
- Printer-friendly version
- Log in to post comments

