Fr, 30.06.2022 - — Tim Lämmermann

![]() In einem früheren Artikel hat der Immunologe Tim Lämmermann (Forschungsgruppenleiter am Max-Planck Institut für Immunbiologie und Epigenetik) über neutrophile Granulozyten berichtet [1]. Diese Fresszellen der angeborenen Immunantwort und Ersthelfer unseres Immunsystems patrouillieren durch Blutgefäße und wandern bei Anzeichen einer Entzündung oder Infektion schlagartig ins Gewebe ein, um dort Krankheitserreger zu eliminieren. Im Gewebe angekommen, schließen sie sich zu beeindruckenden Zellschwärmen zusammen und greifen Erreger gemeinsam an. Nun zeigt Lämmermann, dass Neutrophile ein molekulares Start-Stopp-System entwickelt haben, um ihre Schwarmaktivität selbst zu kontrollieren und Bakterien in Geweben effektiv und ohne Nebenwirkungen zu beseitigen.*
In einem früheren Artikel hat der Immunologe Tim Lämmermann (Forschungsgruppenleiter am Max-Planck Institut für Immunbiologie und Epigenetik) über neutrophile Granulozyten berichtet [1]. Diese Fresszellen der angeborenen Immunantwort und Ersthelfer unseres Immunsystems patrouillieren durch Blutgefäße und wandern bei Anzeichen einer Entzündung oder Infektion schlagartig ins Gewebe ein, um dort Krankheitserreger zu eliminieren. Im Gewebe angekommen, schließen sie sich zu beeindruckenden Zellschwärmen zusammen und greifen Erreger gemeinsam an. Nun zeigt Lämmermann, dass Neutrophile ein molekulares Start-Stopp-System entwickelt haben, um ihre Schwarmaktivität selbst zu kontrollieren und Bakterien in Geweben effektiv und ohne Nebenwirkungen zu beseitigen.*
Immunologische Erstabwehr von Infektionserregern
Unsere Körper sind durch Barrieren wie die Haut gut vor eindringenden Krankheitserregern geschützt. Durch Verletzungen, wie etwa bei einem Riss in der Haut, können jedoch Krankheitserreger durch die Wunde in den Körper eindringen und schwere Infektionen verursachen. In solchen Fällen übernimmt das angeborene Immunsystem die erste Verteidigungslinie mit einem effektiven Arsenal verschiedener zellulärer Waffen. Als einer der ersten Zelltypen vor Ort werden neutrophile Granulozyten, auch kurz Neutrophile genannt, innerhalb weniger Stunden aus dem Blutkreislauf in das verletzte Gewebe rekrutiert, um möglichst schnell mikrobielle Eindringlinge aufzunehmen und zu zerstören.
Schwärme von Fresszellen als angeborener Immunschutz
Neutrophile sind unscheinbar wirkende, runde Immunzellen mit einem Durchmesser von ca. 0,015 Millimetern, die im menschlichen Blut etwa 50-70% der weißen Blutkörperchen ausmachen. Nur an den Orten einer lokalen Entzündung oder Infektion treten sie aus den Blutgefäßen heraus, werden aktiviert und gehen dann im dortigen Gewebe auf die Jagd nach Erregern. Auf diese Weise patrouillieren diese Zellen fast alle Bereiche unseres Körpers.
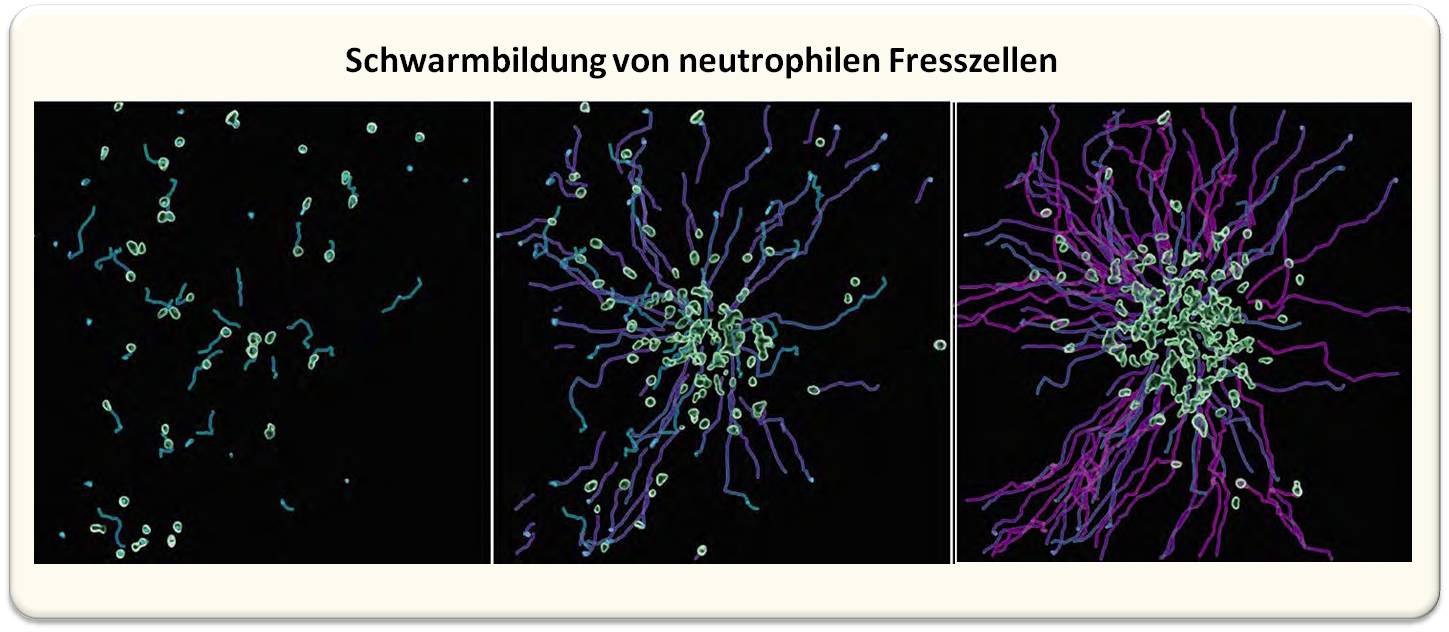
Mittels molekularer Sensoren auf ihrer Zelloberfläche sind Neutrophile besonders darauf spezialisiert, die Alarmsignale von Zellen zu erkennen, die durch Verletzungen oder eindringende Mikroben geschädigt wurden. Sobald einzelne Neutrophile solche Signale erkennen, rufen sie mittels chemischer Botenstoffe weitere Neutrophile zu Hilfe. Im Zuge unserer Forschung ist es uns gelungen, die Schlüsselrolle des Lipids Leukotrien B4, kurz LTB4, für genau diese Kommunikation zwischen den Immunzellen aufzudecken (Abbildung 1).
Dieses Lipid wird von aktivierten Neutrophilen ausgeschüttet, um anderen Neutrophilen die Richtung vorzugeben, der sie folgen sollen. Durch diese interzelluläre Kommunikation bilden Neutrophile imposante Zellschwärme, die zum Teil mehrere Hundert Zellen umfassen können und wie ein Zellkollektiv gemeinsam und fein abgestimmt im Gewebe agieren.
| Abbildung 1: Neutrophile (grün) bilden Zellschwärme und sammeln sich an Gewebestellen, wo sie beschädigte Zellen oder eindringende Mikroben eindämmen und bekämpfen. Die mehrfarbigen Bahnen zeigen die Bewegungspfade von Neutrophilen an. Zwischen dem linken und rechten Bild liegen 30 Minuten. © Max-Planck-Institut für Immunbiologie und Epigenetik/Lämmermann . |
Neben ihrer besonderen Effektivität beim Jagen von Bakterien sind Neutrophile auch noch hervorragend ausgerüstet, um diese zu töten und aus dem Gewebe zu entfernen. Hierzu besitzen sie in ihrem Zellinneren mehrere antibakterielle Substanzen, die Krankheitserreger töten können. Gelangen diese Substanzen jedoch aus der Zelle in ihre Umgebung, dann können sie für die umliegenden Gewebestrukturen aus Eiweißen und Zuckern schädlich sein. Ein Überschießen der nützlichen Entzündungsreaktion kann auf diese Weise zu massiven Gewebeschäden führen und zur Gefahr für den Körper werden. Ein solches Ungleichgewicht liegt häufig bei starken Entzündungsreaktionen vor und wird aktuell auch als eine der Ursachen für Lungenschäden bei schweren Verläufen von Covid-19 Erkrankungen diskutiert.
Eine molekulare Bremse, um den Schwarm zu stoppen
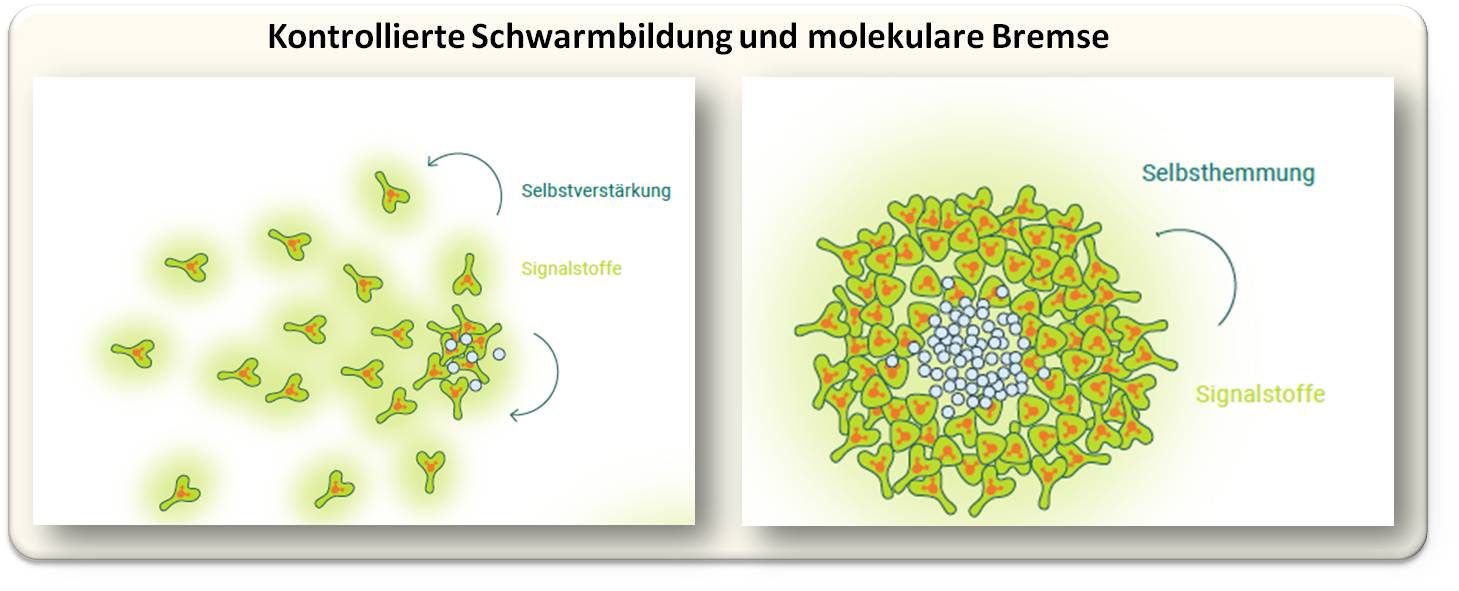
Während in den letzten Jahren immer mehr Erkenntnisse zu den auslösenden Mechanismen von Neutrophilen-Schwärmen gewonnen wurden, blieben diejenigen Prozesse bislang unbekannt, die diesen Teil der Immunreaktion wieder beenden. Am Max-Planck-Institut für Immunbiologie und Epigenetik haben wir uns deshalb der Frage gewidmet, wie das Schwarmverhalten von Neutrophilen und deren unkontrollierte Anhäufung im Gewebe die damit verbundene schädliche Entzündungsreaktion verhindert wird. Abbildung 2.
| Abbildung 2: Neutrophile geben Signalstoffe ab, die immer mehr Zellen anziehen (links). Übersteigt die Konzentration der Signale eine bestimmte Schwelle, kommt die Wanderung der Fresszellen zum Stillstand (rechts). Der so entstehende Schwarm kann eingedrungene Krankheitserreger (graue Kreise) abschirmen und bekämpfen. . |
Unsere Studien zeigen, dass Neutrophile ihre Schwarmaktivität selbst begrenzen und somit eine optimale Balance zwischen Such- und Zerstörungsphasen bei der Beseitigung von Erregern ermöglichen. Diese Erkenntnisse sind überraschend, denn bisherige Annahmen gingen stets von externen Signalen aus der Gewebeumgebung aus, die die Aktivität der Neutrophilen während der Endphase einer Entzündung dämpfen oder beenden. Durch den Einsatz spezieller Mikroskope für die Echtzeit-Visualisierung der Immunzelldynamik in lebendem Mausgewebe konnten wir jedoch zeigen, dass schwärmende Neutrophile mit der Zeit gegenüber ihren eigenen Signalen wie dem Leukotrien LTB4 unempfindlich werden, mit denen sie den Schwarm ursprünglich initiiert haben.
Um dies zu bewerkstelligen, besitzen Neutrophile eine molekulare Bremse, mit der sie ihre Bewegung stoppen, sobald sie hohe Konzentrationen der sich anhäufenden Schwarmlockstoffe in den Neutrophilen-Clustern wahrnehmen.
Jagdstrategien der Fresszellen
Das die Bremswirkung vermittelnde Protein trägt den Namen „G-Protein gekoppelte Rezeptor Kinase 2 (GRK2)“. Es sorgt dafür, dass bei hohen Konzentrationen der sich anhäufenden Schwarmlockstoffe die Zellen nicht mehr auf diese Signale reagieren und somit stehen bleiben. Angesichts der Entdeckung des Start-Stopp-Systems in Neutrophilen lag es nahe, zeitgleich geläufige Hypothesen zu Bewegungsmustern und Jagdstrategien von Fresszellen zu überprüfen. In Experimenten mit Neutrophilen, denen der Start-Stopp-Mechanismus fehlte, beobachteten wir nämlich, dass sich diese Zellen ungebremst im Gewebe bewegten und dadurch in großen Gewebebereichen nach Bakterien Ausschau halten konnten. Die Neutrophilen selbst hatten jedoch keinen Vorteil davon, sich besonders schnell im Gewebe bewegen zu können und ungebremst umherzueilen. Im Gegenteil: Neutrophile agieren viel effektiver, wenn sie als Schwarm eine infizierte Zelle umzingeln und dann dort verharren. Auf diese Weise bilden sie nämlich eine zelluläre Barriere, welche die Vermehrung und die weitere Verbreitung von Bakterien lokal eindämmt.
Fazit
Unsere Ergebnisse haben einen wichtigen Aspekt der Biologie von Neutrophilen entschlüsselt, der besonders für die Immunabwehr gegen Bakterien von Bedeutung ist. Unsere unerwarteten Erkenntnisse zu den Jagdstrategien der Immunzellen können wichtige Impulse für neue therapeutische Ansätze darstellen. Darüber hinaus könnten die hier beschriebenen Mechanismen zum Schwarmverhalten der Neutrophilen auch die Forschungen zum kollektivem Verhalten von Zellverbänden bis hin zum kollektiven Verhalten einiger Insektenarten vorantreiben.
[1] Tim Lämmermann, 08.07.2016: Schwärme von Zellen der angeborenen Immunantwort bekämpfen eindringende Mikroorganismen
* Der Artikel ist unter dem Titel "Wie sich Schwärme von Immunzellen selbst organisieren " im Jahrbuch der Max-Planck Gesellschaft 2021 h https://www.mpg.de/18167365/ie-freiburg_jb_2021?c=153825 und leicht modifiziert unter dem Titel "Schwärmende Fresszellen" in der Sammlung Highlights aus dem Jahrbuch 2021https://www.mpg.de/18802436/jahrbuch-highlights-2021.pdf im Mai 2022erschienen. Die MPG-Pressestelle hat freundlicherweise der Verwendung von Jahrbuch-Beiträgen im ScienceBlog zugestimmt. Der Artikel erscheint hier ohne Literaturzitate; diese können im Original nachgesehen werden.
- Printer-friendly version
- Log in to post comments