Fr, 11.03.2022 — Ricki Lewis

![]() Bei Infektionen mit SARS-CoV-2 können sich innerhalb eines Wirts Varianten des Virus an unterschiedlichen Stellen des Organismus entwickeln, die veränderte Präferenzen für Zelltypen aufweisen und sich vor dem Angriff des Immunsystems tarnen. Wie diese Tarnung erfolgen kann, zeigen neue Untersuchungen an synthetisch hergestellten Virionen: wenn bestimmte Fettsäuren, wie sie bei einer Entzündungsreaktion freigesetzt werden, in einer hochkonservierten Tasche des Spikeproteins binden, so verändert dieses seine Form und wird für das Immunsystem weniger sichtbar. Die Genetikerin Ricki Lewis berichtet darüber.*
Bei Infektionen mit SARS-CoV-2 können sich innerhalb eines Wirts Varianten des Virus an unterschiedlichen Stellen des Organismus entwickeln, die veränderte Präferenzen für Zelltypen aufweisen und sich vor dem Angriff des Immunsystems tarnen. Wie diese Tarnung erfolgen kann, zeigen neue Untersuchungen an synthetisch hergestellten Virionen: wenn bestimmte Fettsäuren, wie sie bei einer Entzündungsreaktion freigesetzt werden, in einer hochkonservierten Tasche des Spikeproteins binden, so verändert dieses seine Form und wird für das Immunsystem weniger sichtbar. Die Genetikerin Ricki Lewis berichtet darüber.*
Als ob es nicht schon genügt hätte, dass Wellen neuartiger SARS-CoV-2 Varianten - Varianten unter Beobachtung (Variants of Interest VOI) und besorgniserregende Varianten (Variants of Concern, VOC) - den Planeten überschwemmen, und dass wir Virus-Versionen finden, die in einem komplexen Muster von Integration und De-Integration in Arten eindringen und aus Arten austreten! Nun entdecken wir, dass das Ganze noch gefährlicher ist. Von einer Forschergruppe am Max Planck Bristol Center of Minimal Biology sind zwei neue Artikel in Nature Communications erschienen, die beschreiben, wie sich das Virus in verschiedenen Teilen desselben Wirts genetisch unterscheiden kann [1,2].
Was kann dies bedeuten
Auch, wenn Impfstoffe und Therapien das Virus in den Atemwegen besiegen, könnte der Erreger anderswo weiter persistieren. Und an neuen Plätzen könnten sich – möglicherweise – Viren unserer Immunantwort besser entziehen, sich besser replizieren und höher infektiös sein.
Bedenkt man, dass der Schutz durch Impfung oder Genesung von COVID-19 nachlässt, sind das keine guten Nachrichten.
Es war uns bereits bekannt, dass das Virus im Körper einer Person mit geschwächtem Immunsystem neue Mutationen erzeugen kann. Und es mutiert schnell in den Ungeimpften. Aber die aktuelle Forschung zeigt, dass bei ein und demselben Individuum neue Varianten in verschiedenen Körpernischen entstehen.
Virus-Varianten, die in ein und demselben Individuum entsehen
„Unsere Ergebnisse haben gezeigt, dass man mehrere verschiedene Virusvarianten im Körper haben kann. Einige dieser Varianten können Nieren- oder Milzzellen als Nische nutzen, um dort geborgen zu sein, während der Körper damit beschäftigt ist, sich gegen den dominanten Virustyp zu verteidigen. Dies könnte es den infizierten Patienten schwer machen, SARS-CoV-2 vollständig loszuwerden“, sagt Kapil Gupta, der Erstautor des einen Artikels [1].
Eine hochkonservierte, essentielle Tasche im Spikeprotein
Der Vorgang beim Eindringen eines Virus in eine Wirtszelle konzentriert sich auf eine Region – eine Tasche – in dem Teil des viralen Spike-Proteins, welches das Immunsystem erkennt. Eine Änderung der dreidimensionalen Form der Tasche wirkt auf das Virus wie die Tarnvorrichtung der Romulaner aus Star Trek, die deren Kriegsschiffe unsichtbar macht, wenn sich ein Raumschiff der Föderation nähert.
Die Forscher haben die Tasche in Viren untersucht, die von einem einzelnen englischen Patienten stammten und eine Deletionsmutation im Spike-Protein aufwiesen, in welcher 8 der 1273 Aminosäuren fehlten. Dabei handelt es sich um eine Deletion in Nachbarschaft zur sogenannten Furin-Spaltstelle, einer kritischen Stelle, an der das Spikeprotein (von einem Enzym der Wirtszelle, Anm. Redn.) in seine zwei Untereinheiten gespalten wird, worauf eine Untereinheit die menschliche Zelle akquiriert und die andere das Virus in die Zelle hineinzieht.
Aber statt dass der fehlende Teil das Virus nun inaktiv macht, haben die Forscher heraus gefunden, dass sich der Erreger in einer Weise verformt, dass er noch in menschliche Zellen eindringen kann.
Das ist ein Weg, wie sich das Virus ständig neu erfindet - auf unterschiedliche Weise in verschiedenen Ritzen und Schlupfwinkeln des unglücklichen Wirtsorganimus'.
Die BriSdelta-Variante
Die Version des Virus aus dem englischen Patienten – BriSdelta genannt – repliziert sich stark in Kulturen von Affennierenzellen und von menschlichen Dickdarmkrebszellen, aber nicht in menschlichen Lungenkrebs-Epithelzellen. Abbildung 1. Das könnte bedeuten, dass sich die Präferenz des Wildtyps für Oberflächen der Atemwege anders wohin verlagert, wenn das Virus beschädigt ist.
|
Abbildung 1: Verglichen mit dem SARS-CoV-2 Wildtyp (blau) ist die BriSDelta-Variante (rot) stärker infektiös in Affennierenzellen (Vero E6) und Dickdarmkrebszellen (Caco-2, dagegen schwächer infektös in Lungenepithelzellen (Calu-3). Bilder aus K. Gupta et al., [1] von Redn. eingefügt,Lizenz: cc-by. |
Die neue Version des Virus kann sich besser replizieren und ist stärker infektiös als frühere Varianten.
„In der heterogenen Umgebung des menschlichen Körpers können solche Deletionsvarianten in geeigneten Zelltypen entstehen, welche als potenzielle Nischen zur Weiterentwicklung oder Spezialisierung von SARS-CoV-2 fungieren“, schreiben die Forscher.
Das ist beängstigend.
Synthetische Minimal-Virionen
Die Forscher haben dann untersucht, wie dies geschieht, indem sie künstliche Versionen des Virus verwendeten, die mit Techniken der synthetischen Biologie zusammengebaut wurden. Abbildung 2.
|
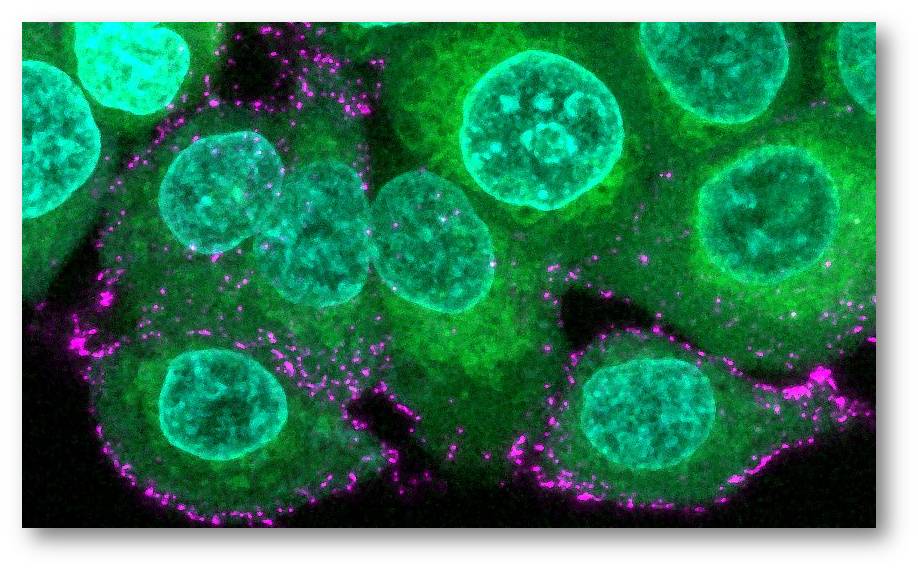
Abbildung 2: Menschliche Epithelzellen (grün mit blauen Kernen) werden mit synthetischen Sars-CoV-2-Viren (magenta) inkubiert, um den Beginn der Infektion und die Immunabwehr zu untersuchen. (Halo Therpeutics). Bilder aus K. Gupta et al., [1] von Redn. eingefügt,Lizenz: cc-by. |
Die zweite Veröffentlichung beschreibt diese „synthetischen Minimalvirionen“, auch bekannt als MiniVs, des Wildtyps SARS-CoV-2 und Kombinationen der Mutationen aus der Parade der Varianten [2].
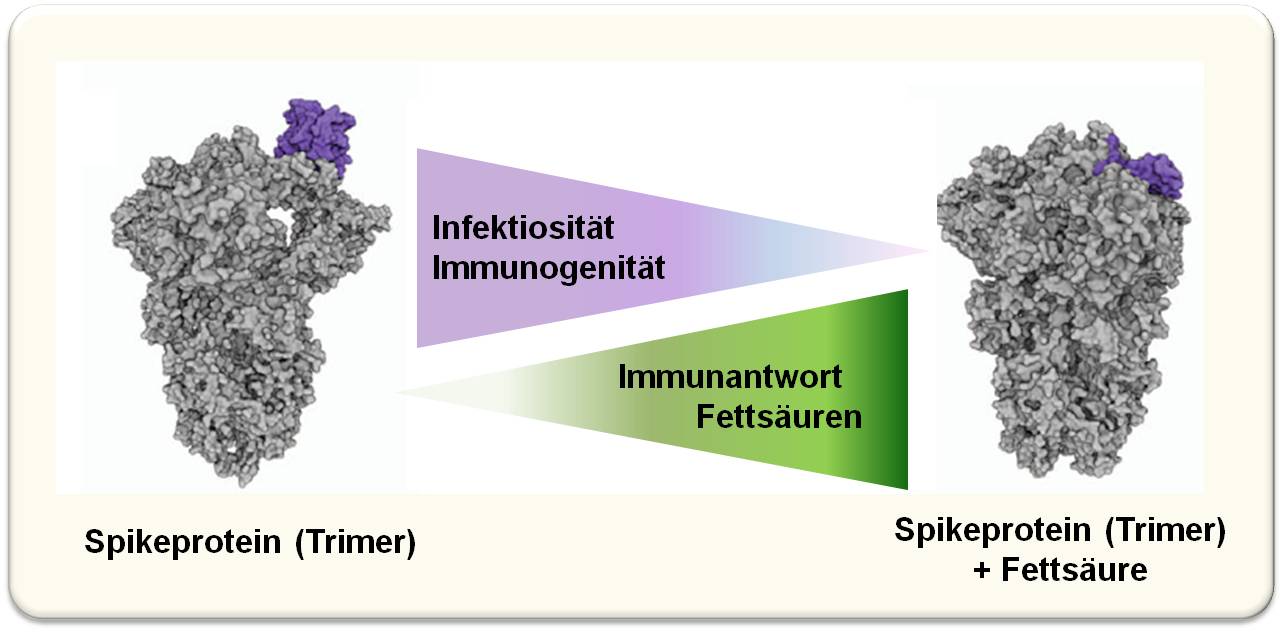
Dabei haben sie herausgefunden, dass Fettsäuren, wie sie während eines Entzündungsprozesses freigesetzt werden (das ist die initiale Reaktion des angeborenen Immunsystems auf eine Infektion), an die neue Mutante binden und dabei ein subtiles Zusammenfalten der Form des Spikeproteins bewirken, die dieses vor dem Ansturm von Antikörpern aus der spezifischeren Reaktion des adaptiven Immunantwort tarnt. Abbildung 3.
|
Abbildung 3: Das Spike-Protein ändert bei der Bindung einer Fettsäure seine Form - damit kann es nicht mehr an den ACE-2-Rezeptor der Wirtszelle andocken und es wird für das Immunsystem weniger sichtbar. Abbildung aus O. Staufer et al., [2] von Redn. eingefügt. Lizenz cc-by |
Die Forscher haben ein Unternehmen, Halo Therapeutics, gegründet, um antivirale Pan-Coronavirus-Mittel zu entwickeln, basierend auf dem Tanz von Spikeprotein-Tasche mit den ACE-2-Rezeptoren auf menschlichen Zellen – egal wo diese sich im Körpebefinden.
Fazit
Wenn wir also unsere Masken abnehmen und fröhlich zu einem Anschein von Normalität zurückkehren, dürfen wir nicht vergessen, dass SARS-CoV-2 immer noch überall da draußen lauert und sich ständig verändert.
Wir müssen für das nächste Mal bereit sein!
[1] Kapil Gupta et al., Structural insights in cell-type specific evolution of intra-host diversity by SARS-CoV-2. Nature Comm. (2022) 13:222 https://doi.org/10.1038/s41467-021-27881-6
[2] Oskar Staufer et al., Synthetic virions reveal fatty acid-coupled adaptive immunogenicity of SARS-CoV-2 spike glycoprotein. Nature Comm. (2022) 13:868 https://doi.org/10.1038/s41467-022-28446-x
* Der Artikel ist erstmals am 3.März 2022 in PLOS Blogs - DNA Science Blog unter dem Titel "SARS-CoV-2 Pops Up, Mutated, Beyond the Respiratory Tract"
https://dnascience.plos.org/2022/03/03/sars-cov-2-pops-up-mutated-beyond-the-respiratory-tract/ erschienen und steht unter einer cc-by Lizenz . Die Autorin hat sich freundlicherweise mit der Übersetzung ihrer Artikel durch ScienceBlog.at einverstanden erklärt, welche so genau wie möglich der englischen Fassung folgen. Einige Überschriften und Abbildungen 1 und 3 plus Legenden wurden von der Redaktion eingefügt.
- Printer-friendly version
- Log in to post comments