Do 07.10.2021 — Benjamin List

![]() Wilhelm Ostwald hatte 1901 den Begriff des Katalysators definiert: "Ein Katalysator ist jeder Stoff, der, ohne im Endprodukt einer chemischen Reaktion zu erscheinen, ihre Geschwindigkeit verändert." Bis vor 20 Jahren kannte man 2 Gruppen von Katalysatoren: i) in der Biosphäre eine schier unendliche Zahl an Enzymen, die hochselektiv die Synthese aller organischen Verbindungen (d.i. Gerüste aus Kohlenstoff, Wasserstoff und N-, O-, S- Und P-Gruppen) ermöglichen und ii) Metalle (Metallverbindungen), die von Akademie und Industrie zur zielgerichteten chemischen Synthese diverser organischer Moleküle eingesetzt werden. Eine dritte Klasse von Katalysatoren haben um 2000 Benjamin List (damals Scripps-Research Institute, US) und David MacMillan (Princeton University) voneinander unabhängig entdeckt: kleine organische Moleküle, die hochselektiv und effizient chemische Reaktionen katalysieren und ein enormes Potential für die industrielle Anwendung haben. Die beiden Forscher wurden für diese fundamentale Entdeckung mit dem diesjährigen Chemie-Nobelpreis ausgezeichnet. Im Folgenden findet sich ein kurzer Bericht von Benjamin List (Direktor am Max-Planck-Institut für Kohlenforschung, Mülheim, D) , den er nach seiner Rückkehr nach Deutschland 2003 über das neue Gebiet der Organokatalyse verfasst hat.*
Wilhelm Ostwald hatte 1901 den Begriff des Katalysators definiert: "Ein Katalysator ist jeder Stoff, der, ohne im Endprodukt einer chemischen Reaktion zu erscheinen, ihre Geschwindigkeit verändert." Bis vor 20 Jahren kannte man 2 Gruppen von Katalysatoren: i) in der Biosphäre eine schier unendliche Zahl an Enzymen, die hochselektiv die Synthese aller organischen Verbindungen (d.i. Gerüste aus Kohlenstoff, Wasserstoff und N-, O-, S- Und P-Gruppen) ermöglichen und ii) Metalle (Metallverbindungen), die von Akademie und Industrie zur zielgerichteten chemischen Synthese diverser organischer Moleküle eingesetzt werden. Eine dritte Klasse von Katalysatoren haben um 2000 Benjamin List (damals Scripps-Research Institute, US) und David MacMillan (Princeton University) voneinander unabhängig entdeckt: kleine organische Moleküle, die hochselektiv und effizient chemische Reaktionen katalysieren und ein enormes Potential für die industrielle Anwendung haben. Die beiden Forscher wurden für diese fundamentale Entdeckung mit dem diesjährigen Chemie-Nobelpreis ausgezeichnet. Im Folgenden findet sich ein kurzer Bericht von Benjamin List (Direktor am Max-Planck-Institut für Kohlenforschung, Mülheim, D) , den er nach seiner Rückkehr nach Deutschland 2003 über das neue Gebiet der Organokatalyse verfasst hat.*
Organokatalyse ist eine neue Katalysestrategie, bei der kleine, rein organische Katalysatoren verwendet werden. Obwohl die Natur eine ähnliche metallfreie Katalyse in vielen Enzymen verwendet, haben Chemiker erst vor kurzem das große Potenzial der Organokatalyse als einer hochselektiven und umweltfreundlichen Synthesemethode realisiert. In den letzten Jahren wurden spektakuläre Fortschritte auf dem Gebiet erzielt und seit kurzem wird Organokatalyse auch am Max-Planck-Institut für Kohlenforschung in Mülheim betrieben. Sie ergänzt dort bereits existierende Forschung auf den Sektoren der Biokatalyse, Metallkatalyse und der Heterogenen Katalyse.
Chemiker bemühen sich seit langem, die Effizienz und Selektivität von Enzymen mit synthetischen Katalysatoren nachzuahmen. Insbesondere ist es ein Ziel, die hohe Selektivität, die Enzyme gegenüber spiegelbildlichen Molekülen aufweisen, auch in chemisch katalysierten Reaktionen zu erreichen. Diese so genannte Enantioselektivität ist von herausragender Bedeutung in der Synthese von Wirkstoffen, da spiegelbildliche Moleküle unterschiedliche biologische Aktivitäten aufweisen.
Überraschenderweise basieren die für diesen Zweck entwickelten Katalysatoren fast ausschließlich auf Metallkomplexen, während etwa die Hälfte aller Enzyme völlig metallfrei ist. Erst seit kurzem realisiert man, dass auch niedermolekulare organische Katalysatoren hoch effizient und selektiv chemische Reaktionen katalysieren können. Das Potenzial solcher organokatalytischer Reaktionen ist insbesondere für die industrielle Synthese sehr groß, da die verwendeten Katalysatoren robust, günstig erhältlich, ungiftig und einfach zu synthetisieren sein sollen. Außerdem werden organokatalytische Reaktionen häufig bei Raumtemperatur durchgeführt und sind unempfindlich gegenüber Luft und Feuchtigkeit; viele Reaktionen lassen sich in der Tat in wässrigen Lösungsmitteln durchführen. Eine bedeutend leichtere Anbindung an die feste Phase zur effizienten Abtrennung und Rückgewinnung des Katalysators ist ebenfalls möglich. Das große Potenzial dieses Gebiets wird inzwischen akzeptiert und eine exponentiell wachsende Anzahl von Forschergruppen beschäftigt sich weltweit mit dieser noch nicht einmal ansatzweise ausgeschöpften Thematik.
|
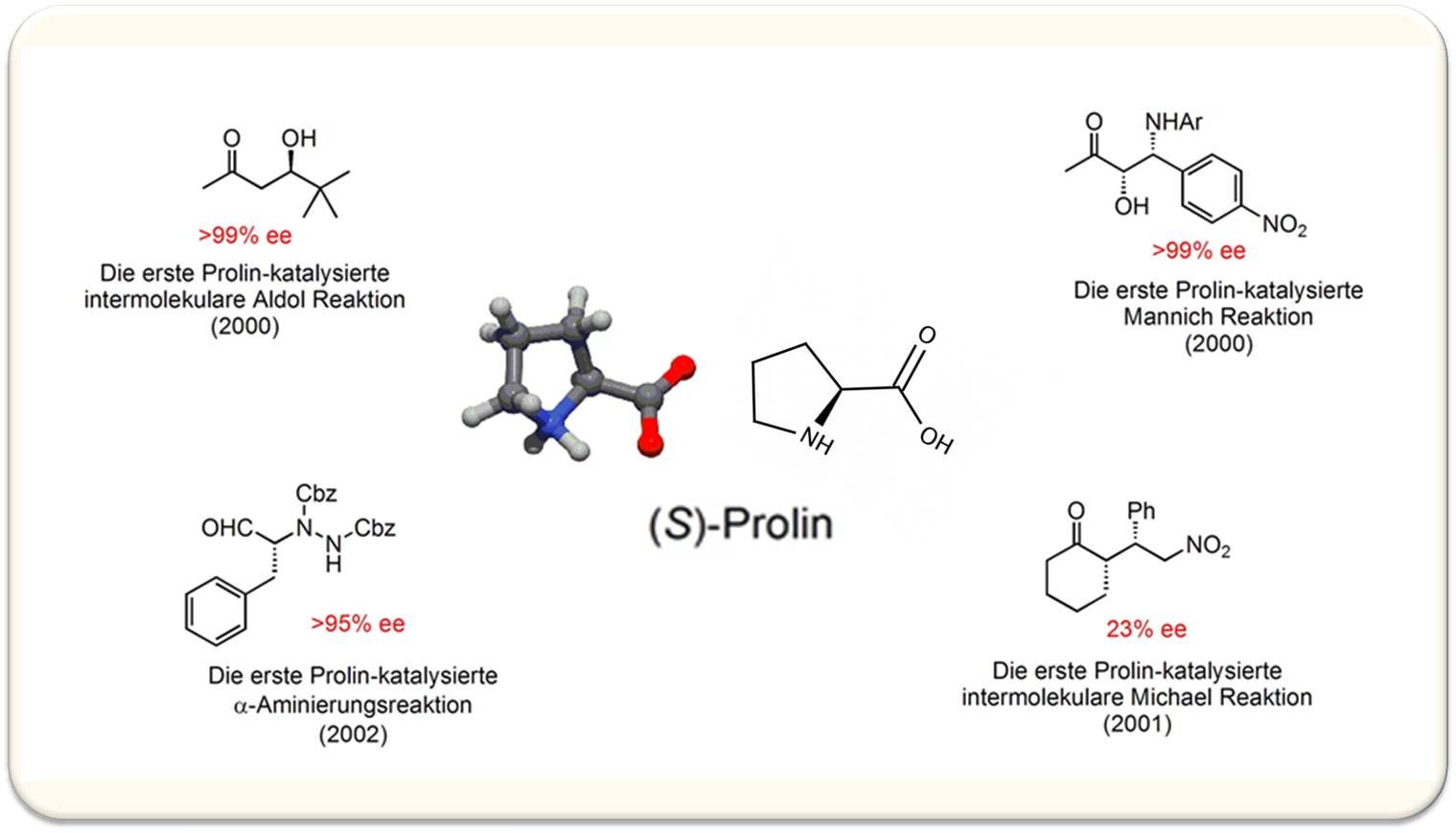
Abbildung: Produkte neu entdeckter Prolin-katalysierter Reaktionen. Ausbeuten enantioselektiver Produkte (ee rot) in Prozent. (In das Bild wurde von Redn. die Strukturformel des Prolin eingefügt.) |
Eine wichtige Klasse von organokatalytischen Reaktionen, die insbesondere am Max-Planck-Institut für Kohlenforschung untersucht werden, sind solche, die durch Amine und Aminosäuren katalysiert werden können. So konnten in den letzten Jahren eine Reihe von Reaktionen entwickelt werden, die durch die Aminosäure Prolin katalysiert werden, so zum Beispiel hochselektive Aldol-, Mannich-, Michael- und Aminierungsreaktionen (Abbildung). Diese neuen Reaktionen liefern in exzellenten Ausbeuten und Enantioselektivitäten chirale Alkohole, Amine und Aminosäurederivate von potenziellem Nutzen für die Synthese funktionaler Moleküle, insbesondere von Wirkstoffen. Vor kurzem wurden außerdem neuartige Zyklisierungsreaktionen entdeckt.
* Der vorliegende Artikel von Bejamin List ist dem Jahrbuch 2003 der Max-Planck-Gesellschaft unter dem Titel "Organokatalyse: Eine neue und breit anwendbare Synthesemethode" (https://www.mpg.de/870377/forschungsSchwerpunkt1?c=154862) erschienen und kann mit freundlicher Zustimmung der MPG-Pressestelle im ScienceBlog verbreitet werden. Der Abstract (kursiv) zum Artikel wurde von der Redaktion eingefügt. Der folgendeText und eine Abbildung wurden unverändert übernommen, allerdings fehlt der abschließende Teil über eine Reihe weiterer wichtiger Prolin-katalysierter Reaktionen und die Darstellung ihrer Synthesewege, da dafür eine Vertrautheit mit der Sprache der organischen Chemie nötig ist. Auch für die Literaturzitate wird auf den Originalartikel verwiesen.
Weiterführende Links
Benjamin List homepage: https://www.kofo.mpg.de/de/forschung/homogene-katalyse
Catarina Pietschmann: Eine Perspektive fürs Leben (6. Oktober 2021), Ein Porträt des Direktors am Max-Planck-Institut für Kohlenforschung und Chemie-Nobelpreisträgers 2021. Chemie (M&T) Preise
Nobelpreis für Chemie 2021: Press release: https://www.nobelprize.org/prizes/chemistry/2021/press-release/und
Popular information: Their tools revolutionised the construction of molecules. https://www.nobelprize.org/prizes/chemistry/2021/popular-information/
BR Mediathek: Benjamin List erklärt seine Methode der asymmetrischen Organokatalyse. (ARD alpha campus talk 2019). Video 11;26 min. https://www.br.de/mediathek/video/nobelpreis-fuer-chemie-benjamin-list-erklaert-seine-methode-der-asymmetrischen-organokatalyse-av:615da7fdeb179f00072e4570
- Printer-friendly version
- Log in to post comments