So 04.07.2021.... Inge Schuster 
![]()
Chemisch betrachtet ist Hyaluronsäure ein ganz einfaches Molekül: ein natürliches, in unseren Organismen vorkommendes Biopolymer, das aus zwei miteinander verknüpften, sich wiederholenden Zuckerresten (d.i. einem Disaccharid) besteht, die enorm viel Wasser binden können. Als eine wesentliche Komponente des extrazellulären Raums hält Hyaluronsäure unsere Gewebe - Haut, Knorpel, Gelenke - feucht und straff, eine Fähigkeit, die aber mit zunehmendem Alter leider abnimmt. Unterschiedlichste Anwendungen in der Medizin und vor allem im Kosmetiksektor boomen derzeit; für 2027 wird global ein Umsatz von mehr als16 Milliarden US $ prognostiziert.
Seit ihrer Entdeckung im Glaskörper von Kuhaugen vor fast 90 Jahren ist das Interesse an Hyaluronsäure und ihren möglichen Anwendungen in Medizin und Kosmetik enorm gestiegen. Unter dem Stichwort "hyaluronic acid" verzeichnet PubMed.gov - die US-Amerikanische Datenbank für Biomedizinische Publikationen - aktuell insgesamt 31 350 wissenschaftliche Artikel , wobei mehr als 2 000 Artikel jährlich dazukommen, die globale Datenbank https://clinicaltrials.gov/ nennt 519 klinische Studien, die von ästhetischer Medizin über Arthrosen bis hin zu Wundheilung reichen und Google schließlich listet unüberschaubare 50,9 Millionen Einträge und nahezu 2 Millionen Videos, die meisten davon bewerben Cremen, Seren und Haut-Füller, die eine faltenfreie jugendliche Haut versprechen. Sie lassen den an seriöser Information interessierten Laien einigermaßen ratlos zurück.
Hyaluronsäure boomt - dies spiegelt sich im Marktgeschehen wider. Neben zahlreichen kleineren Unternehmen sind auch "Big Player" in Pharma - beispielsweise Allergan, Galderma und Sanofi - am Hyaluron-Business beteiligt. Laut dem Marktforschungsunternehmen Grand View Research dürfte 2020 der globale Markt für medizinische Hyaluronsäure(produkte) bei etwa US $ 9,6 Mrd. liegen und bis 2027 wird eine Steigerung auf US $ 16,5 Mrd erwartet. Unter den Anwendungen dominieren derzeit Osteoarthritis (rund 41 % des Markts) und "Hautfüller" (rund 30 % des Markts). Die prognostizierten hohen Wachstumsraten sind auf den stark ansteigenden Anteil der älteren/geriatrischen Bevölkerung zurückführen, die sich von Hyaluronsäure, angewandt mit minimal invasiven Methoden, eine Besserung ihres Bewegungsapparats und eine Verjüngung ihres äußeren Erscheinungsbildes erhofft.
Was ist Hyaluronsäure?
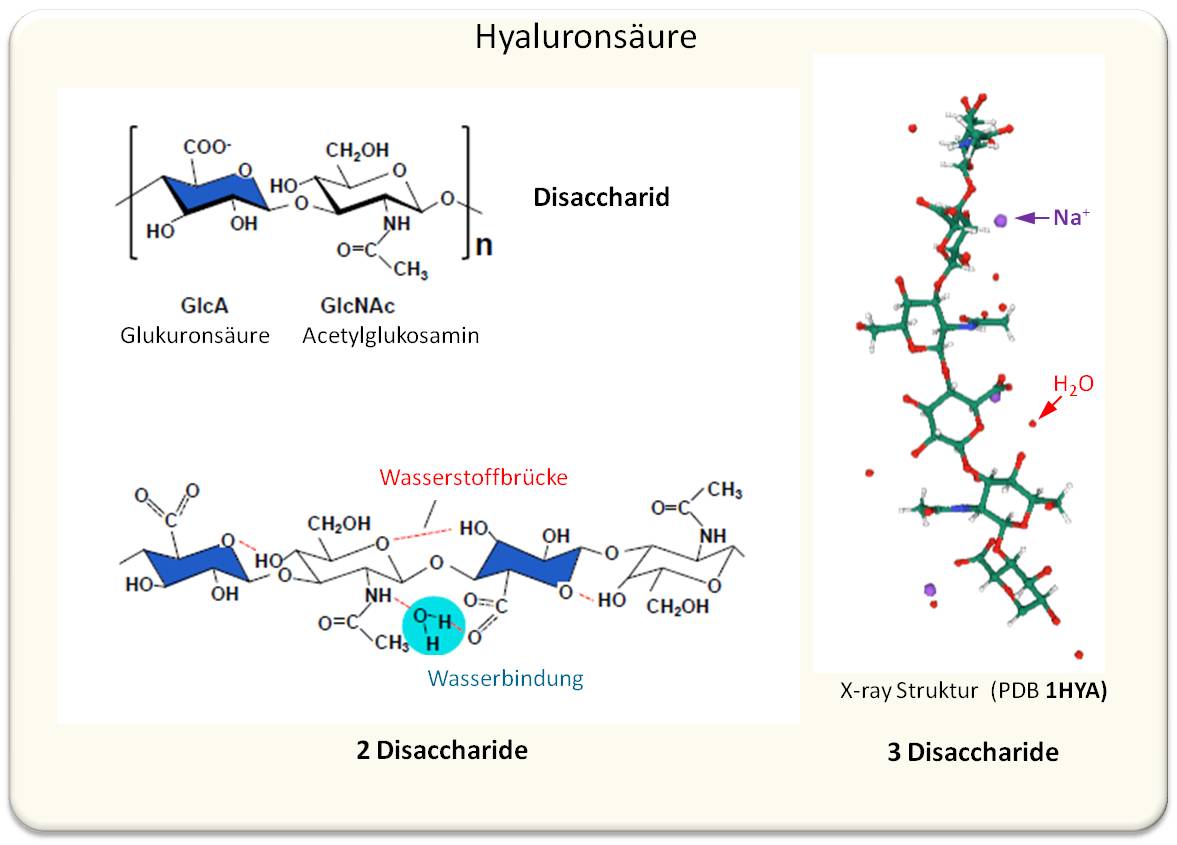
Es ist ein langkettiges, lineares Biopolymer, das in allen Wirbeltieren produziert wird und in nahezu allen Teilen des Körpers vorhanden ist (s.u.). Hyaluronsäure setzt sich aus zwei sich wiederholenden, von Glukose abgeleiteten Einheiten, sogenannten Disacchariden - Glukuronsäure und Acetylglukosamin - zusammen. Die Säuregruppen der Glukuronsäure machen das Polymer zum Polyanion. Die Fülle an hydrophilen (d.i. mit Wasser wechselwirkenden) Gruppen (Hydroxyl-, Caboxyl- und Acetamidgruppen) kann über Wasserstoffbrücken in der Molekülkette selbst miteinander interagieren und im wässrigen Milieu enorme Mengen an Wassermolekülen anlagern (Abbildung 1). Das hochflexible Polymer bildet mit steigender Kettenlänge Knäuel ("random coils"), die über Wasserstoffbrücken temporäre netzförmige Strukturen ausbilden und ein bis zu mehr als Tausendfaches ihres Gewichts an Wasser zu speichern vermögen (1mg Hyaluronsäure bis 6 g Wasser).
|
Abbildung 1.Hyaluronsäure setzt sich aus sich wiederholenden Disaccharideinheiten - Glukuronsäure und N-Acetylglukosamin - zusammen. Das Disaccharid zeigt die Fülle an hydrophilen Gruppen - -OH-, COO--, C=O-, NH-, - die über Wasserstoffbrücken mit Gruppen in der Kette und auch mit H2O wechselwirken (unten). Rechts: Röntgenstruktur der linearen aus 3 Disacchariden bestehende Kette mit 3 Na-Ionen (lila) und einigen Wassermolekülen (rot). (Quelle links: modifiziert nach T.Kobayashi et al., Biomolecules 2020, 10, 1525; doi:10.3390/biom10111525; Lizenz cc-by und rechts: https://www.rcsb.org/3d-view/1HYA/1). |
Diese netzförmigen Strukturen zeichnen sich durch hohe Viskoelastizität aus, d.i. sie können sich schnell neu konfigurieren und so an räumliche Gegebenheiten anpassen (Elastizität) aber auch zu ursprünglichen Konfigurationen zurückkehren (Viskosität). Von der Kettenlänge und Konzentration hängen die physikalischen, chemischen und physiologischen Eigenschaften der Hyaluronsäure ab und diese variieren in den unterschiedlichen Geweben. Die Kettenlänge reicht dabei von Oligomeren, die aus bis zu 20 Disacchariden (Molekulargewicht bis zu 7 600 Da) bestehen, bis hin zu hochmolekularen Polymeren mit über 10 000 Disaccharideinheiten (MW über 4 000 000 Da), wie sie beispielsweise in der Gelenksflüssigkeit (Synovia) vorkommen. Die lange Kettenlänge und hohe Konzentration in der Gelenksflüssigkeit (Abbildung 2) macht Hyaluronsäure zu einem hervorragenden Schmiermittel der Gelenke und bewirkt viskoelastische Eigenschaften bei Bewegungen.
Wo kommt Hyaluronsäure vor?
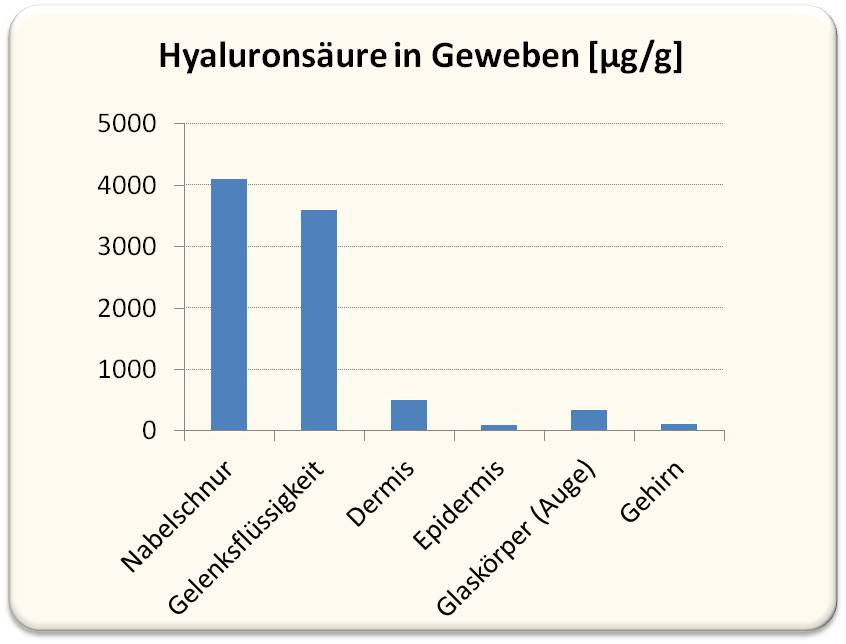
Insgesamt enthält der Körper eines Erwachsenen (mit rund 70 kg Körpergewicht ) etwa 15 g Hyaluronsäure, die einem raschen Turnover unterliegt: täglich wird etwa ein Drittel abgebaut und wieder neu synthetisiert. Hohe Konzentrationen finden sich (abgesehen von der Nabelschnur) in der Gelenksflüssigkeit, im Glaskörper des Auges und in der Haut (vor allem in der Dermis). Auf Grund ihrer Größe enthält die Haut etwa die Hälfte der im Körper vorhanden Hyaluronsäure. Abbildung 2.
|
Abbildung 2.Konzentration von Hyaluronsäure (in µg/g) in einigen Geweben des menschlichen Körpers. Angaben beziehen sich auf maximal gemessene Konzentrationen. Daten stammen aus P. Snetkov et al., Polymers 2020, 12, 1800; doi:10.3390/polym12081800 (Artikel steht unter cc-by Lizenz). |
Hyaluronsäure ist ein Hauptbestandteil des extrazellulären Raums
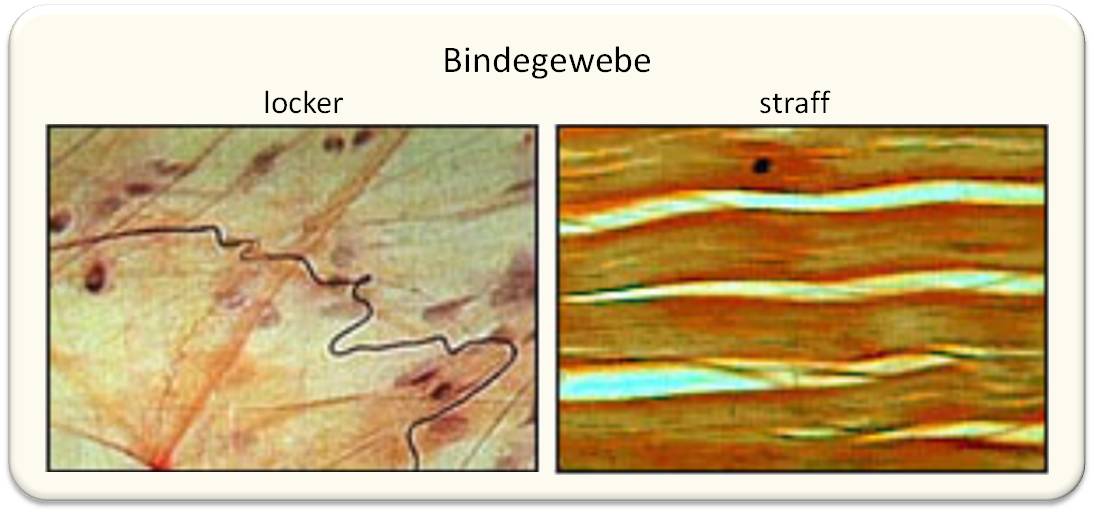
und findet sich in nur geringen Mengen in den Körperzellen. In stark hydratisierter Form bildet sie - zusammen mit anderen Polysacchariden, Glykoproteinen und Proteoglykanen (s.u.) - die sogenannte Grundsubstanz, ein viskoses, gelartiges Milieu , das die Zellen umgibt, Wasser im extrazellulären Raum speichert und so die Diffusion von Nährstoffen und Stoffwechselprodukten von und zu den Zellen ermöglicht. Strukturiert durch Kollagenfasern und elastische Fasern wird die Grundsubstanz zur sogenannten extrazellulären Matrix. Aus Grundsubstanz, Faserproteinen und relativ wenigen darin lose liegenden und anhaftenden Zellen setzen sich dann die verschieden Arten der Bindegewebe zusammen. In straffen und lockeren Bindegewebstypen sind Fibroblasten die hauptsächlichen Zelltypen, daneben gibt es auch verschiedene (patrouillierende) Zelltypen des Immunsystems. Abbildung 3.
|
Abbildung 3.Zwei Typen des Bindegewebes unter dem Mikroskop. Links: Lockeres Bindegewebe, wie es in diversen Zwischenräumen im Körper vorkommt und auch das Gerüst vieler Organe bildet. Es überwiegt hier häufig die Grundsubstanz, die von Kollagenfasern (orangerot gefärbt) und elastischen Fasern (dunkelblau)durchzogen wird. Vereinzelte Zellen (dunkle Kerne) sind lose eingebettet. Rechts: Straffes Bindegewebe mit einem hohen Anteil an Kollagenfasern und weniger Grundsubstanz. Durch die parallele Anordnung in Sehnen und Bändern wird deren Zugfähigkeit erhöht. (Bild: https://en.wikipedia.org/wiki/Connective_tissue#/media/File:Illu_connective_tissues_1.jpg; gemeinfre). |
Bindegewebe halten Körperorgane an ihren Positionen, stellen die Verbindung zwischen Blutgefäßen, Lymphgefäßen und Zellen und zwischen verschiedenen Gewebetypen her. Darunter fallen so unterschiedliche Typen wie man sie in der Haut - hier vor allem in der Dermis - findet, im Knorpel, im Gallertkern der Bandscheiben, in der Gelenksflüssigkeit, in den Sehnen, Knochen, in Muskel- und Fettgeweben, im Zahnfleisch, im Auge (Glaskörper), in den Hirnhäuten und im Gehirn. In all den verschiedenen Bindegeweben spielt Hyaluronsäure eine wesentliche Rolle, verleiht diesen (nicht komprimierbares) Volumen, Elastizität, viskoses Verhalten und fungiert u.a. als Stoßdämpfer und als Schmierung. Hyaluronsäure liegt dabei nicht nur als unmodifiziertes Polymer vor, sondern kann auch mit Glykoproteinen verknüpft sein und riesige Aggregate - sogenannte Proteoglykane - bilden (beispielsweise Aggrecan im Knorpel). Hirngewebe zeichnet sich durch geringe Steifigkeit aus - hier enthält die extrazelluläre Matrix nur geringe Mengen an Faserproteinen und hohe Konzentrationen an Hyaluronsäure und Proteoglycanen.
Physiologische Eigenschaften
Über lange Zeit beschränkte sich die Hyaluronsäure-Forschung im wesentlichen auf die biomechanischen, hydrodynamischen und chemischen Eigenschaften des Polymers. Hyaluronsäure vermag wesentlich mehr. Durch spezifische Bindung an Rezeptoren an Zelloberflächen aktiviert sie in den Zellen Signale, welche die dynamischen Eigenschaften von Zellen - wie Motilität, Adhäsion und Proliferation - regulieren können. Hyaluronsäure kann damit in physiologische Prozesse - von Wundheilung bis Morphogenese - involviert sein aber auch zu pathologischen Auswirkungen - Entzündung bis Tumorwachstum - beitragen. Der erste derartige, vor rund 30 Jahren charakterisierte Rezeptor - CD44 -, der auf vielen Zelltypen exprimiert wird aber auch durch einige andere Biomoleküle (z.B. Osteopontin) aktiviert werden kann, spielt u.a. eine wichtige Rolle in der Aktivierung von Lymphozyten. Daneben trägt CD44 wesentlich zum Abbau der Hyaluronsäure bei. Diese wird im Komplex mit CD44Komplex von den Zellen internalisiert ("receptor-mediated endocytosis") und in den Lysosomen enzymatisch von sogenannten Hyaluronidasen zu kleinen, niedermolekularen Bruchstücken abgebaut, die in den zellfreien Raum sezerniert werden. Derartige Abbauprodukte sind biologisch durchaus aktiv und können beispielsweise in Fibroblasten der Dermis und auch in Keratinocyten (den Hauptzellen der Epidermis) die Synthese neuer Hyaluronsäure stimulieren.
In der Folge wurden und werden weitere Rezeptoren für Hyaluronsäure identifiziert wie der Rezeptor für Hyaluronsäure-vermittelte Mobilität (RHAMM), der Endothelzell-Rezeptor der Leber, der Lymphendothelzell-Rezeptor (LYVE-1) u.a.m.
Das an und für sich einfach gestrickte Polymer zeigt eine mehr und mehr komplexe Fülle an Eigenschaften und physiologisch wichtigen Funktionen. Diese sind derzeit Gegenstand intensiver Forschung, versprechen sie doch ein tieferes Verstehen dieser Regulationsvorgänge und damit neue Konzepte und /oder verbesserte Voraussetzungen für medizinische Anwendungen.
Anwendungen
Molekülgröße und Konzentration der Hyaluronsäure sind für die Eigenschaften der extrazellulären Matrix in den verschiedensten Geweben ausschlaggebend und werden durch Synthese und Abbau feinreguliert. Innerhalb von 2 - 3 Tagen erfolgt so ein kompletter Austausch der gesamten Hyaluronsäure.
Mit zunehmendem Alter wird allerdings die Balance zwischen Synthese und Abbau gestört: die Synthese verlangsamt sich (reduzierte Enzymaktivitäten) und der Abbau (enzymatisch aber auch , durch bestimmte Umweltfaktoren verursacht) nimmt zu. Davon betroffen sind die Gelenksflüssigkeit ebenso wie Knorpel, Bandscheiben, Sehnen, Haut, etc. Um die gestörte Balance in der extrazellulären Matrix/ in den Bindegeweben wieder herzustellen, wird versucht die spärlich vorhandene Hyaluronsäure durch Präparate zu substituieren, die häufig biotechnologisch aus Streptokokken -Kulturen produziert werden. Da Hyaluronsäure auf natürliche Weise im Menschen vorkommt, ist mit guter Verträglichkeit zu rechnen.
Hyaluronsäure wird in verschiedensten medizinischen Indikationen eingesetzt, u.a. bei trockenen Augen und Schleimhäuten, in der Wundheilung und bei Verbrennungen. Am weitesten verbreitet sind Behandlungen von Arthrosen, vor allem Arthrosen des Kniegelenks.
Behandlung von Arthrosen
Wie weiter oben beschrieben verschaffen hohe Konzentrationen von hochmolekularer Hyaluronsäure die erforderlichen viskoelastischen Eigenschaften in den Gelenken. Nimmt altersbedingt die Hyaluronsäure in Gelenksflüssigkeit und Knorpeln ab, so führt dies zu Steifheit der Gelenke, eingeschränkter Beweglichkeit und Schmerzen. Eine von der FDA bereits seit den 1990er Jahren zugelassene Anwendung der Hyaluronsäure erfolgt bei Arthrosen, vor allem bei Kniearthrosen. Die Hyaluronsäure wird dabei mehrmals direkt ins Gelenk injiziert und soll über mehrere Monate (vielleicht auch ein ganzes Jahr) die Symptome lindern (auch wenn sie nur Stunden bis wenige Tage am Applikationsort verbleibt). Wie Metaanalysen zeigen, sind die Behandlungsergebnisse allerdings nicht durchgehend überzeugend, reichen von mangelnder Wirksamkeit in älteren Untersuchungen bis zu temporärer Schmerzhemmung bei milden/moderaten Arthrosen in neueren Analysen. Bei der Injektion ins Gelenk kann es zudem zu unerwünschten Nebenwirkungen kommen wie Beschädigungen des Knorpels, Infektionen im Gelenk - kommen.
Hautalterung
Im Vergleich zu einem Baby mit einer ganz prallen, faltenfreien Haut enthält die Dermis einer 50 Jahre alten Person im Mittel nur mehr halb so viel Hyaluronsäure und diese nimmt mit zunehmendem Alter noch weiter ab. Neben veränderten Synthese/Abbauaktivitäten sind vor allem Schäden durch Umwelt und Sonnenlicht (UV-Licht) für die Reduktion verantwortlich.
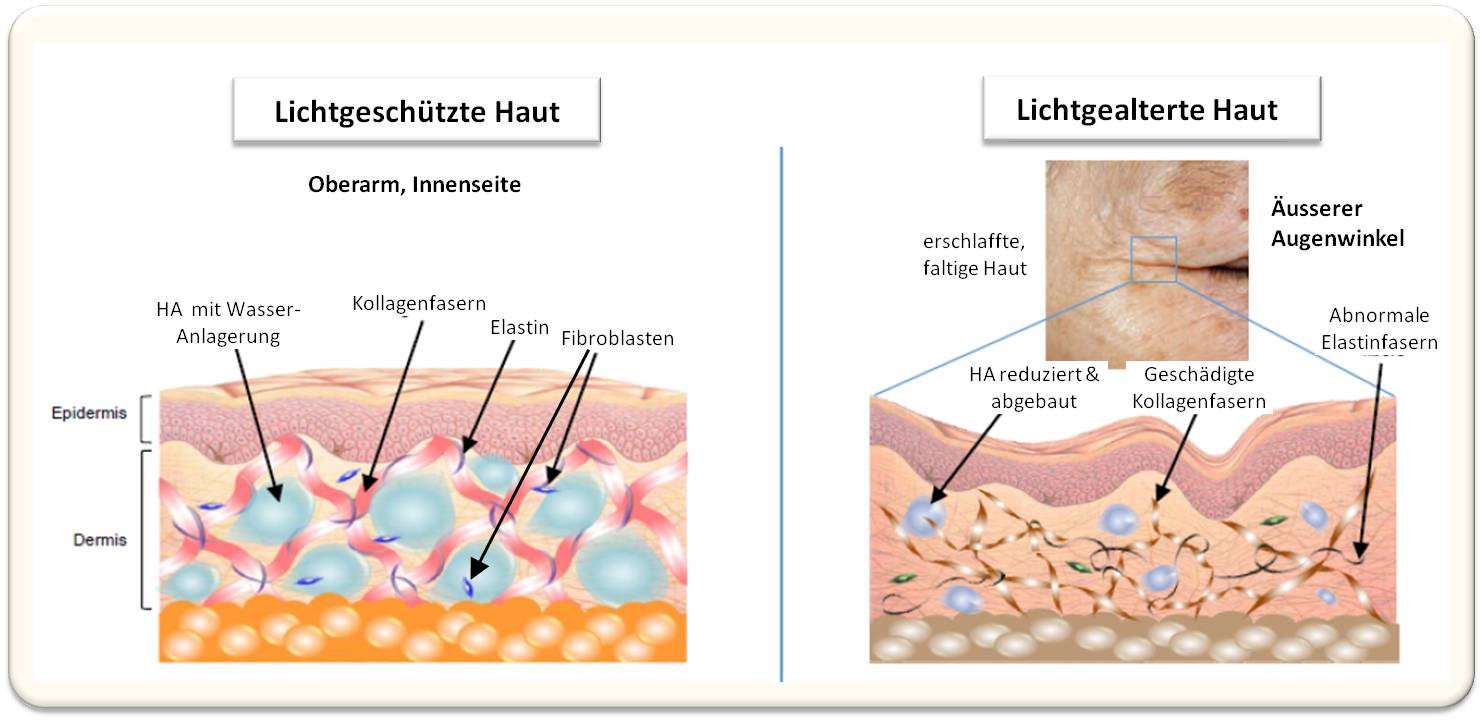
Abbildung 4 zeigt schematisch die Folgen der Sonneneinstrahlung. Die Hyaluronsäure ist reduziert und teilweise abgebaut, damit sinkt der Wassergehalt in der extrazellulären Matrix der Dermis, Wechselwirkungen mit den Kollagen- und Elastinfasern werden dezimiert und der Abbau der Fasern erleichtert. Die vormals straffe Haut ist nun erschlafft und zeigt Falten.
Abbildung 4.Vergleich einer lichtgeschützten Haut mit einer lichtgealterten Haut. Beschreibung im Text (Bild modifiziert nach: Hiroyuki Yoshida & Yasunori Okada, Int. J. Mol. Sci. 2019, 20, 5804; doi:10.3390/ijms20225804. Lizenz: cc-by).
Um dem Wunsch nach jugendlicher, faltenfreier Haut zu begegnen, verwenden Firmen seit rund 20 Jahren Hyaluronsäure als Feuchtigkeitsspender und Faltenglätter in ihren kosmetischen Produkten. Die meisten Hautcremen und Seren enthalten Hyaluronsäure in niedermolekularer bis hochmolekularer Form und auch in Form von Nanopartikeln. Werden diese Produkte aufgetragen, so dringen sie größenabhängig zwar unterschiedlich weit in die Haut ein, erreichen aber nicht die tieferen Schichten der Dermis, die ja zu wenig Hyaluronsäure enthält und zur Hauterschlaffung führt. Große Moleküle (Kettenlänge über 1 000 Disaccharideinheiten) bleiben auf der obersten Schichte - der Hornhaut - liegen, bilden eine Barriere, die Feuchtigkeit zurückhält und die Hornhaut etwas aufquellen lässt. Niedermolekulare Hyaluronsäure bringt Feuchtigkeit in die dichten Zellschichten der rund 0,15 mm tiefen Epidermis. Wie oben erwähnt hofft man an, dass kurzkettige Bruchstücke der Hyaluronsäure dort in den Keratinocyten die Synthese neuer Hyaluronsäure stimulieren können. Das Ergebnis ist bestenfalls eine geschmeidigere Haut und etwas flachere Fältchen.
Will man feinere Falten an Lippen und Augenpartien auffüllen, tiefe Falten, wie Nasolabialfalten, Zornesfalten und Augenpartien korrigieren, so wird Hyaluronsäure in unterschiedlicher Dichte als "Hautfüller" in die Dermis injiziert. Einige dieser Präparate wurden von der FDA zugelassen . Hautfüller kommen auch zur Schaffung von Volumen, Wiederherstellen von Gesichtskonturen in der plastischen Chirurgie zur Anwendung. Die Ergebnisse dieser minimal invasiven Behandlung sind sofort sichtbar und im Allgemeinen recht gut. Allerdings können Hautreizungen, Verformungen und Klumpenbildung und damit ein unerwünschtes Erscheinungsbild auftreten. Die straffende Wirkung ist allerdings nicht von Dauer; nach einem halben Jahr (vielleicht auch etwas später) sind Nachspritzungen erforderlich.
Fazit
Die physikalisch - chemischen und physiologischen Eigenschaften der im Menschen natürlich vorkommenden Hyaluronsäure weisen auf ein enormes Potential für gut verträgliche, minimal invasive medizinische Anwendungen und Korrekturen des äußeren Erscheinungsbildes hin. Einige dieser Anwendungen sind bereits etabliert und haben ein großes, stark steigendes Marktvolumen. Verbesserungen sind aber auch hier notwendig - beispielsweise in den Techniken und Produkteigenschaften der bis jetzt unbefriedigenden Therapie von Arthrose oder in der Verlängerung der Wirksamkeitsdauer. Die Forschung zu diesen Problemen aber auch zu völlig neuen Aspekten der Hyaluronsäure-Funktionen und -Anwendungen boomt und lässt auf innovative Produkte und Techniken nicht nur im Anti-Aging Sektor hoffen.
Literatur (open access), die dem Artikel zugrundeliegt, u.a.:
A.Fallacara et al., Hyaluronic Acid in the Third Millennium, Polymers 2018, 10, 701; doi:10.3390/polym10070701.
P. Snetkov et al., Hyaluronic Acid: The Influence of Molecular Weight on Structural, Physical, Physico-Chemical, and Degradable Properties of Biopolymer. Polymers 2020, 12, 1800; doi:10.3390/polym12081800
T. Kobayashi et al., Hyaluronan: Metabolism and Function. Biomolecules 2020, 10, 1525; doi:10.3390/biom10111525
A. Kaul et al., Hyaluronidases in Human Diseases. Int. J. Mol. Sci. 2021, 22, 3204. https://doi.org/10.3390/ijms22063204
Artikel zu verwandten Themen im ScienceBlog:
Georg Wick, 22.11.2012: Erkrankungen des Bindegewebes: Fibrose – eine häufige Komplikation bei Implantaten.
Inge Schuster, 17.07.2015: Unsere Haut – mehr als eine Hülle. Ein Überblick
Inge Schuster, 06.09.2018: Freund und Feind - Die Sonne auf unserer Haut
- Printer-friendly version
- Log in to post comments