Fr, 23.09.2016 - 15:26 — Inge Schuster

![]() Abgesehen von einem (relativ geringen) Risiko von Nebenwirkungen tragen Antibiotika wesentlich dazu bei, dass wir gesund bleiben und lang leben. Allerdings entwickeln Bakterien gegen diese Substanzen schnell Resistenzen, in vielen Fällen werden sie multiresistent. Es besteht die Gefahr, dass die vorhandenen Antibiotika schneller unwirksam werden als innovative, neue Substanzen auf den Markt kommen. Dies könnte zu einer Pandemie führen.
Abgesehen von einem (relativ geringen) Risiko von Nebenwirkungen tragen Antibiotika wesentlich dazu bei, dass wir gesund bleiben und lang leben. Allerdings entwickeln Bakterien gegen diese Substanzen schnell Resistenzen, in vielen Fällen werden sie multiresistent. Es besteht die Gefahr, dass die vorhandenen Antibiotika schneller unwirksam werden als innovative, neue Substanzen auf den Markt kommen. Dies könnte zu einer Pandemie führen.
Vor kurzem hat mich ein Freund angerufen. Er hatte am 15. September das ARD-Magazin "Kontraste" gesehen und war nun zutiefst verunsichert. In dieser Sendung wurde über dauerhafte Gesundheitsschäden berichtet, die durch die Einnahme des Antibiotikums Ciprofloxacin entstanden waren. Dieses Arzneimittel war meinem Freund eben verschrieben worden, da er nach einer Operation an einer massiven Infektion im Urogenitaltrakt litt. Er fürchtete sich nun vor Nebenwirkungen - Sehnenabrisse, Nervenschäden sowie Angstattacken und Psychosen -, wie dies in der TV-Sendung an Hand zweier nahezu bewegungsunfähiger junger Männer überaus drastisch vor Augen geführt wurde.
Bereits der einleitende Satz der Sprecherin machte klar, wer für diese Schäden die Verantwortung zu tragen hätte: "unsere Geschichte handelt von fahrlässigen Ärzten, einer trägen Arzneimittelbehörde und einem tatenlosen Minister." In den folgenden rund siebeneinhalb Minuten wurden Ängste geschürt - es gäbe keine aktuellen Warnungen von Seiten der Arzneimittelbehörde oder gar eine dick-schwarz umrandete (Black Box) Warnung auf den Beipackzetteln, wie dies die amerikanische Arzneimittelbehörde FDA (allerdings erst vor 4 Monaten) getan hatte und auch keine breite öffentliche Aufklärung der Patienten (wie in den USA). Ein Patient klagte " ich bin hinterhältig vergiftet worden, ohne überhaupt gewarnt zu werden" Dass der Beipackzettel [2] alle Risiken und für die Anwendung wichtigen Informationen enthält, wurde kommentiert "da steht dermaßen viel drin, dass kein Mensch, kein Verbraucher und auch kein Arzt überblicken kann, was alles drin steht". Viele Zuseher fühlten sich von diesem Report offensichtlich sehr betroffen, gerieten in Panik und setzten ihre Medikamente ab - zumindest war dies aus Diskussionen In Internetforen zu entnehmen.
Was ist Ciprofloxacin?
Ciprofloxacin ist bereits seit rund 30 Jahren am Markt. Die Grundstruktur - ein Chinolon - stammt (wie auch das verwandte Chinin) aus der China-Rinde. Erfolgreiche Derivatisierung hat dann zu einem breiten Spektrum an behandelbaren Keimen geführt, zu erhöhter Wirksamkeit, verbesserter Stabilität im und Verfügbarkeit für den menschlichen Organismus (zum Unterschied zu vielen anderen Antibiotika kann es oral verabreicht werden). Abbildung 1.
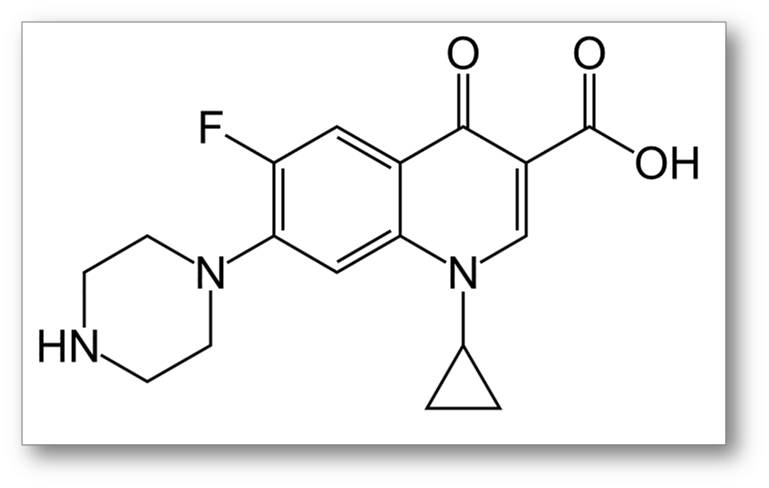 Abbildung 1. Ciprofloxacin ist ein kleines, synthetisches Molekül, das 1987 von Bayer auf den Markt gebracht wurde. Als oral anwendbares Breitbandantibiotikum hat es sich zum Blockbuster (> 1Mrd $ Umsatz) entwickelt.
Abbildung 1. Ciprofloxacin ist ein kleines, synthetisches Molekül, das 1987 von Bayer auf den Markt gebracht wurde. Als oral anwendbares Breitbandantibiotikum hat es sich zum Blockbuster (> 1Mrd $ Umsatz) entwickelt.
Ciprofloxacin ist ein Breitbandantibiotikum: es wirkt gegen gram-positive (u.a. Pneumokokken) und gram-negative Keime (u.a. Chlamydien, Pseudomonas, E. coli,…) und tötet diese ab. Besondere Bedeutung hat es in der Behandlung von schweren Infektionen, vor allem von solchen, die durch Pseudomonas aerugenosa hervorgerufen wurden. Es wird bei Infektionen des Bauchraums, der Atemwege, von Harnwegsinfektionen, akute Nierenbeckenentzündung, Infektionen der Gallenwege und auch bei Milzbrand (Anthrax) angewandt, gilt aber auch als Reserveantibiotikum (kommt zum Einsatz, wenn andere Antibiotika - u.a. beta-Lactame, Tetracycline - erfolglos waren).
In den letzten Jahrzehnten sind praktisch keine neuen, gegen gram-negative Bakterien gerichtete, Antibiotika auf den Markt gekommen. Ciprofloxacin ist und bleibt also auch weiterhin ein wichtiger Bestandteil des antibiotischen Armentariums:
- Die World Health Organisation (WHO) führt Ciprofloxacin in der Liste essentieller Arzneistoffe unter Antibacterials (14 beta-Lactame und 14 "other antibacterials", darunter Ciprofloxacin).
- Chinolone gehören - trotz ihrer Nebenwirkungen (siehe unten) - auch weiterhin zu den Strukturen, die modifiziert werden und als Entwicklungssubstanzen in die klinische Prüfung kommen. Derzeit befinden sich 39 Substanzen in den klinischen Phasen 1 -3, darunter sind 7 Chinolone, 3 davon in der letzten Phase (Phase III) [4].
Nutzen versus Risiko
Im vergangenen Jahrhundert ist die Lebenserwartung in der westlichen Welt stark gestiegen. Lag sie für Neugeborene in Deutschland um 1900 bei rund 42 Jahren (Mittel aus m + f), so war sie um 1960 auf 67 (m) und 72 (w) Jahre angestiegen. Dies war neben besserer Ernährung und Hygiene vor allem der wirksamen Bekämpfung von Infektionskrankheiten mit Medikamenten, insbesondere von bakteriellen Infektionen mit Antibiotika, und Vakzinen zu verdanken. Vormals tödliche Erkrankungen wie Tuberkulose oder Lungenentzündung konnten nun geheilt werden.
Insgesamt stehen heute rund 200 unterschiedliche Wirkstoffe zur Verfügung, die gegen verschiedene Erreger eingesetzt werden, zum Teil sind sie gegen ein weites Spektrum von Bakterien wirksam - sogenannte Breitband-Antibiotika -, zum Teil nur gegen einzelne spezielle Keime.
Allerdings ist mit jeder Antibiotikatherapie auch das Risiko von Nebenwirkungen verbunden (auch, wenn diese zum Glück vhm. selten auftreten). Um nur einige davon zu nennen:
- bei beta-Laktamen (Penicillinen, Cephalosporinen, Penemen) können neben gastrointestinalen Beschwerden vor allem allergische Reaktionen bis hin zum anaphylaktischen Schock auftreten.
- Bei Folsäureantagonisten können es Veränderungen des Blutbilds und Knochenmarksschädigungen sein,
- bei Makroliden Hörstörungen und Leberschäden bis hin zur cholestatischen Hepatitis.
- Bei der Gruppe der Chinolone, zu denen das bereits erwähnte Ciprofloxacin gehört, sind es u.a. gastrointestinale Beschwerden, Ausschlag, Leberschäden, Sehnenentzündungen bis hin zu Sehnenrissen, Nervenschäden und Psychosen. Ob Chinolone mehr Nebenwirkungen verursachen als Cephalosporine, darüber differieren die Meinungen.
Einer Antibiotikabehandlung sollte daher eine Risikoabwägung vorausgehen: ist die Wirkung weitaus höher einzuschätzen als der Schaden durch mögliche Nebenwirkungen? (So wie er Gebrauchsanweisungen für diverse Geräte studiert, sollte der mündige Patient auch den Beipackzettel zu seinem Medikament ansehen.)
Ein sozio-ökonomisch weit bedrohlicheres Szenario als das Risiko von Nebenwirkungen, ist allerdings die sich ausbreitende Resistenz gegenüber den Antibiotika.
Resistenzentwicklung – Antibiotika verlieren ihre Wirksamkeit
Dass Bakterien - aber auch andere Mikroorganismen - gegen antimikrobielle Substanzen resistent werden, ist ein ganz natürlicher Vorgang. Viele dieser Organismen produzieren ja selbst Antibiotika und müssen daher Mechanismen haben, um sich davor schützen. Resistenz ist aber auch logische Folge eines Evolutionsprozesses - von Mutation und Selektion: Bakterien vermehren sich sehr rasch und machen bei der Kopierung ihres Erbguts relativ viele Fehler. Beeinträchtigt eine Mutation nun die Zielstruktur (Target) gegen die ein Antibiotikum wirkt, so hat das betroffene Bakterium einen Vorteil, es kann sich in Gegenwart des Antibiotikums munter weiter vermehren und es entsteht eine neue, resistentere Population.
Bakterienpopulationen sind stets heterogen. Bei Behandlung mit Antibiotika werden zuerst die dagegen empfindlichsten Populationen eliminiert/abgetötet, dann die weniger sensitiven, dann die noch weniger sensitiven, usf. Wird die Behandlung zu früh abgebrochen, oder war die Dosis zu gering, so bleiben die resistenteren Keime über und vermehren sich - auf das Antibiotikum in der üblichen Dosierung spricht diese Population nicht mehr an.
Resistenzgene können auch von einem auf andere Bakterien - über die Speziesgrenzen hinweg - übertragen werden und diese damit gegen unterschiedliche Antibiotika resistent werden. So entstehen dann multiresistente Erreger.
Gegen Antibiotika resistente Bakterien findet man überall und in allen Ländern . Sie sind in Lebensmitteln , in der Umwelt, in Tier und Mensch. Eine enorme Bedrohung stellen sie in Spitälern und in Pflegeeinrichtungen dar.
Die Resistenzentwicklung wird durch exzessive Anwendung von Antibiotika und Missbrauch beschleunigt, beispielsweise, wenn oft allzu leichtfertig Antibiotika gegen virale Infektionen wie Influenza oder Erkältungen verschrieben werden, gegen die sie ja völlig wirkungslos sind, oder wenn sie tonnenweise in der Viehzucht eingesetzt werden, um schnelleres Wachstum zu erreichen. Ein Beispiel aus West-Bengalen zeigt, wie dort pathogene Erreger (E. coli) in den letzten Jahren zunehmend gegen das gesamte Arsenal an Antibiotika resistent wurden. Abbildung 2
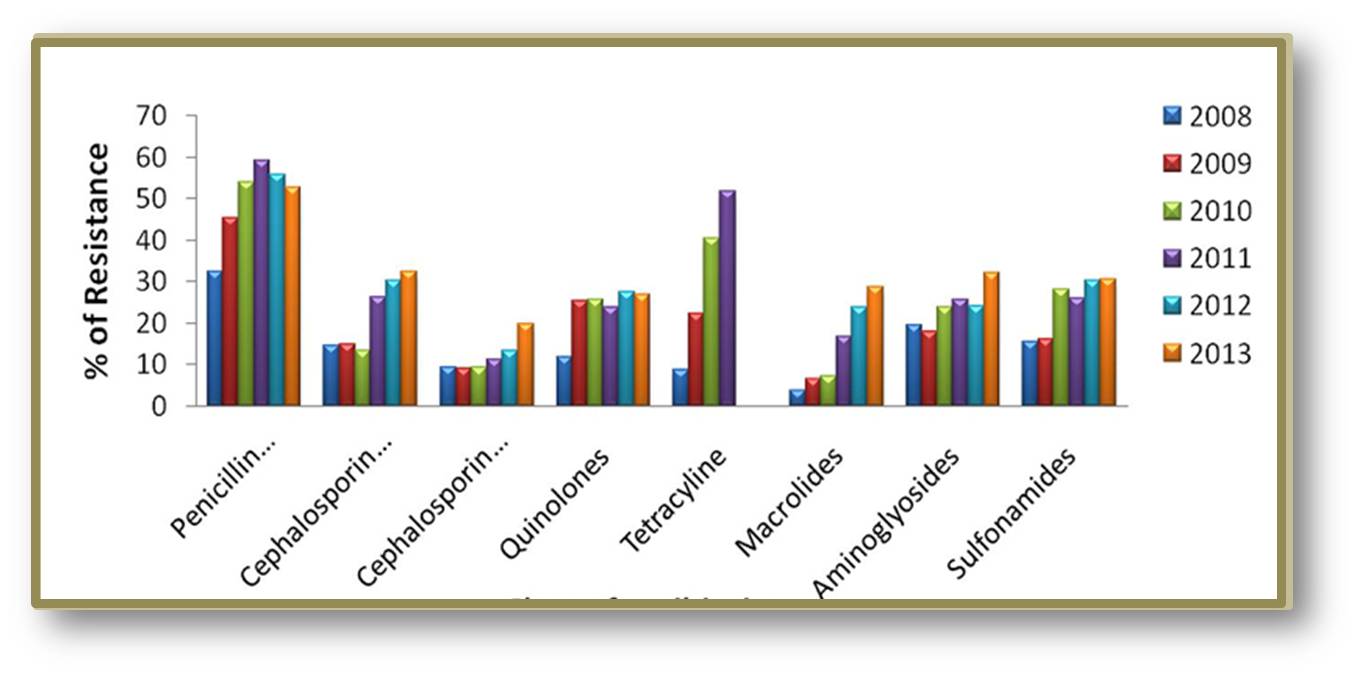 Abbildung 2 . Wie E.coli in den Jahren 2008 bis 2013 Resistenzen gegen das Spektrum von Antibiotika entwickelte. Insgesamt 5476 Isolate aus Harnproben (von Harnwegsinfektionen) wurden analysiert, rund 2/3 der enthaltenenKeime waren E. coli, rund 22 % Klebsiellen (die Resistenzentwicklung ist hier noch dramatischer). Bei den beiden Angaben zu Cephalosporinen handelt es sich um Cephalosporine der dritten und vierten Generation. Daten aus West-Bengalen, Indien (Quelle: S.Saha et al., Front. Microbiol., 18 September 2014 | http://dx.doi.org/10.3389/fmicb.2014.00463) cc-by-Lizenz
Abbildung 2 . Wie E.coli in den Jahren 2008 bis 2013 Resistenzen gegen das Spektrum von Antibiotika entwickelte. Insgesamt 5476 Isolate aus Harnproben (von Harnwegsinfektionen) wurden analysiert, rund 2/3 der enthaltenenKeime waren E. coli, rund 22 % Klebsiellen (die Resistenzentwicklung ist hier noch dramatischer). Bei den beiden Angaben zu Cephalosporinen handelt es sich um Cephalosporine der dritten und vierten Generation. Daten aus West-Bengalen, Indien (Quelle: S.Saha et al., Front. Microbiol., 18 September 2014 | http://dx.doi.org/10.3389/fmicb.2014.00463) cc-by-Lizenz
Dass Antibiotika gegen virale Infektionen wirkungslos sind, ist EU-weit leider noch nicht allgemein bekannt. Dies zeigt eine eben erschienene Eurobarometer-Umfrage [5]. Immerhin glauben über 40 % unserer Landsleute, dass Antibiotika gegen Erkältung und Grippe wirken und merkwürdigerweise nahezu zwei Drittel, dass Viren durch Antibiotika zerstört werden. Abbildung 3. Zweifellos haben diese Einschätzungen negative Auswirkungen auf die Nutzung, trägt zur weiteren Resistenzentwicklung bei.
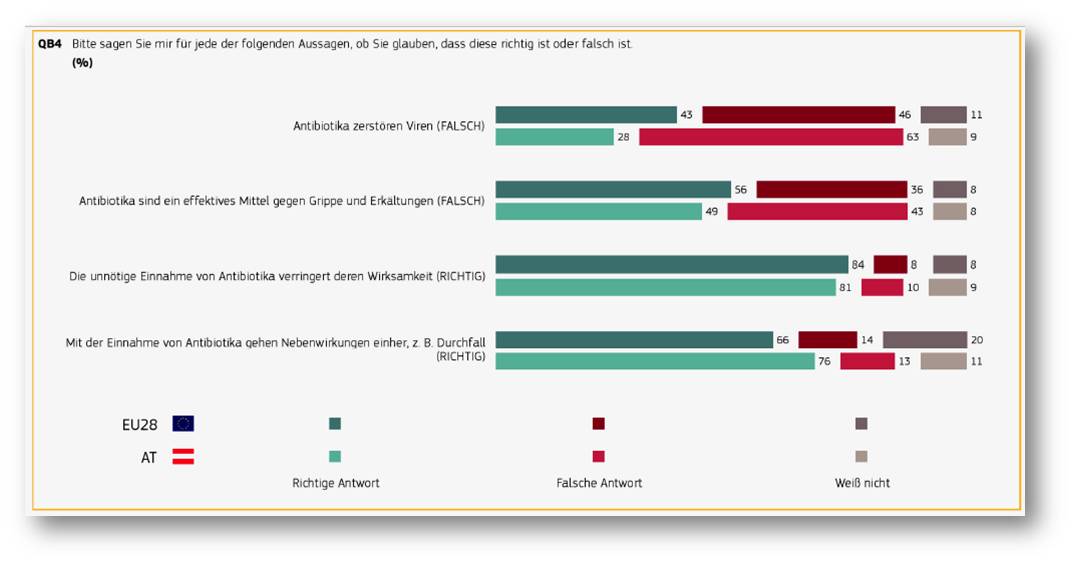 Abbildung 3. Spezial-Eurobarometer 445: Antibiotikaresistenz (April 2016). Fragen zur Wirksamkeit von Antibiotika gegen Viren, Grippe und Erkältungen, zum Wirkungsverlust durch Missbrauch und zu Nebenwirkungen. (Quelle: ebs_445_fac_at_de.pdf)
Abbildung 3. Spezial-Eurobarometer 445: Antibiotikaresistenz (April 2016). Fragen zur Wirksamkeit von Antibiotika gegen Viren, Grippe und Erkältungen, zum Wirkungsverlust durch Missbrauch und zu Nebenwirkungen. (Quelle: ebs_445_fac_at_de.pdf)
Wir haben dringenden Bedarf für neue Antibiotika
In etwas mehr als 50 Jahren wurde ein breites Arsenal an Antibiotika entdeckt und zu hochwirksamen Arzneimitteln optimiert : es waren dies vor allem die ersten Verteter der beta-Lactame - Penicillin (1938) und Cephalosporin -, Aminglykoside (1946), Tetracycline (1952), Makrolide (1951) und Chinolone (1968). Allerdings begannen sich bald Resistenzen auszubilden und zwar gegen alle Antibiotika. Bis nach der Einführung die ersten Resistenzen beobachtet wurden, dauerte es von weniger als 1 Jahr bis zu mehreren Jahren.
Erkrankungen durch multiresistente Bakterien sind nun nicht mehr selten: im Jahr 2013 waren es in den USA bereits rund zwei Millionen Menschen, von denen 23 000 starben; 400 000 Erkrankungen und eine ähnliche Zahl an Todesfällen - 25 000 wurden auch für die EU geschätzt.
Wenn sich diese Entwicklung fortsetzt, ohne dass neue Medikamente auf den Markt kommen, werden 2050 voraussichtlich bereits 10 Millionen Menschen an Infektionskrankheiten sterben, mehr als an der bisherigen Nummer 1, den Krebserkrankungen. Abbildung 4. 
Abbildung 4. Schlechte Aussichten für 2050: Infektionskrankheiten werden mehr Todesopfer fordern als Krebserkrankungen (Quelle: Niall McCarthy, https://www.statista.com/chart/3095/drug-resistant-infections. Lizenz: cc-by-nd
Antibiotika-Dämmerung
Der Anstieg von Resistenzen gegen vorhandene Antibiotika und die Entwicklung von multiresistenten Erregern, gegen die das vorhandene Arsenal an Antibiotika nichts mehr ausrichtet, wirkt bedrohlich. Insbesondere, weil offensichtlich vorhandene Wirkstoffe schneller unwirksam werden als innovative, neue auf den Markt kommen. Abbildung 5.
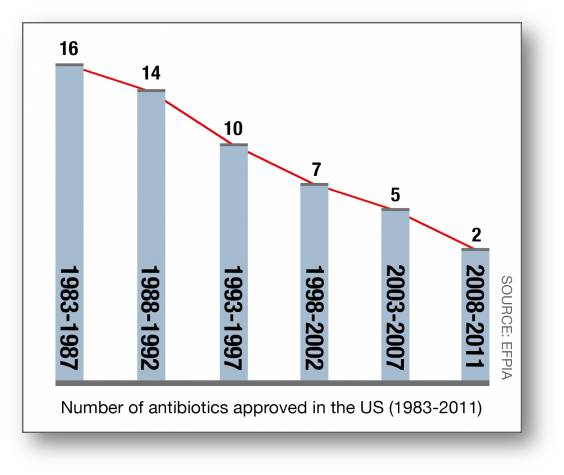 Abbildung 5. Die Zahl der in den USA neu-zugelassenen Antibiotika sinkt rapide (Quelle: EFPIA)
Abbildung 5. Die Zahl der in den USA neu-zugelassenen Antibiotika sinkt rapide (Quelle: EFPIA)
Die Gründe dafür sind erklärbar: Das "Goldene Zeitalter" der Antibiotikaforschung in den1950 - 1960-Jahren hat viele Pharmakonzerne bewogen in Infektionskrankheiten zu investieren. Praktisch alle großen Konzerne - Roche, Ciba, Sandoz, Pfizer, Bristol-Myers Squibb , Eli-Lilly und wie sie damals alle hießen - haben Forschungseinrichtungen gebaut, die sich nun diesem großen, erfolgsverheißenden Thema widmeten.
Einige Jahre später schlug bei nahezu allen Firmen die Aufbruchstimmung in eine Mischung aus wissenschaftlicher und kommerzieller Frustration um.
- Wissenschaftliche Frustration, weil trotz enormer Anstrengungen es nur wenige innovative, neue Substanzen bis in die klinische Prüfung schafften, und noch weniger den Markt erreichten. Der Blick auf das nun größer gewordene Arsenal der Antibiotika ließ das Marketing aber argumentieren, es gäbe bereits ausreichend Antibiotika, für neue bestünde nur mehr wenig Bedarf, sie würden nur miteinander konkurrieren. (Anders als bei nicht-ansteckenden chronischen Erkrankungen dauern Antibiotika-Therapien nur Tage bis wenige Wochen - man braucht also hohen Absatz, um die enormen Entwicklungskosten adzudecken.) Dass Resistenzentwicklung einen Kahlschlag unter den Antibiotika verursachen könnte, wusste man damals noch nicht.
- Kommerzielle Frustration, weil das Return on Investment (ROI) nicht den Erwartungen entsprach und das Management sich nach einiger Zeit Gebieten zuwandte, die lohnender schienen (O-Ton unseres Forschungsleiters bei Sandoz: "Wir wollen gutes Geld nicht dem schlechten Geld nachwerfen").
Später, als die Auswirkungen der Resistenzentwicklung klarer wurden, kam noch ein weiterer, sehr wichtiger kommerzieller Aspekt dazu: Um gegen ein neues hochwirksames Antibiotikum nicht schnell Resistenzen entstehen zu lassen, dürfte es nur äußerst sparsam eingesetzt werden, nur in Fällen, wo nichts anderes mehr helfen würde. Das heißt, das Mittel wäre dann im wesentlichen auf Spitäler beschränkt, die aber davon auch nur ganz wenige Packungen auf den Regalen stehen hätten, gleichbedeutend mit minimalem Absatz. Pharma müßte also die extrem hohen Forschungs-und Entwicklungskosten auf ein Produkt aufwenden, von dem dann nur sehr wenig Absatz findet. Wenn aber der geringe Absatz in den Preis kalkuliert wird, ist das Mittel nahezu unerschwinglich.
So endete für viele große Firmen der Ausflug in die Infektionskrankheiten relativ bald. Die Experten wurden anderen (Forschungs)richtungen zugeteilt oder freigesetzt, die sehr umfangreichen Sammlungen von pathogenen Bakterienstämmen wurden aufgelasen und das Das Know-How ging verloren. Sandoz stieg bereits 1986 aus den Infektionskrankheiten aus, das halbierte Forschungsinstitut in Wien widmete sich bis zu seiner Einebnung dem Hoffnungsgebiet Dermatologie. Interessanterweise wurde die anfangs der 1970er Jahre in Wien entdeckte Gruppe der Pleuromutiline nun wieder reanimiert, eine Substanz ist bereits in der letzten Phase der klinischen Prüfung.
Wie kann es weitergehen?
Sowohl auf der wissenschaftlichen Seite als auch auf der organisatorisch-ökonomischen Seite sind viele Fragen noch offen.
Was die unzähligen Naturstoffe betrifft, deren antibiotische Wirksamkeit man entdeckt hat, wissen wir nur von den allerwenigsten, wo ihre Angriffspunkte (Targets) im/am Bakterium liegen . Auf der anderen Seite hat man bis jetzt nur wenige der bakteriellen Genprodukte als Targets untersucht und verwendet. Hier liegt die Möglichkeit zu innovativen neuen Wirkstoffen, die man dann gezielt hinsichtlich Wirkspektrum und Stabilität und vor allem nach weniger (schweren) Nebenwirkungen optimieren kann.
Die organisatorisch-ökonomische Seite ist komplex: Wir brauchen dringendst neue Antibiotika - dafür ist hoher finanzieller und personeller Aufwand erforderlich - neue Antibiotika bleiben dann in Reserve/werden äußerst sparsam verwendet - der Aufwand wird nicht ersetzt. Dies ist für einzelne Firmen, aber auch für die öffentliche Hand (in den meisten Staaten) nicht machbar. Es sind nun eine Reihe auf Kooperation basierender Initiativen gegründet worden:
- Von besonderer Bedeutung ist hier die " Declaration by the Pharmaceutical, Biotechnology and Diagnostics Industries on Combating Antimicrobial Resistance" (January 2016) [6] Darin haben sich 85 Pharma-, Biotech-und Diagnostische Unternehmen (darunter die TOP-Unternehmen) auf gemeinsame globale Prinzipien in der Entwicklung neuer Arzneimittel , Diagnostika und Vaccinen geeinigt. (Über die Finanzierung wird allerdings nichts gesagt.)
- "New Drugs 4 Bad Bugs" (ND4BB) ist ein gemeinsames europäisches Projekt der "Innovative Medicines Initiative" (IMI) der EU und der "European Federation of Pharmaceutical Industries and Associations" (EFPIA), das Mittel (223,7 mio €) zur Unterstützung der Forschung von kleinen und mittleren Unternehmen und akademischen Einrichtungen zur Verfügung stellt.
- "Antimicrobial Resistance Diagnostic Challenge" ist ein 20 Mio$ Preis der "National Institutes of Health" (NIH) und deren "HHS Office of the Assistant Secretary for Preparedness and Response (ASPR)"
Wie der Wettlauf zwischen Resistenzentwicklung und Einführung neuer Antibiotika zu gewinnen ist? Die Red Queen (Alice im Wunderland (Carol Lewis)) würde dazu meinen:
"Now, here, you see, it takes all the running you can do, to keep in the same place. If you want to get somewhere else, you must run at least twice as fast as that!"
So einfach wäre das! :-)
[2] Beipackzettel https://www.bayer.at/static/documents/produkte/gi/Ciprox500FT.pdf
[3] http://www.who.int/medicines/publications/essentialmedicines/EML2015_8-M...
[4] Antibiotics Currently in Clinical Development http://www.pewtrusts.org/~/media/assets/2015/12/antibiotics_datatable_20...
[5] Spezial-Eurobarometer 445: Antibiotikaresistenz (April 2016). ebs_445_fac_at_de.pdf
[6] Declaration by the Pharmaceutical, Biotechnology and Diagnostics Industries on Combating Antimicrobial Resistance. January 2016. https://amr-review.org/sites/default/files/Declaration_of_Support_for_Co...
Weiterführende Links
Wie wirken Antibiotika? Video 5:44 min. Eine sehr leicht verständliche Zusammenfassung (2015; Standard YouTube Lizenz)
Wachsende Bedrohung durch Keime und gleichzeitig steigende Antibiotika-Resistenzen? Video 7:18 min (aus der Uniklinik Bonn - stimmt auch für Österreich) Standard YouTube Lizenz.
Warum gibt es Antibiotika-Resistenzen? Video 2:43 min (Standard YouTube Lizenz)
- Printer-friendly version
- Log in to post comments
