Do, 31.10.2019 — Nora Schultz
Die Psyche und ebenso ihre Erkrankungen sind stofflich solide verankert. Die Entwicklungsbiologin Nora Schultz gibt einen Überblick wie Neurotransmitter, neuronale Netze und Genvarianten Aufschluss über psychiatrische Mechanismen und Risiken geben, und wie auch das Immunsystem und die Darmflora dabei mitmischen. *
René Descartes kannte noch zwei klar unterscheidbare Zutaten des Menschen: das Körperliche, die res extensa oder „ausgedehnte Substanz“, und das Geistige, die res cogitans oder „denkende Substanz“, zu der er neben den Gedanken auch alle weiteren Aspekte der Psyche zählte. Dieser auch als Dualismus bezeichnete Denkansatz hallt bis heute nach. Noch immer werden Körper und Psyche vielfach als getrennte Sphären wahrgenommen – Erkrankungen der Psyche gelten infolge als stofflich kaum begreifbar oder sogar als reine Einbildung.
Tatsächlich wissen wir inzwischen, dass die Psyche keineswegs in einem körperlichen Vakuum schwebt. Descartes‘ ursprüngliche Idee, dass Körper und Geist exklusiv über die Zirbeldrüse miteinander in Austausch stehen, hat sich zwar inzwischen als falsch herausgestellt. Doch über die echten stofflichen Wurzeln und Blüten des menschlichen Geistes – und somit auch seiner Erkrankungen – wird immer mehr bekannt.
Lehrreiche Nebenwirkungen
Die ersten großen Durchbrüche gelangen in den 1950er und 1960er Jahren, als Forscher erstmals zu ahnen begannen, wie manche Chemikalien sich auf das Gemüt auswirken. Die Tuberkulosepatienten in der Sea View Klinik auf Staten Island etwa erholten sich 1952 nach Einnahme des neuen Medikaments Iproniazid nicht nur von ihrer Infektionskrankheit, sondern tanzten plötzlich euphorisch durch die Gänge. Das ursprünglich als allergielinderndes Antihistaminikum entwickelte Medikament Chlorpromazin wurde, nachdem Ärzten seine beruhigende Wirkung aufgefallen war, 1952 mit dramatischen Erfolgen zur Behandlung von manischen und schizophrenen Patienten eingesetzt. Erst im folgenden Jahrzehnt entdeckten Forscher wie der Schwede Arvid Carlsson, der dafür 2000 den Nobelpreis erhielt, die Botenstoffe im Gehirn, deren Wirkung von diesen Medikamenten beeinflusst wurde, allen voran Dopamin, Serotonin und Glutamat.
Vor allem zwischen Serotonin und Dopamin und wichtigen psychischen Erkrankungen wurden bald Zusammenhänge entdeckt. Abbildung 1. Die Beobachtungen, dass eine Depression oft von einem Mangel an Serotonin begleitet wird und Schizophrenie von Dopaminüberschüssen, haben bis heute Bestand. Allerdings erweist sich die Sache als wesentlich komplexer, wie die Forschung in den nachfolgenden Jahrzehnten aufgedeckt hat [1].
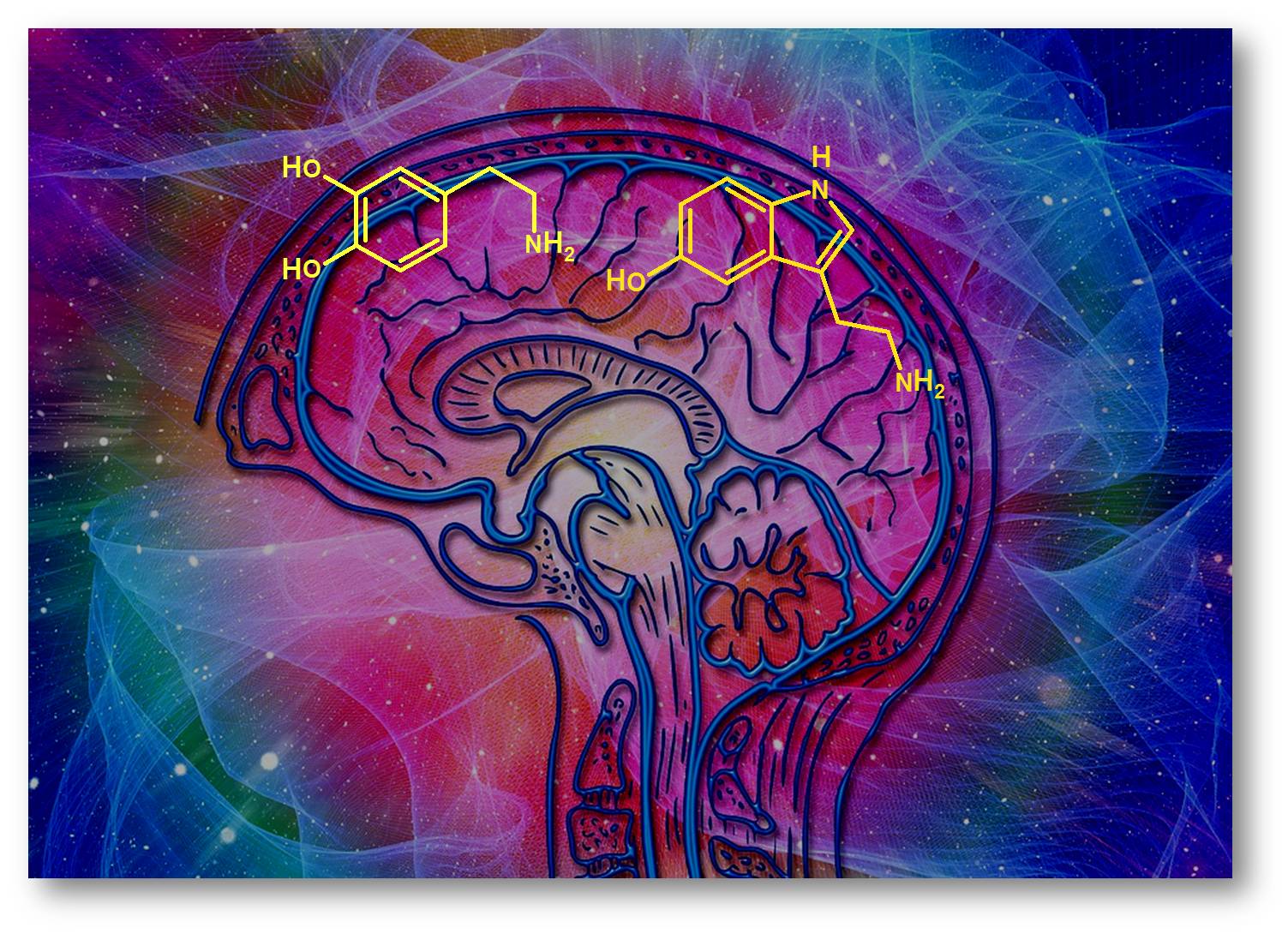 Abbildung 1. Zu den wichtigsten Neurotransmittern zählen Dopamin (links oben) und Serotonin (rechts oben); Mangel oder Überschuss können zu psychiatrischen Krankheitsbildern führen.(Das von Pixabay stammende Bild ist gemeinfrei und wurde von der Redaktion modifiziert und. eingefügt).
Abbildung 1. Zu den wichtigsten Neurotransmittern zählen Dopamin (links oben) und Serotonin (rechts oben); Mangel oder Überschuss können zu psychiatrischen Krankheitsbildern führen.(Das von Pixabay stammende Bild ist gemeinfrei und wurde von der Redaktion modifiziert und. eingefügt).
So bestätigte sich zwar, dass ein Dopaminüberschuss etwa im limbischen System zu Reizüberüberflutung und dadurch zu den sogenannten pychotischen Plussymptomen des schizophrenen Krankheitsbilds beitragen kann, also etwa Wahnvorstellungen oder Halluzinationen. Für die ebenfalls auftretenden Minussymptome – emotionaler oder sozialen Rückzug zum Beispiel – wird hingegen inzwischen eine verminderte Dopaminübertragung mitverantwortlich gemacht, vor allem im Stirnhirn. Auch eine reduzierte Übertragung des Neurotransmitters Glutamat im präfrontalen Cortex und in den Verbindungen zu tiefer gelegenen Kerngebieten wie dem Striatum, spielen wahrscheinlich eine Rolle. Zudem beeinflussen sich das Dopaminsystem und das Glutamatsystem gegenseitig.
Auch der Zusammenhang zwischen Serotonin und Depressionen hat sich längst nicht als so eindeutig entpuppt, wie ursprünglich angenommen. Selektive Serotonin-Wiederaufnahme-Hemmer (SSRI) wie der bekannte Wirkstoff Fluoxetin wirken zwar bei vielen Betroffenen gut gegen Depressionen. Oftmals stellt sich der Effekt jedoch erst nach vielen Wochen der Behandlung ein. Würde sich eine erhöhte Serotoninkonzentration in den Synapsen direkt auf die Stimmung auswirken, wäre dagegen ein viel schnellerer Effekt zu erwarten.
Neurogenese durch Antidepressiva?
Inzwischen deutet vieles darauf hin, dass Serotonin seine heilsame Wirkung dadurch entfaltet, dass es neuronale Wachstumsprozesse beeinflusst. Häufig ist in den Gehirnen von Menschen mit Depression ein verkleinerter Hippocampus zu finden – eine Hirnregion, die eine wichtige Rolle bei vielen Emotionen und Lernprozessen spielt. Unter dem Einfluss von Serotonin modellieren hier Neuronen ihre Synapsen beim Bilden von Gedächtnisinhalten besonders intensiv um. Und möglicherweise entstehen auch im Erwachsenenalter noch neue Nervenzellen. Genetisch veränderte Mäuse, denen der molekulare Kanal fehlt, mit dem Serotonin recycelt wird, reagierten trotzdem weniger depressiv auf chronischen Stress, wenn sie SSRI-Medikamente erhielten. Auch die vor einigen Jahren entdeckte antidepressive Wirkung des Schmerzmittels Ketamin beruht wohl darauf, dass die Substanz die neuronale Plastizität (d.i. die Fähigkeit von Synapsen, Nervenzellen und ganzen Hirnarealen, sich abhängig vom Grad ihrer Nutzung zu verändern) stimuliert. Das Wachstum neuer Nervenzellen ebenso wie das Entstehen frischer Verknüpfungen von Nervenzellen helfen dabei, der Depression zu entkommen – vermutlich, weil sie es erleichtern, einen besseren Umgang mit Stressfaktoren zu erlernen.
Neuronale Plastizität spielt auch bei der Schizophrenie eine Rolle. Fachleute betrachten die Krankheit inzwischen weitgehend als Entwicklungsstörung des Gehirns, bei der synaptische Umbauarbeiten im Jugendalter schief laufen. Es werden zu viele Verbindungen zwischen Nervenzellen wieder abgebaut und die Feinjustierung der Botenstoffsysteme während dieser Entwicklungsphase wird gestört. Doch was verursacht die Ungleichgewichte in den Signalsystemen? Die hohe Plastizität im jugendlichen Gehirn mag es anfälliger für zufällige Fehler machen, aber auch empfindlicher für intensive Eindrücke und Erlebnisse, die ihre Spuren in den Netzwerken und Transmittersystemen hinterlassen können. Jugenderfahrungen bleiben nachweislich besonders intensiv im Gedächtnis haften und haben einen großen Einfluss darauf, wie sich Persönlichkeit und Verhaltensmuster ausformen. Jugendliche reagieren auch mit größerer Wahrscheinlichkeit heftig oder nachhaltig auf die Einnahme psychoaktiver Drogen wie Cannabis: Das Schizophrenie-Risiko steigt.
Auch bei Erwachsenen können intensiver Stress und emotionale Belastungen sowie Drogenkonsum psychiatrische Erkrankungen begünstigen. So treten Depressionen, Schizophrenie und Angststörungen häufig infolge besonders herausfordernder Lebensereignisse auf, seien es Komplikationen während Schwangerschaft und Geburt oder traumatische Erlebnisse wie Todesfälle, Gewalt oder Missbrauch. Studien zeigen, dass Stress genau entgegengesetzt zu Antidepressiva auf die Neubildung von Nervenzellen und synaptischen Verbindungen wirkt – er behindert beides. Abbildung 2.
 Abbildung 2. Auswirkungen auf die Psyche durch Entzündungsprozesse, Stressreaktionen und auch durch die Darmflora.
Abbildung 2. Auswirkungen auf die Psyche durch Entzündungsprozesse, Stressreaktionen und auch durch die Darmflora.
Gestörte Konnektivität
Mithilfe funktioneller Magnetresonanz-Bildgebung lassen sich die neuronalen Verknüpfungen eines Gehirns als „Konnektom“ darstellen. Eine Untersuchung solcher Konnektome von über 1.000 Menschen mit und ohne psychiatrische Erkrankungen ergab, dass sowohl bei Patienten mit psychotischen Symptomen als auch bei solchen mit Depressionen im Vergleich zu Gesunden die neuronalen Verknüpfungen im frontoparietalen Netzwerk reduziert sind. Je massiver die Störung des Netzwerks, desto schwerer sind die Symptome. Die Details unterscheiden sich jedoch je nach Krankheitsbild. So finden sich im Gehirn von Menschen, die „nur“ an Depressionen oder einer bipolaren Störung leiden, vor allem Auffälligkeiten in den frontoparietalen und limbischen Netzwerken. Wer an psychotischen Symptomen leidet, zeigt hingegen oft breiter gestörte Konnektivität, die auch das Ruhezustandsnetzwerk betrifft.
Die Psyche ist aber auch jenseits der neuronalen Netze viel intensiver und komplexer körperlich verankert, als ursprünglich angenommen. So häufen sich mittlerweile die Hinweise darauf, dass auch Entzündungsprozesse und die Darmflora Auswirkungen auf die Psyche haben können. Entzündungen entstehen z. B. in Reaktion auf Infektionen oder Verletzungen, aber auch Stress, und dienen eigentlich dazu, durch erhöhte Temperatur und Immunaktivitäten Erregern den Garaus zu machen. Betrifft die Entzündungsreaktion den gesamten Körper, schlägt sie sich auch in typischen Krankheitssymptomen wie Abgeschlagenheit, Gliederschmerzen, Müdigkeit und Appetitlosigkeit nieder, die dazu verleiten, sich ins Bett zu verkriechen und sich auszukurieren.
Bleiben Entzündungswerte und -symptome dauerhaft erhöht, z.B. durch chronischen Stress oder chronische entzündliche Erkrankungen wie Diabetes oder Rheuma, können sich diese Symptome zu einer depressiven Dauerverstimmung auswachsen. Chronische Entzündungen und Depressionen treten häufig gemeinsam auf. Es gibt Hinweise darauf, dass die an Entzündungsprozessen beteiligten Botenstoffe die Blut-Hirn-Schranke überwinden und sich direkt auf Neurotransmittersysteme auswirken. Entzündungsfördernde Zytokine können zum Beispiel die Produktion von Serotonin mindern oder die Aktivität von Serotonin-Transportern erhöhen und so die Serotonin-Ungleichgewichte begünstigen, die sich bei vielen Depressionen zeigen. Zudem haben Wissenschaftler beobachtet, dass Entzündungsstoffe neurotoxisch wirken oder die Neurogenese im Hippocampus hemmen können.
Vom Darm ins Gehirn
Dass auch Darmbakterien sich auf die Psyche auswirken können, ist eine relativ neue Erkenntnis. Sie wirken offenbar über das Immunsystem, indem sie etwa spezialisierte Abwehrzellen auf den Plan rufen und Entzündungen fördern. Tatsächlich kann dies Immunzellen im Darm dazu anregen, Chemikalien zu produzieren, die bis ins Gehirn gelangen und dort psychiatrisch relevante Effekte entfalten. Einige Darmbakterien produzieren aber auch selbst psychiatrisch wirksame Substanzen oder stimulieren den Vagusnerv, der Signale aus dem Darm direkt ins Gehirn weiterleitet. Schraubt man am Gleichgewicht der Darmflora, kann das therapeutische Effekte haben. Sowohl die direkte Gabe erwünschter Mikroorganismen (Probiotika) als auch ein Plus an bestimmten Ballaststoffen in der Nahrung, die das Wachstum solcher Organismen im Darm fördern (Präbiotika), vermögen etwa Angststörungen positiv zu beeinflussen.
Ob eine psychiatrische Störung auftritt oder sich durch gezielte Eingriffe in die bislang bekannten biologischen Mechanismen beeinflussen lässt, hängt allerdings auch von genetischen Faktoren ab. Liegen risikofördernde Genvarianten vor, kann dies das Entstehen psychiatrischer Erkrankungen begünstigen und das therapeutische Bemühen erschweren. Genomweite Assoziationsstudien haben bereits Zusammenhänge zwischen etlichen Genvarianten und dem Auftreten von Störungen wie Schizophrenie oder Depression entdeckt. Sie betreffen zum Beispiel Proteine, die am Dopamin- oder Glutamatsystem beteiligt sind oder eine Rolle in der synaptischen Funktion und der neuronalen Entwicklung spielen. Eine Variante des Gens für den Wachstumsfaktor BDNF zum Beispiel produziert eine weniger verfügbare Form des Proteins, was vermutlich Einschränkungen bei der Neurogenese und synaptischen Plastizität nach sich zieht. Träger der Variante haben einen kleineren Hippocampus und entwickeln infolge starker Stressbelastungen, wie sie etwa nach einem Trauerfall oder einer Scheidung auftreten können, eher Depressionen oder Angststörungen als Menschen ohne diese Genvariante.
400 Jahre sind vergangen, seit René Descartes versuchte, die Wechselwirkungen zwischen Körper und Geist zu ergründen. Seine Nachfahren mögen voller Stolz auf den enormen Wissensschatz verweisen, den Wissenschaftler seitdem zusammengetragen haben, sowie auf die unzähligen Details, die auf die stofflichen Grundlagen von Gemütserkrankungen verweisen. Noch immer aber ist das Puzzle nicht komplett. Und mit der Umsetzung ihrer Erkenntnisse steht die moderne psychiatrische Forschung womöglich gerade erst am Anfang.
[1] O. Howes et al., Glutamate and dopamine in schizophrenia: an update for the 21st century. J Psychopharmacol. 2015 February ; 29(2): 97–115. doi:10.1177/0269881114563634
*Der Artikel stammt von der Webseite www.dasGehirn.info, einer exzellenten Plattform mit dem Ziel "das Gehirn, seine Funktionen und seine Bedeutung für unser Fühlen, Denken und Handeln darzustellen – umfassend, verständlich, attraktiv und anschaulich in Wort, Bild und Ton." (Es ist ein Projekt der Gemeinnützigen Hertie-Stiftung und der Neurowissenschaftlichen Gesellschaft e.V. in Zusammenarbeit mit dem Zentrum für Kunst und Medientechnologie Karlsruhe). Im Fokus des Monats Oktober steht die "Zukunft der Psychiatrie", zu dem auch der vorliegende, unter einer cc-by-nc-sa Lizenz stehende Text unter dem Titel "Die Substanz der Psyche" erschienen ist. Der Artikel wurde von der Redaktion geringfügig für den Blog adaptiert und es wurden Abbildungen eingefügt.
Weiterführende Literatur
- Dinan TG, Stanton C, Cryan JF: Psychobiotics: A Novel Class of Psychotropic.Biological Psychiatry. 2013 Nov; 74(10): 720–726 (zum Abstract).
- Amodeo G, Trusso MA, Fagiolini A: Depression and Inflammation: Disentangling a Clear Yet Complex and Multifaceted Link.Neuropsychiatry. 2017. 7(4): 448-457 (zum Volltext).
- Durstewitz D, Koppe G, Meyer-Lindenberg A: Deep Neural Networks in Psychiatry. Molecular Psychiatry. 2019. doi: 10.1038/s41380-019-0365-9 (zum Volltext).
- Printer-friendly version
- Log in to post comments

