Do, 02.02.2017 - 11:42 — Francis S. Collins

![]() In der Forschung zur Gentherapie gibt es eine immerwährende Herausforderung: Es ist die Suche nach einem verlässlichen Weg, auf dem man eine intakte Kopie eines Gens sicher in relevante Zellen einschleusen kann, welches dann die Funktion eines fehlerhaften Gens übernehmen soll. Mit der aktuellen Entdeckung leistungsfähiger Instrumente der Genchirurgie ("Gene editing"), insbesondere des CRISPR-Cas9 Systems - beginnen sich nun die Chancen einer erfolgreichen Gentherapie zu vergrößern. Francis Collins, Direktor der US National Institutes of Health (NIH) und ehem. Leiter des "Human Genome Project" berichtet hier von einer zukunftsweisenden Untersuchung , die nicht nur Fortschritte in der Heilung der seltenen Erbkrankheit "septische Granulomatose" verspricht, sondern auch von vielen anderen Erbkrankheiten.*
In der Forschung zur Gentherapie gibt es eine immerwährende Herausforderung: Es ist die Suche nach einem verlässlichen Weg, auf dem man eine intakte Kopie eines Gens sicher in relevante Zellen einschleusen kann, welches dann die Funktion eines fehlerhaften Gens übernehmen soll. Mit der aktuellen Entdeckung leistungsfähiger Instrumente der Genchirurgie ("Gene editing"), insbesondere des CRISPR-Cas9 Systems - beginnen sich nun die Chancen einer erfolgreichen Gentherapie zu vergrößern. Francis Collins, Direktor der US National Institutes of Health (NIH) und ehem. Leiter des "Human Genome Project" berichtet hier von einer zukunftsweisenden Untersuchung , die nicht nur Fortschritte in der Heilung der seltenen Erbkrankheit "septische Granulomatose" verspricht, sondern auch von vielen anderen Erbkrankheiten.*
Fortschritte in der Genchirurgie ("Gene editing")
Anstatt, dass man mit einer, ein sperriges Gen enthaltenden Injektionsnadel die Zellmembran durchstößt, versuchen die Forscher die Instrumente des "Gene editings" nun direkt in den Zellkern zu bringen: Ziel ist es, die Krankheit verursachenden Fehler in einem Gen herauszuschneiden und so seine korrekte Funktion zu ermöglichen. Abbildung 1.
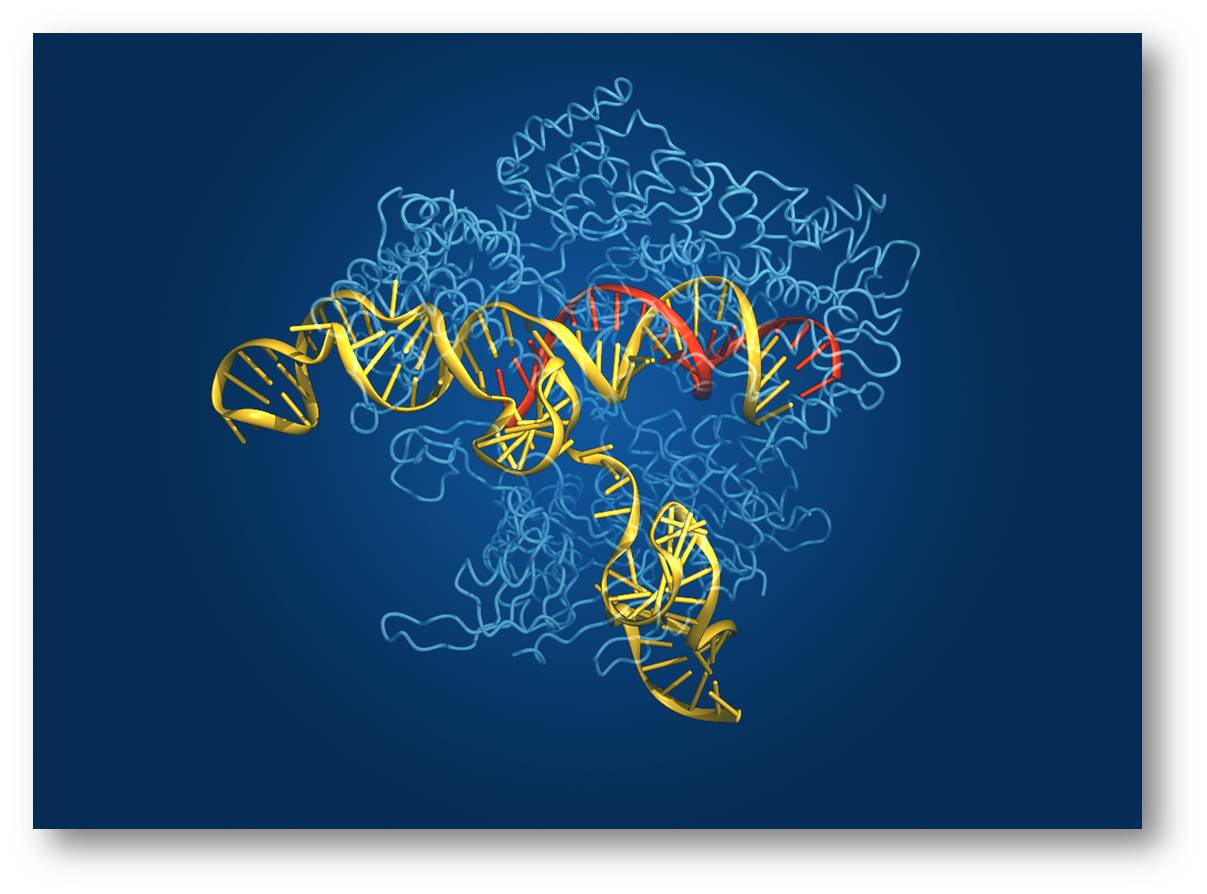 Abbildung 1. Das CRISPR/Cas9 System ermöglicht Mutationen gezielt aus einem Gen zu entfernen und durch eine korrekte Version zu ersetzen. Das ursprünglich in Bakterien entdeckte Enzym Cas9 (Kristallstruktur, hellblau) kann eine DNA (gelb) an der gewünschten Stelle durchschneiden. Die präzise Positionierung der Schnittstelle wird durch ein an Cas9 gebundenes kurzes Gegenstück zur zu schneidenden DNA - einer "guide RNA" (rot) - ermöglicht. (Credit: Bang Wong, Broad Institute of Harvard and MIT, Cambridge, MA)
Abbildung 1. Das CRISPR/Cas9 System ermöglicht Mutationen gezielt aus einem Gen zu entfernen und durch eine korrekte Version zu ersetzen. Das ursprünglich in Bakterien entdeckte Enzym Cas9 (Kristallstruktur, hellblau) kann eine DNA (gelb) an der gewünschten Stelle durchschneiden. Die präzise Positionierung der Schnittstelle wird durch ein an Cas9 gebundenes kurzes Gegenstück zur zu schneidenden DNA - einer "guide RNA" (rot) - ermöglicht. (Credit: Bang Wong, Broad Institute of Harvard and MIT, Cambridge, MA)
Während diese Forschung gerade anläuft, wurden bereits Fortschritte in einer seltenen, angeborenen Immunschwäche, der sogenannten "septischen Granulomatose" (CGD - chronic granulomatous disease), erzielt.
In einer jüngst in Science Translational Medicine erschienenen Arbeit beschreiben NIH-Forscher, wie sie mit Hilfe des CRISPR/Cas9-Systems eine Mutation in adulten hämatopoietischen (blutbildenden) Stammzellen korrigieren konnten, die eine übliche Form der CGD verursacht [1]. Besonders anzumerken ist dabei, dass diese Korrektur erfolgt, ohne dass irgendwelche neuen und möglicherweise Krankheit verursachenden Fehler in den benachbarten DNA-Sequenzen auftreten.
Als derart behandelte, humane Zellen in Mäuse transplantiert wurden, siedelten sich die Zellen ganz korrekt im Knochenmark an und begannen voll funktionsfähige weiße Blutkörperchen zu erzeugen. Die chirurgisch veränderten Zellen blieben bis zu 5 Monate in Knochenmark und Blutstrom der Tiere nachweisbar - ein prinzipieller Beweis dafür, dass die lebenslange genetische Krankheit CGD und ähnliche Defekte eines Tages geheilt werden können und dies ohne die Risiken und Einschränkungen unserer gegenwärtigen Behandlungen.
Was ist Septische Granulomatose (CGD)?
Menschen, die an CGD leiden, tragen eine oder mehrere genetische Mutationen, die es ihren weißen Blutkörperchen unmöglich machen, infektiöse Eindringlinge - Bakterien, Pilze - anzugreifen und abzutöten. Es sind dies Defekte auf Genen, die für einen Enzymkomplex kodieren, welcher für die antimikrobielle Aktivität verantwortlich ist. Dabei handelt es sich um Komponenten des Enzyms NADPH-Oxidase 2 (NOX2), das reaktiven Sauerstoff (Superoxid) generiert und damit Neutrophile zur Abtötung von Krankheitserregern befähigt (Anm. Red.).
CGD-Patienten müssen daher spezielle Maßnahmen ergreifen, um sich zu schützen; dies inkludiert auch eine permanente Einnahme von Medikamenten gegen diverse Infektionen. Aber auch dann besteht das Risiko lebensbedrohender Infektionen mit Bakterien und Pilzen.
Finden und Ersetzen
Wissenschafter am NIH’s National Institute for Allergy and Infectious Diseases (NIAID) haben nun begonnen das Potential der CRISPR/Cas9 Genschere auszutesten, um Menschen mit GCD helfen zu können [1]:
In einem ersten Schritt haben sie adulte Stammzellen von zwei Patienten gewonnen, die dieselbe GCD-verursachende Mutation aufwiesen - im konkreten Fall war es ein einzelner Buchstabe (d.i. ein einzelnes Nukleotid) in der Sequenz eines Gens auf dem X-Chromosom - und haben sodann die Fähigkeit des CRISPR/Cas9-Systems getestet diese Mutation herauszuschneiden. Abbildung 2.
 Abbildung 2. Die zu den weißen Blutkörperchen gehörenden neutrophilen Granulozyten ("Neutrophile") sind essentiell in die Bekämpfung von Infektionen involviert. Links: Zwei Neutrophile in einer Mehrzahl von roten Blutkörperchen (Bild von der Redaktion eingefügt; Quelle: Wikipedia, Mgiganteus (talk | contribs) disease.CC BY-SA 3.0). Rechts: Ein Neutrophiler, dessen DNA "korrigiert" wird, um seine Fähigkeit zur Infektionsabwehr wieder herzustellen (Quelle: Jill George, NIH).
Abbildung 2. Die zu den weißen Blutkörperchen gehörenden neutrophilen Granulozyten ("Neutrophile") sind essentiell in die Bekämpfung von Infektionen involviert. Links: Zwei Neutrophile in einer Mehrzahl von roten Blutkörperchen (Bild von der Redaktion eingefügt; Quelle: Wikipedia, Mgiganteus (talk | contribs) disease.CC BY-SA 3.0). Rechts: Ein Neutrophiler, dessen DNA "korrigiert" wird, um seine Fähigkeit zur Infektionsabwehr wieder herzustellen (Quelle: Jill George, NIH).
Das CRISPR/Cas9-System
verwendet kleine RNA-Moleküle - sogenannte "guide RNAs" zusammen mit einem scherenartig wirkenden Enzym Cas9 um präzise am richtigen Ort die defekte Stelle in der DNA-Sequenz zu finden und dort zu schneiden (siehe Abbildung 1). Wenn die DNA durchgeschnitten ist, schließt die Zelle den Eingriff ab, indem sie die korrekte Gensequenz einsetzt - diese wird von den Forschern in Form eines DNA-Fragments als Vorlage zur Verfügung gestellt. Man kann diesen Vorgang als ein Finden und Ersetzen sehen.
In ihrem in vitroTestsystem haben die Forscher festgestellt, dass mittels CRISPR/Cas9 etwa 20 - 30 % der Stammzellen "repariert werden konnten. Dort, wo die Genchirurgie funktionierte, war ausschliesslich die defekte Sequenz ersetzt worden. Die guide RNA war tatsächlich genügend spezifisch, um die DNA-Sequenz mit dem falschen Buchstaben zu finden und zu ersetzen.
Genkorrigierte humane Zellen funktionieren in Mäusen
Diese Ergebnis führte zur nächsten groß angelegten Untersuchung, in welcher die Forscher jeweils rund 500 000 der Gen-modifizierten humanen Zellen in jedes Versuchstier einbrachten. Da die Mäuse immundefizient waren und mit dem Zytostatikum Busulfan vorbehandelt worden waren, um die eigenen blutbildenden Zellen zu unterdrücken und für die transplantierten Zellen Platz zu machen, akzeptierten die Tiere die humanen Zellen und gestatteten es, dass deren Immunsystem "in Betrieb" ging.
Zweifelsfrei haben die Infusionen funktioniert. Die reparierten blutbildenden Stammzellen haben sich im Knochenmark der Mäuse angesiedelt und dort reife Blutzellen produziert, inklusive funktionierender neutrophiler Granulozyten, die ja den an GCD Erkrankten fehlen. Nach fünf Monaten trugen noch 10 - 20 % der Blutzellen die Korrektur. Das ist beachtlich viel, da eine langandauernde Präsenz des korrigierten Gens in nur10 % der Blutzellen wahrscheinlich ausreicht um Patienten zu nützen.
Zur Gentherapie am Menschen
Während diese Ergebnisse äußerst vielversprechend sind, muss allerdings noch sehr viel getan werden, bevor eine derartige Vorgehensweise in Patienten mit GCD getestet werden kann. Die Forscher sagen, dass sie die Genkorrektur in einen noch höheren Anteil der Stammzellen einfügen möchten. Der Prozess muss auch hochskaliert werden, um insgesamt viel mehr Zellen korrigieren zu können: Im Vergleich zu den mit 500 000 Zellen behandelten Mäusen werden ja für den ungleich größeren Menschen Hunderte Millionen korrigierter Stammzellen benötigt.
CRISPR Strategien bieten enorme Vorteile zur Präzision der Gentherapie, es zeigen sich aber auch andere Verfahren vielversprechend. Eine klinische Untersuchung ist derzeit an den NIH und anderen Stellen in den US im Laufen, die eine mehr konventionelle Gentherapie von CGD ins Auge fasst. Es wird dabei ein inaktiviertes, nicht-infektiöses Virus verwendet, um ein funktionelles Gen in die Zellen von GCD Patienten einzuschleusen. Es ist aber noch zu früh um zu wissen, ob dieser Ansatz erfolgreich sein wird; die ersten Hinweise sind aber sehr ermutigend.
Fazit
Die Forscher am NIAID haben Jahrzehnte damit verbracht die GCD besser zu verstehen und Wege aufzufinden um diese chronische, lebensbedrohende Krankheit effizienter behandeln zu können. Die jüngsten Ergebnisse sind als ein ermutigendes Zeichen eines Fortschritts zu sehen - nicht nur in der Behandlung von CGD, sondern auch von vielen anderen Erbkrankheiten.
Es ist eine Story, die es wert ist weiter verfolgt zu werden.
*Dieser Artikel von NIH Director Francis Collins, M.D., Ph.D. erschien unter dem Titel:" Find and Replace: DNA Editing Tool Shows Gene Therapy Promise" zuerst (am 24. Jänner 2017) im NIH Director’s Blog:. https://directorsblog.nih.gov/2017/01/24/find-and-replace-dna-editing-tool-shows-gene-therapy-promise/.
Reprinted (and translated by ScienceBlog) with permission from the National Institutes of Health (NIH).
[1] CRISPR-Cas9 gene repair of hematopoietic stem cells from patients with X-linked chronic granulomatous disease. De Ravin SS, Li L, Wu X, Choi U, Allen C, Koontz S, Lee J, Theobald-Whiting N, Chu J, Garofalo M, Sweeney C, Kardava L, Moir S, Viley A, Natarajan P, Su L, Kuhns D, Zarember KA, Peshwa MV, Malech HL. Sci Transl Med. 2017 Jan 11;9(372).
[2] Study of Gene Therapy Using a Lentiviral Vector to Treat X-linked Chronic Granulomatous Disease. Clinicaltrials.gov
Weiterführende Links
- Gen-editing mit CRISPR/Cas9 Video 3:13 min (deutsch) , Max-Planck Gesellschaft (2016) (Standard-YouTube-Lizenz )
Die Entdeckung, dass sich auch Bakterien mit einer Art Immunsystem gegen Viren wehren können, hat zunächst nur Mikrobiologen begeistert. Seitdem aber bekannt wurde, dass sich mit dem als CRISPR/Cas9 bezeichneten System das Erbgut unterschiedlichster Organismen manipulieren lässt, interessieren sich auch Nicht-Wissenschaftler für die neue Gentechnik-Methode. Doch wie funktioniert die Methode mit dem unaussprechlichen Namen? - Schöne neue Gentechnik - Neue Hoffnung in der Medizin - 3sat 2016 - myDoku, Video 44:17 min.
- Printer-friendly version
- Log in to post comments
