Do, 13.04.2017 - 07:19 — Redaktion 
![]()
Der Zusammenhang zwischen einer einfachen Genmutation und deren Konsequenz auf die Entwicklung ist komplexer ist, als man bisher angenommen hat. Das zeigt eine ausgedehnte Untersuchung (an der auch Forscher von der Medizinischen Universität in Wien beteiligt waren) an Mausembryonen: In Mäusen mit identem genetischen Hintergrund kann dieselbe Mutation eines Gens in den einzelnen Individuen zu einem unterschiedlichen Spektrum phänotypischer Anomalien führen.*
Wenn man untersuchen will, welche Rolle bestimmte Gene in der Entwicklung und bei Krankheiten des Menschen spielen, so verwendet man bereits seit langer Zeit Tiermodelle als experimentelle Surrogate. Da über die Tierspezies hinweg Gensequenzen und -Funktionen erstaunlich konserviert geblieben sind, hat dieser Ansatz zweifellos seine Berechtigung.
Die genmanipulierte Maus als Modell
Ein übliches Modell zur Erforschung der Genfunktion ist die genmanipulierte Maus. Das ambitionierteste der mit diesem Modell konzipierten Projekte wird derzeit vom International Mouse Phenotyping Consortium (IMPC) koordiniert und hat das Ziel einen Katalog der Funktionen aller Gene zu erstellen. Dazu werden systematisch Mauslinien generiert, in denen genomweit jeweils ein Gen ausgeschaltet ist (knock outs) und die individuellen Gen-knockouts (KO) phänotypisch charakterisiert. Die bis jetzt erfolgten Untersuchungen haben gezeigt, dass rund ein Drittel aller Gene lebensnotwendig sind. Schaltet man diese aus, so führt dies zum Absterben im Embryonalstadium oder um die Geburt herum.
Die Untersuchung derartiger KO-Mauslinien bietet somit eine einzigartige Möglichkeit einen Überblick über die genetischen Komponenten zu erhalten, welche die normale embryonale Entwicklung kontrollieren und - als Schlussfolgerung - welche Gene es sind, die auf Grund von Mutationen zu angeborenen Defekten oder Störungen in der Entwicklung des Menschen führen können.
Die Entschlüsselung der Mechanismen von Entwicklungsstörungen
(Mechanisms of Developmental Disorders- DMDD) ist ein vom Wellcome Trust finanziertes 5-Jahresprogramm, das vom Francis Crick Institute in England koodiniert wird. Das Ziel ist insgesamt 240 embryonal letale Mauslinien phänotypisch zu charakterisieren.
In einer groß-angelegten Studie (die vorgestern von den Reviewern akzeptiert wurde) hat ein Forscherteam insgesamt 220 Mäuseembryonen am Tag 14,5 ((E14,5), d.i. gegen das Ende der embryonalen Entwicklung) untersucht. In jedem dieser Embryos war jeweils eines von 42 Genen ausgeschaltet - untersucht wurden die homozygoten Mutanten (d.i. in den diploiden Zellen trugen beide Allele des Gens die Mutation, Anm. Red.). Wie ein normaler Embryo in diesem Stadium aussieht, ist in Abbildung 1 gezeigt .
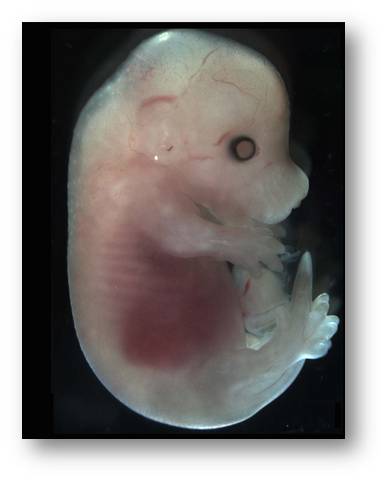 Abbildung 1. Normaler Mausembryo am Tag 14,5 der Entwicklung. Die Länge des Tieres beträgt etwa 13 mm. (Abbildung von der Redaktion beigefügt. Das Bild steht unter einer cc.by-Lizenz und stammt aus: Beck-Cormier S, Escande M, Souilhol C, Vandormael-Pournin S, Sourice S, Pilet P, et al. (2014) Notchless Is Required for Axial Skeleton Formation in Mice. PLoS ONE 9(5): e98507. https://doi.org/10.1371/journal.pone.0098507 )
Abbildung 1. Normaler Mausembryo am Tag 14,5 der Entwicklung. Die Länge des Tieres beträgt etwa 13 mm. (Abbildung von der Redaktion beigefügt. Das Bild steht unter einer cc.by-Lizenz und stammt aus: Beck-Cormier S, Escande M, Souilhol C, Vandormael-Pournin S, Sourice S, Pilet P, et al. (2014) Notchless Is Required for Axial Skeleton Formation in Mice. PLoS ONE 9(5): e98507. https://doi.org/10.1371/journal.pone.0098507 )
Abgesehen von dem jeweils ausgeschalteten Gen handelte es sich um Mäuse mit identem genetischen Hintergrund.
Indem die Forscher jeden Embryo in minutiösem Detail mittels eines High Resolution Episcope Microscope (HREM, siehe Video in: weiterführende Links) scannten, konnten sie auch winzigste Unterschiede in Merkmalen erkennen, ob es nun einzelne Nerven, Muskeln oder kleine Blutgefäße waren, die Anomalitäten aufwiesen. Die Bewertung der Phänotypen basierte schließlich auf der Analyse von mehr als 1,6 Millionen Bildern.
Das Ergebnis war völlig überraschend
In den einzelnen Individuen einer Linie genetisch identer Mäuse führte die Ausschaltung desselben essentiellen Gens zu einem Spektrum unterschiedlicher, teilweise überlappender physischer Merkmale und Anomalitäten. Dies ist in Abbildung 2 für vier unterschiedliche Mauslinien mit je fünf Individuen dargesstellt: die Differenz zwischen entdeckten Anomalitäten (rot) in den individuellen Tieren einer Linie ist frappant.
 Abbildung 2. Phänotypische Charakterisierung von vier Mauslinien, in denen jeweils ein essentielles Gen (hier die Gene Atp11a, Brd2, Celf4 und Tcf712) ausgeschaltet wurde. Die individuellen Embryonen einer Linie zeigen unterschiedliche, teilweise überlappende Anomalien. (Bild: ist aus [1], Figure 2 entnommen.)
Abbildung 2. Phänotypische Charakterisierung von vier Mauslinien, in denen jeweils ein essentielles Gen (hier die Gene Atp11a, Brd2, Celf4 und Tcf712) ausgeschaltet wurde. Die individuellen Embryonen einer Linie zeigen unterschiedliche, teilweise überlappende Anomalien. (Bild: ist aus [1], Figure 2 entnommen.)
Dies lässt darauf schließen, dass der Zusammenhang von Genmutation und deren Auswirkung wesentlich komplexer ist, als man bisher angenommen hat.
Ganz allgemein stellen Kliniker fest, dass Menschen, die denselben genetischen Defekt tragen, unterschiedliche Symptome mit unterschiedlichen Schweregraden zeigen können. Zum Teil dürfte dies wahrscheinlich darauf zurückgeführt werden, dass wir in unserem genauen genetischen Make-up differieren. Die Studie in Mäusen zeigt nun aber:
sogar wenn die einzelnen Individuen einen praktisch identen genetischen Hintergrund haben, kann dieselbe Mutation zu einer Vielfalt unterschiedlicher Ergebnisse in den betroffenen Embryonen führen.
In den Augen des Studienleiters Tim Mohum ist dies ein überaus verblüffendes Ergebnis: "Es zeigt uns, dass sogar mit einer anscheinend einfachen und wohldefinierten Mutation das Ergebnis komplex und variabel sein kann. Um zu verstehen, warum das so ist, müssen wir noch eine Menge über die Rolle dieser letalen Gene in der embryonalen Entwicklung dazulernen." Und Andrew Chisholm , Leiter der Cellular and Developmental Sciences von Wellcome und Finanzier von DMDD, meint: "Diese Untersuchung ändert unseren Blick auf das, was wir als eine einfache Beziehung angesehen haben, zwischen dem, was in unseren Genen kodiert ist und dem, wie wir uns entwickeln. Es ist eine zusätzliche Ebene der Komplexität, welche die Forscher nun miteinbeziehen müssen, ebenso wie das Bestreben die komplizierten Vorgänge der genetischen Steuerung zu entflechten."
*Der vorliegende Artikel basiert auf einem News Article des Wellcome Trust Sanger Institute vom 11.April 2017: http://www.sanger.ac.uk/news/view/how-genetic-mutations-affect-development-more-complex-previously-thought . Dieser Artikel wurde weitestgehend wörtlich übersetzt und durch ebenfalls übersetzte Teile (Einleitung) und Figure 2 aus der zugrundeliegenden Publikation ergänzt:
[1] Wilson R, Geyer SH, Reissig L et al. Highly variable penetrance of abnormal phenotypes in embryonic lethal knockout mice [version 1; referees: 1 approved, 2 approved with reservations] Wellcome Open Research 2016, 1:1 (doi: 10.12688/wellcomeopenres.9899.1).
Die Inhalte der Website des Sanger Instituts und auch [1] stehen unter einer cc-by 3.0 Lizenz.
Weiterführende Links
Wellcome Trust Sanger Institute: http://www.sanger.ac.uk/ (Motto: We use genome sequences to advance understanding of the biology of humans and pathogens to improve human health).
International Mouse Phenotyping Consortium: http://www.mousephenotype.org
High resolution episcopic microscopy (HREM). Wellcome Collection; Video (englisch) 5:10 min https://www.youtube.com/watch?v=t0WEHUpaxlI Tim Mohun, Leiter der oben besprochenen Studie, erklärt die Technik, die unglaublich detaillierte 3D-Bilder von winzigen Strukturen, u.a. von Maus -Embryonen ermöglicht.
Artikel im ScienceBlog
Francis S. Collins, 13.10.2016: Von Mäusen und Menschen: Gene, die für das Überleben essentiell sind.
- Printer-friendly version
- Log in to post comments
