Nobelpreis für Chemie 2018: Darwins Prinzipien im Reagenzglas oder "Gerichtete Evolution von Enzymen"
Nobelpreis für Chemie 2018: Darwins Prinzipien im Reagenzglas oder "Gerichtete Evolution von Enzymen"Do, 04.10.2018 - 14:03 — Inge Schuster 
![]()
Eine Revolution, die auf Evolution basiert - so kündigte Claus Gustafsson, Vorsitzender des Nobel-Komitees die bahnbrechenden Arbeiten zur "Gerichteten Evolution von Enzymen und Bindungsproteinen" an, die gestern mit dem Nobelpreis 2018 für Chemie ausgezeichnet wurden. Eine Hälfte des Preises ging an Frances H. Arnold, die mit Hilfe evolutionärer Methoden Enzyme optimiert und neu designt, sodass sie auch in der Natur noch unbekannte Reaktionen ausführen. Die andere Hälfte ging an George P. Smith und Sir Gregory P. Winter für die Methode des Phagen-Display, die von eminenter Bedeutung für die Herstellung von Biopharmaka, insbesondere von hochspezifischen Antikörpern ist. In Hinblick auf die Länge des Artikels wird im Folgenden nur über die Arbeiten von France H. Arnold berichtet.
Frances H. Arnold, aus Pittsburgh stammende US-Amerikanerin hatte ursprünglich Maschinenbau studiert, wandte sich dann aber der chemischen Verfahrenstechnik zu, worin sie 1985 an der University of Berkeley (California) promovierte. Beginnend als Postdoc am California Institute of Technology (Caltech) wurde sie zur Pionierin in der gerichteten Evolution von Enzymen; sie ist nun am Caltech Linus-Pauling-Professor für Chemieingenieurwesen, Biochemie und Bio-Ingenieurwesen. Ihre bahnbrechenden Arbeiten führen zu Enzymen mit Tausenden Male schnellerem Umsatz, zu neuen Enzymen, die in der Natur noch unbekannte Reaktionen katalysieren. Es ist gleichermaßen Grundlagenforschung und angewandte Forschung, die zur umweltfreundlichen, kostensparenden Herstellung eines sehr breiten Spektrums von Produkten führt: von Arzneimitteln bis zu Biotreibstoffen.
Die Erfolge haben Arnold (Abbildung 1) viele hochrangige Preise und Mitgliedschaften eingebracht. Besonders zu erwähnen ist der mit 1 Million € dotierte Milleniums-Technologie-Preis, den sie als erst Frau 2016 erhielt.
 Abbildung 1. Frances H. Arnold um 2012. (Bild: Wikipedia, Beaverchem2. cc-by-sa-Lizenz)
Abbildung 1. Frances H. Arnold um 2012. (Bild: Wikipedia, Beaverchem2. cc-by-sa-Lizenz)
Was ist gerichtete Evolution?
Seit Leben auf unserem Planeten entstanden ist, musste es sich an eine ständig verändernde Umwelt anpassen und in Konkurrenz mit anderen Lebensformen treten. Diese Anpassung erfolgte durch natürliche Evolution: Mutationen in Genen führten manchmal zu Proteinen, die besser mit der neuen Umwelt zurechtkamen und dies konnte dann in einer Selektion der betreffenden Spezies resultieren. Selektion bevorzugter Eigenschaften ist auch die Basis auf der wir Menschen über Jahrtausende Pflanzen und Haustiere für unsere Zwecke optimierten.
Seit der zweiten Hälfte des 20. Jahrhundert nimmt das Wissen über Strukturen und Funktionen von Proteinen zu und Wissenschafter sind bestrebt Proteine/Enzyme zu optimieren - für technische Anwendungen (z.B. Waschmittel) und ebenso zur Synthese von Arzneimitteln. Es ist ein ziemlich mühsames, langwieriges Unterfangen, da wir noch ziemlich weit davon entfernt sind aus punktuellen Änderungen in der Struktur auf Änderungen in den Eigenschaften schließen zu können: Jedes mutierte Gen wird isoliert in einem Mikroorganismus zur Expression gebracht, das betreffende Genprodukt dann auf Aktivität getestet, in den meisten Fällen wegen unbefriedigender Eigenschaften verworfen und anschliessend dann die nächste Genvariante getestet. Die gerichtete Evolution folgt dem natürlichen Prozess von Mutation und Selektion ist aber ungleich rascher als die konventionelle "Variante nach Variante" Vorgangsweise. Abbildung 2:
 Abbildung 2. Die gerichtete Evolution von Enzymen ist ein iterativer Prozess, der so lange wiederholt wird, bis die gewünschten Eigenschaften erreicht sind (Bild: ©Johan Jarnestad/The Royal Swedish Academy of Sciences”; Lizenz: cc-by-nc)
Abbildung 2. Die gerichtete Evolution von Enzymen ist ein iterativer Prozess, der so lange wiederholt wird, bis die gewünschten Eigenschaften erreicht sind (Bild: ©Johan Jarnestad/The Royal Swedish Academy of Sciences”; Lizenz: cc-by-nc)
Es beginnt damit, dass in das Gen für das zu optimierende Enzym Punktmutationen nach dem Zufallsprinzip eingefügt werden (Schritt 1; Mutationen rot markiert). Alle mutierten Gene werden dann in Bakterien zur Expression gebracht - eine ganze Bibliothek von Enzymvarianten entsteht (Schritt 2). Alle diese Varianten werden dann auf ihre Aktivität für eine bestimmte chemische Reaktion getestet (Schritt 3), diejenigen mit der höchsten Aktivität selektiert (die anderen verworfen) und in einen neuen Zyklus von Mutation und Selektion eingebracht (Schritt 4). Bereits nach einigen Zyklen können so Enzyme erhalten werden, die nun Tausend Mal schneller katalysieren als das Ausgangsenzym.
Dass diese Strategie funktioniert, konnte Arnold 1993 an Hand einer relativ kleinen Protease (Subtilisin E) demonstrieren: bereits nach vier Zyklen von Mutation und Selektion resultierte eine Form, die 256 mal schneller als das ursprüngliche arbeitete.
Enzyme der Cytochrom P450 Familie
Arnold hat in der Folge unterschiedliche Enzyme optimiert (hinsichtlich Thermostabilität, Aktivität in bestimmten Lösungsmitteln, etc.). Eine zentrale Rolle spielen Enzyme der sogenannten Cytochrom P450 Familie. Es ist dies eine riesengroße Familie an Enzymen, deren erster Vertreter bereits vor fast genau 60 Jahren entdeckt wurde. Derartige Enzyme finden sich bereits in den frühesten Lebensformen; ausgehend von einem Ur-P450 haben sie sich im Laufe der Evolution an die erstaunlichsten Lebensbedingungen angepasst und finden sich in Prokaryoten ebenso wie in praktisch allen höheren Organismen im Pilz-, Pflanzen-und Tierreich. Die Cytochrom P450 Enzyme katalysieren von Natur aus bereits eine Vielfalt an Reaktionen, die alle auf der Basis von Oxydation - in den meisten Fällen durch Einführung von reaktivem Sauerstoff in ein organisches Molekül - zu verstehen sind: es sind u.a. Hydroxylierungen aliphatischer und aromatischer C-H-Bindungen, Epoxydierungen, Desalkylierungen, Sulfoxydierungen, Nitrierungen, etc. Viele physiologischen Substanzen, wie z.B. Alkaloide, Cholesterin, Steroidhormone, Vitamin D, etc. benötigen spezifische P450-Formen für Synthese und Abbau, andere P450 Enzyme sind in den Abbau/die Entgiftung von Fremdstoffen - organischen Molekülen - involviert. Sofern sie lipophil (fettlöslich) sind und ihre Größe (Molekulargewicht) 1000 D nicht wesentlich übersteigt, werden praktisch alle Fremdstoffe aus Umwelt und Synthese über P450 Enzyme abgebaut.
Trotz ihrer einzigartigen enzymatischen Fähigkeiten konnten bis vor kurzem P450-Formen nicht in die industrielle Produktion von Substanzen eingesetzt werden. Der Grund dafür: die meisten P450-Formen sind Membranproteine und damit in wässrigem Milieu unlöslich, sie haben ungenügende Stabilität und häufig unbefriedigende Aktivität. Mit gerichteter Evolution lassen sich diese Eigenschaften nun optimieren. Die Einsatzmöglichkeiten sind Legion - um nur ein Beispiel zu nennen: mittels optimierter P450-Formen können - umweltverträglich, effizient und kostensparend - Biotreibstoffe (z.B. Isopropanol) aus kurzkettigen Alkanen produziert werden.
Neben der Optimierung vorhandener Cytochrom P450 Enzyme hat Arnold neue Fornen designt, die ungewöhnliche Reaktionen ausführen, welche in der synthetischen Chemie wohl möglich sind, jedoch nicht dem natürlichen Spektrum der P450-Formen entsprechen. Varianten der designten Form P411 (Abbildung 3) reduzieren beispielsweise Azide, führen Amingruppen ein und katalysieren andere für P450-Enzyme völlig neue Reaktionen - dabei geht alles im gewünschten Milieu mit sehr hoher Aktivität und Selektivität vor sich. 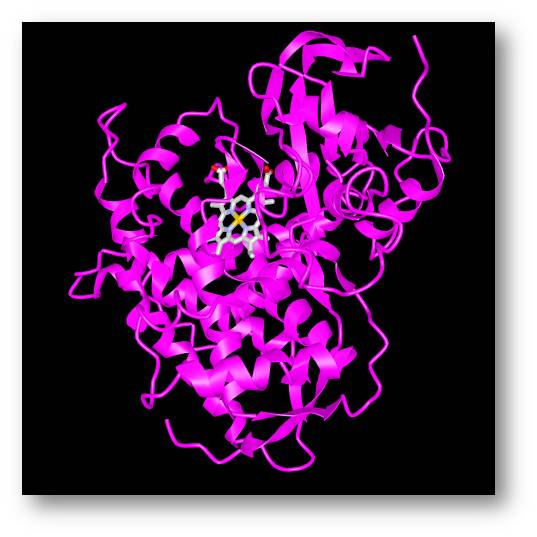
Abbildung 3. Struktur der Cytochrome P450-Variante P411: PDB 4H23 (Quelle: Proteindata Bank; Artikel: A serine-substituted P450 catalyzes highly efficient carbene transfer to olefins in vivo. Coelho PS, et al., Nat. Chem. Biol. (2013) 9 p.485-487)
Wohin geht die Reise?
Anwendungsorientiert entstehen immer mehr Enzyme mit katalytischen Fähigkeiten, die denen der klassischen synthetischen Chemie gleichwertig sind oder diese sogar übertreffen. Völlig neu sind beispielsweise Enzymvarianten eines Cytochrom c (ein Haemprotein wie P450), welche Kohlenstoff-Silicium-Bindungen knüpfen können - eine technologisch sehr wichtige Reaktion, die aber in der Natur nicht vorkommt. Das Ergebnis der gerichteten Evolution ergab ein Enzym, das 15 mal schneller arbeitete als der bislang beste Katalysator in der chemischen Synthese. Anwendungsmöglichkeiten der Reaktionsprodukte sind sehr weit, finden sich u.a. in der Produktion von Elastomeren, in der medizinischen Chemie, in bildgebenden Verfahren, u.a.
Die mittels gerichteter Evolution erhaltenen Enzyme zeichnen sich dadurch aus, dass sie innerhalb von lebenden Zellen funktionieren, für unterschiedliche Substrate, Aktivitäten und Selektivitäten optimiert werden können.Wir erleben einen Paradigmenwechsel: Favorisierte Reaktionen der synthetischen Chemie können mit der herausragenden Selektivität und Adaptierbarkeit enzymatischer Prozesse "vermählt" werden.
Tatsächlich wird Arnolds Methode der gerichteten Evolution heute bereits weltweit in sehr vielen Labors und Industrien eingesetzt. Die modifizierten Enzyme treten zunehmend an die Stelle von Prozessen der synthetischen Chemie, die zu kostspielig, langwierig und/oder kompliziert sind oder auch von solchen Prozessen, für die inadäquate Mengen fossiler Rohstoffe eingesetzt werden müssten. Oder, wie es Frances Arnold bereits 1999 ausgedrückt hat:
"My vision is of a biotechnology-based chemicals industry that makes no messes to clean up"
Weiterführende Links
TEDxUSC - Frances Arnold - Sex, Evolution, and Innovation Video 16:26 min (2012) (USC Stevens Center for Innovation cc-by-Lizenz)
Frances H. Arnold: New Enzymes by Evolution Lecture at the Molecular Frontiers Symposium at the Royal Swedish Academy of Sciences, Sweden, May 2017. Video 38:38 min.
Artikel im ScienceBlog zu verwandten Themen
- Themenschwerpukt Evolution
- Inge Schuster, 04.05.2017: Manfred Eigen: Von "unmessbar" schnellen Reaktionen zur Evolution komplexer biologischer Systeme
- Peter Schuster, 12.04.2012: Wie universell ist das Darwinsche Prinzip?
- Rita Bernhardt, 13.02.205: Aus der Werkzeugkiste der Natur - Zum Potential von Cytochrom P450 Enzymen in der Biotechnologie
- Inge Schuster, 25.01.2014: Cytochrom P450-Enzyme: Tausendsassas in allen Bereichen unserer Biosphäre
- Inge Schuster, 17.11.2011: Zu Wirkung und Nebenwirkungen von Medikamenten