So, 19.04.2026— Inge Schuster
Wirksame Therapien gegen Alzheimer Demenz sind dringendst erforderlich. Basierend auf der Amyloid-Kaskaden-Hypothese wurden monoklonale Anti-amyloid-beta Antikörper, die Amyloid-Plaques beseitigen können, als möglicher Durchbruch in der Alzheimer-Therapie entwickelt. Ein eben erschienener Cochrane Review zeigt im Vergleich zu Placebo keine oder nur sehr geringe klinisch relevanten Verbesserungen durch solche Antikörper auf Kognition, den Schweregrad der Demenz und funktionelle Fähigkeiten, dagegen aber deutliche Zunahmen von unerwünschten Nebenwirkungen wie Gehirnschwellungen und Mikroblutungen. Laut Cochrane-Team sollte sich künftige Forschung zu krankheitsmodifizierenden Behandlungen der Alzheimer-Krankheit auf andere Behandlungen konzentrieren.
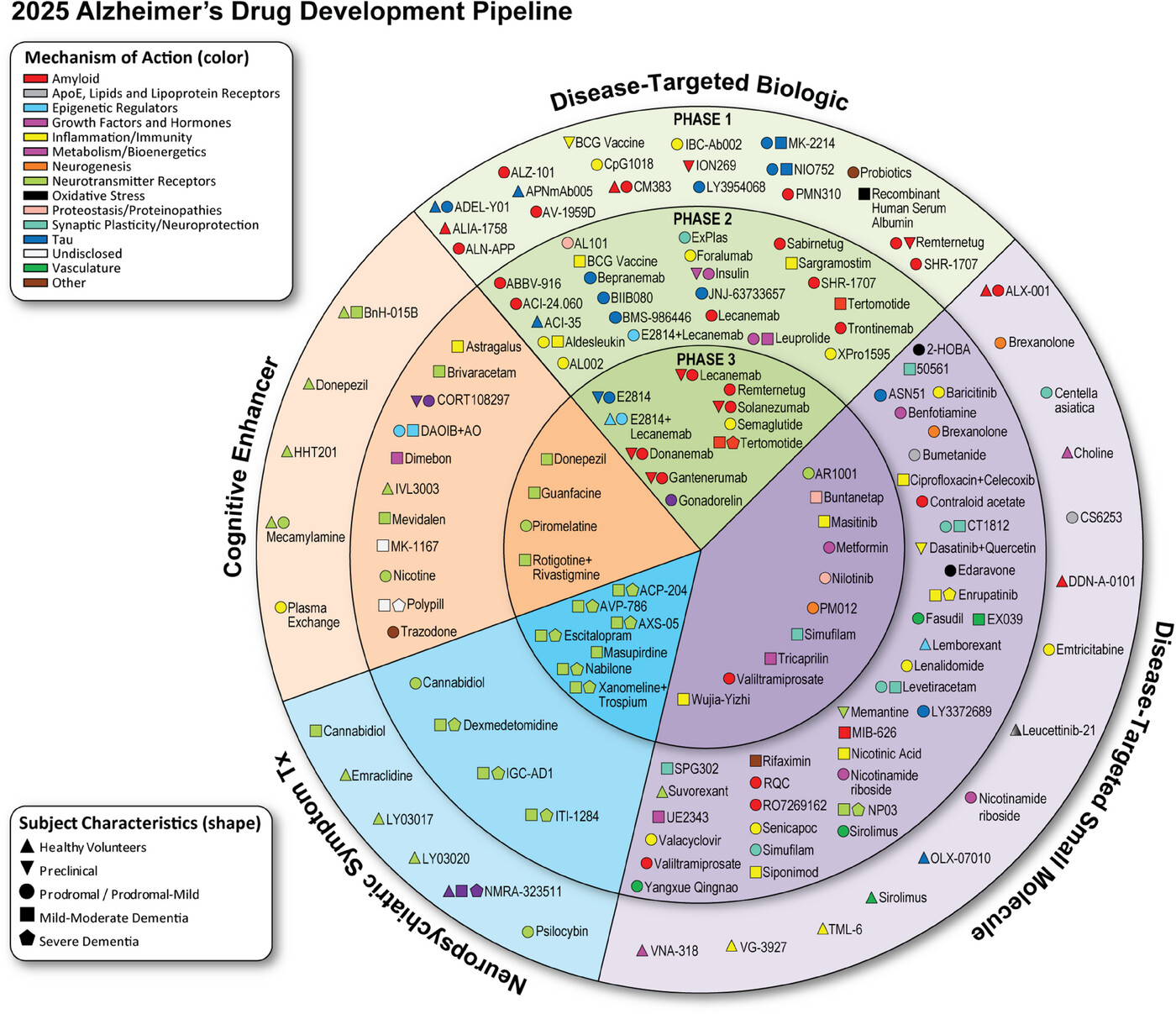
Bereits am Beginn des 20 Jahrhunderts hatte der Arzt Alois Alzheimer extrazellulär abgelagerte Plaques im Gehirn einer dementen Patientin festgestellt; fortan galten diese als Charakteristika, der nach ihm benannten Krankheit. Die Analyse solcher Plaques erfolgte erst in den 1980er Jahren und zeigte als Hauptbestandteil aggregierte neurotoxische Ketten aus dem etwa 40 Aminosäuren langen β-Amyloid Peptid. Diese Aggregate wurden von vielen über lange Zeit als wesentlicher Treiber der Alzheimer Pathologie gesehen (Amyloid-Kaskaden-Hypothese), dementsprechend waren seit mehr als 30 Jahren Hemmung der Bildung von β-Amyloid-Aggregaten und/oder deren Auflösung besonders wichtige Strategien in Forschung und Entwicklung von Alzheimer-Therapeutika. Daneben wurden in insgesamt 4139 klinischen Versuchen weitere Ansatzpunkte (therapeutische Targets) untersucht - bislang ohne einen tatsächlichen Durchbruch zu erzielen. Eine aktuelle Veröffentlichung gibt eine Übersicht der derzeitigen (Stichtag 1.1.2025) in klinischer Entwicklung befindlichen Therapeutika [1]. Abbildung. Laut der kuratierten Datenbank von Alzforum https://www.alzforum.org/therapeutics gibt es 2026 insgesamt 357 unterschiedliche Target-Typen, wobei sich 92 davon auf β-Amyloid beziehen.
|
Abbildung. Therapeutika zur Behandlung der Alzheimer-Krankheit in klinischen Studien (am Indexdatum 1. Januar 2025 laut clinicaltrials.gov). Innerer Ring: Therapeutika in Phase-3, mittlerer Ring: Therapeutika in Phase 2, äußerer Ring: Therapeutika in Phase-1. Therapeutika in Grünflächen sind Biologika; jene in violetten Bereichen sind kleine Moleküle; in orangefarbenen Bereichen sind es Stoffe, die eine kognitive Verbesserung anstreben, in den blauen Abschnitten Stoffe, die sich auf auf verhaltensbezogene und neuropsychiatrische Symptome richten. (Quelle: Abbildung 1 in Cummings et al, 2025; [1].https://doi.org/10.1002/trc2.70098 Lizenz: cc-by-nc-nd.) |
Die Amyloid-Kaskaden-Hypothese ist allerdings ins Wanken geraten, als rasch zunehmende Gehirn-Scans (PET-Scans) in allen Bevölkerungsschichten eine schlechte Korrelation zwischen Amyloid-Plaques und kognitiven Fähigkeiten aufzeigte: Einerseits finden sich derartige Ablagerungen auch im Gehirngewebe von geistig gesunden alten Menschen, andererseits führte die Reduktion solcher Plaques bei Patienten mit milder kognitiver Beeinträchtigung zu keiner Verbesserung der kognitiven Fähigkeiten. Die Reduktion/Beseitigung von β-Amyloid aus dem Hirngewebe ist dabei durch verschiedene monoklonale Antikörper durchführbar, die gezielt an β-Amyloid-Formen binden und damit eine Immunreaktion auszulösen, die zum Abbau/zur Entfernung der Plaques führt.
Kein Durchbruch mit Anti-Amyloid Antikörper-Therapien
Die anfangs als Wendepunkt in der Alzheimer Therapie bejubelten, von der FDA kürzlich zugelassenen Antikörper Aducanumab, Lecanemab und zuletzt Donanemab konnten zwar die β-Amyloid-Belastung in den Gehirnen deutlich senken, zeigten jedoch bei der Verbesserung von kognitiven Parametern nur stark limitierte Wirksamkeit. (Aducanumab wurde inzwischen von der Herstellerfirma Biogen vom Markt zurückgezogen. [2]) Lecanemab (von Eisai) und Donanemab (von Eli Lilly) sind seit 2025 auch in der Europäischen Union für die Behandlung leichter kognitiver Beeinträchtigung zugelassen, wobei aber nur ein stark eingeschränkter Patientenkreis in Betracht kommt, dessen Amyloid-Plaque-Belastung nachgewiesen ist und der höchstens eine Kopie des Risikogens ApoE4 besitzen darf.
Der klinische Nutzen der Antikörper Therapie ist begrenzt: es ist keine Heilung zu erwarten, keine Umkehr der Erkrankung, nur eine vielleicht geringfügige Verlangsamung - entsprechend einem Unterschied von 0,45 Punkten auf einer 18-Punkte-Skala, mit der kognitive Fähigkeiten wie Orientierung, Sprachvermögen oder Erinnerungsfähigkeit gemessen werden. Als Negativa sind neben dem hohen Risiko für Gehirnschwellungen (ARIA-E) und Gehirnblutungen (ARIA-H) - in klinischen Studien mit Lecanemab waren bis zu 20 % der Patienten betroffen, mit Donanemab bis zu 30 % - auch die sehr hohen Therapiekosten zu erwähnen: für die Antikörper allein sind bis rund 25 000 € jährlich zu rechnen, dazu kommen die laufenden Kosten für Infusionen, aufwändige Diagnostik (Liquor-Analytik, PET-Scans) und engmaschiges MRT-Monitoring.
Auf Basis der Studiendaten hat nun der Gemeinsame Bundesausschuss in Deutschland (als Grundlage für die Preisverhandlungen zwischen Krankenkassen und Hersteller) festgestellt, dass weder für Lecanemab noch für Donanemab ein Zusatznutzen im Vergleich zur bisherigen Standardtherapie (mit Inhibitoren der Cholinesterase) belegt ist.
Eine eben von der Cochrane Collaboration erschienene systematische Übersichtsarbeit fasst den Wissensstand zu den Anti-Amyloid Antikörpern zusammen, bewertet die Belastbarkeit der klinischen Studienergebnisse nach den strengen Kriterien der weltweit als Goldstandard anerkannten Methodik von Cochrane und kommt zu einem wenig optimistischen Schluss [3]:
Der Cochrane Review
Die Autoren des Cochrane Reviews haben das Ziel ihrer Untersuchung klar umrissen:„Sind Medikamente (anti-amyloide monoklonale Antikörper), die die Ansammlung abnormaler Proteine im Gehirn reduzieren, eine wirksame Behandlung für Menschen mit leichter kognitiver Beeinträchtigung oder leichter Demenz infolge der Alzheimer-Krankheit, und verursachen sie unerwünschte Effekte?“ [3]
Insgesamt haben die Forscher 17 randomisierte kontrollierte klinische Studien mit 20342 Teilnehmern (Durchschnittsalter 70 -74 Jahre) analysiert, deren Dauer der leichten kognitiven Beeinträchtigung/leichten Demenz zwischen 17 und 52 Monaten lag. In den Studien wurden sieben verschiedene Anti-Amyloid monoklonale Antikörper bewertet, wobei in acht Studien drei Antikörper der ersten Generation untersucht wurden, die sich gegen das monomere β-Amyloidpeptid richteten (Solanezumab, Bapineuzumab und Crenezumab) und wegen klinischer Unwirksamkeit aufgegeben worden waren. In neun klinischen Studien wurden vier gegen aggregiertes β-Amyloid gerichtete Antikörper der zweiten Generation (Aducanumab, Lecanemab, Donanemab und Gantenerumab) untersucht.
Achtzehn Monate nach Studienbeginn lauten die Kernaussagen der Cochrane Studie [3]:
- Bei Menschen mit leichten Gedächtnis- und Denkproblemen (leichte kognitive Beeinträchtigung)/leichter Demenz infolge der Alzheimer-Krankheit führen anti-amyloide monoklonale Antikörper, die potenziell schädliche Ansammlungen von Amyloidproteinen im Gehirn angreifen und entfernen, im Vergleich zu Placebo wahrscheinlich zu geringem bis keinem Unterschied im Rückgang der Gedächtnisfunktion und Denkfähigkeit oder der Schwere der Demenzsymptome. Wahrscheinlich gibt es auch wenig oder gar keinen Unterschied in der Fähigkeit alltägliche Aktivitäten zu managen.
- Anti-amyloide monoklonale Antikörper verursachen wahrscheinlich mehr Gehirnschwellungen und winzige (Mikro-)Blutungen als Placebo. Sie erhöhen aber keine anderen schwerwiegenden Nebenwirkungen oder Todesfälle im Vergleich zu Placebo.
Fazit
Die erfolgreiche Entfernung von Amyloid-Proteinen aus dem Gehirn scheint bei Menschen mit milder kognitiver Beeinträchtigung oder leichter Demenz aufgrund der Alzheimer-Krankheit nicht mit klinisch relevanten Verbesserungen verbunden zu sein.
Das Cochrane-Team empfiehlt: Künftige Forschung zu krankheitsmodifizierenden Behandlungen der Alzheimer-Krankheit sollte sich auf andere Behandlungen konzentrieren.
[1] Cummings JL, Zhou Y, Lee G, et al. Alzheimer's disease drug development pipeline: 2025. Alzheimer's Dement. 2025;11:e70098. https://doi.org/10.1002/trc2.70098
[2] Inge Schuster, 05.02.2024: Alzheimer-Therapie: Biogen gibt seinen umstrittenen Anti-Amyloid-Antikörper Aduhelm auf
[3]Nonino F et al., (16.04.2026): Amyloid-beta-targeting monoclonal antibodies for people with mild cognitive impairment or mild dementia due to Alzheimer’s disease. Cochrane Database of Systematic Reviews 2026, Issue 4. Art. No.: CD016297. DOI: 10.1002/14651858.CD016297
Die Alzheimer-Erkrankung im ScienceBlog
Inge Schuster, 08.01.2026: Mens sana in corpore sano - eine multimodale, personalisierte Strategie gegen Demenz zeigt Erfolg.
Inge Schuster, 14.08.2022: Alzheimer-Forschung - richtungsweisende Studien dürften gefälscht sein
Irina Dudanova, 23.09.2021: Wie Eiweißablagerungen das Gehirn verändern
Francis S. Collins, 14.02.2019: Schlaflosigkeit fördert die Ausbreitung von toxischem Alzheimer-Protein
Inge Schuster, 24.06.2016: Ein Dach mit 36 Löchern abdichten - vorsichtiger Optimismus in der Alzheimertherapie
Francis S. Collins, 27.05.2016: Die Alzheimerkrankheit: Tau-Protein zur frühen Prognose des Gedächtnisverlusts
Gottfried Schatz, 03-07.2015: Die bedrohliche Alzheimerkrankheit — Abschied vom Ich
- Printer-friendly version
- Log in to post comments