Auf dem Weg zu einem antiviralen Breitband-Wirkstoff
Auf dem Weg zu einem antiviralen Breitband-WirkstoffFr.21.11.2025 — Redaktion

![]() Virale Pandemien sind eine Bedrohung für die globale Gesundheit. Anders als bei bakteriellen Infektionen fehlen Breitband-Wirkstoffe, die ein schnelles Reagieren auf neu auftretende, gefährliche Viren ermöglichen würden. Proteine auf der Virusoberfläche sind als Zielstrukturen für die Entwicklung von Breitband-antiviralen Stoffen ungeeignet, da sie zu unterschiedlich sind und sich überdies zu schnell verändern. Eine neue Studie zeigt eine andere Strategie: Kleine synthetische Moleküle (SCRs), die an Kohlenhydrate auf Virusoberflächen binden, konnten Infektionen von Epithelzellen durch unterschiedliche Arten von Hochrisiko-Viren blockieren. Die Wirksamkeit derartiger Verbindungen konnte in vivo an einem Tiermodell bestätigt werden. Diese Ergebnisse lassen es möglich erscheinen, ein antivirales Breitbandmedikament zur Bekämpfung schwerer Virusinfektionen zu entwickeln.*
Virale Pandemien sind eine Bedrohung für die globale Gesundheit. Anders als bei bakteriellen Infektionen fehlen Breitband-Wirkstoffe, die ein schnelles Reagieren auf neu auftretende, gefährliche Viren ermöglichen würden. Proteine auf der Virusoberfläche sind als Zielstrukturen für die Entwicklung von Breitband-antiviralen Stoffen ungeeignet, da sie zu unterschiedlich sind und sich überdies zu schnell verändern. Eine neue Studie zeigt eine andere Strategie: Kleine synthetische Moleküle (SCRs), die an Kohlenhydrate auf Virusoberflächen binden, konnten Infektionen von Epithelzellen durch unterschiedliche Arten von Hochrisiko-Viren blockieren. Die Wirksamkeit derartiger Verbindungen konnte in vivo an einem Tiermodell bestätigt werden. Diese Ergebnisse lassen es möglich erscheinen, ein antivirales Breitbandmedikament zur Bekämpfung schwerer Virusinfektionen zu entwickeln.*
Breitbandantibiotika sind in der Lage ein weites Spektrum von Bakterien zu bekämpfen, die Infektionen in verschiedenen Körperregionen verursachen. Die Verbindungen wirken, indem sie essentielle Zielstrukturen angreifen, die vielen verschiedenen infektiösen Bakterien gemeinsam sind. Bislang gibt es jedoch keinen vergleichbaren, für die Anwendung am Menschen zugelassenen Breitband-Wirkstoff gegen Viren.
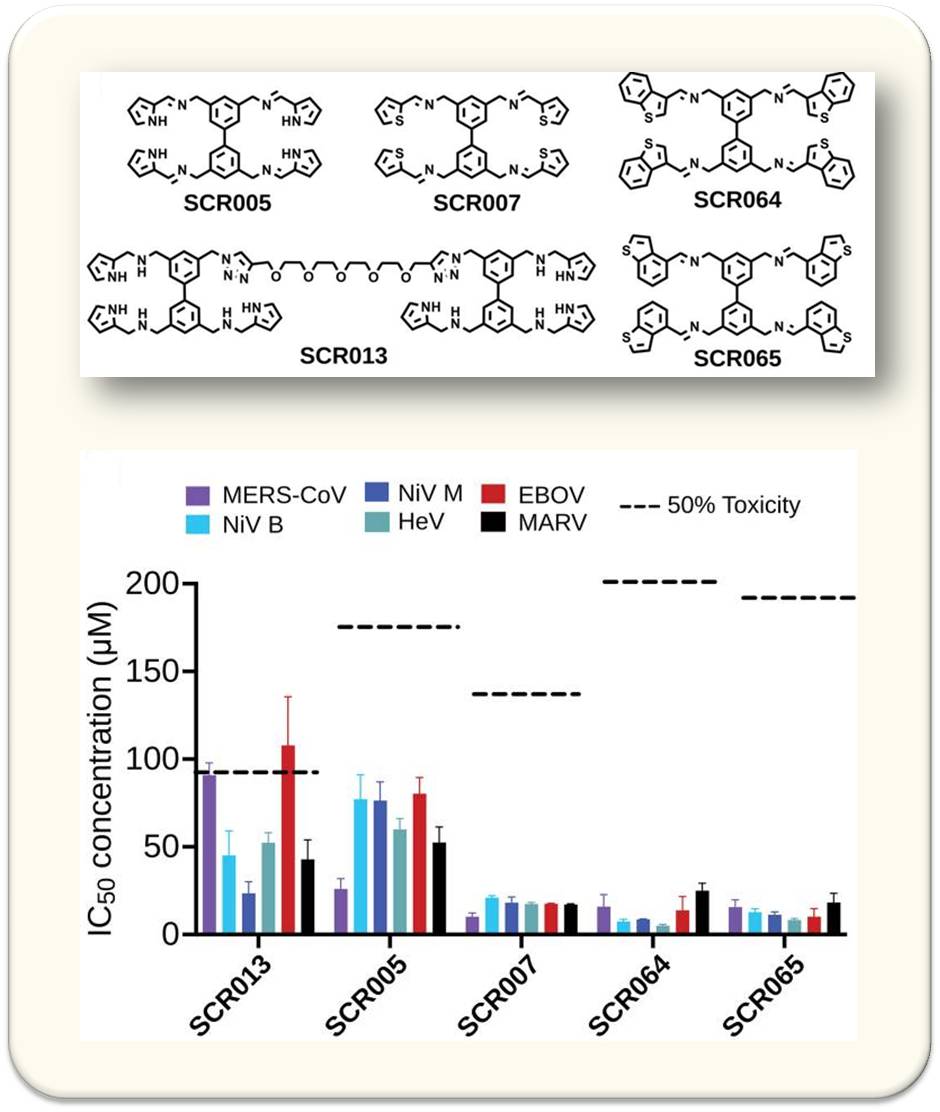
| Abbildung 1: SRCs können das Eindringen unterschiedlicher Viren (SARS-CoV-2, SARS-CoV-1, MERS-CoV, Nipah-, Hendra-, Ebola- und Marburg-Viren) in Zellkulturen blockieren. Oben: Chemische Strukturen von SCRs mit breitem antiviralen Wirkungsspektrum, SRC013 ist als inaktive Kontrollverbindung angeführt. Unten: Infektionswerte (IC50) und Toxizität in Epithelzellen (Vero E-6), die mit SCRs (10 µM) vorbehandelt und dann mit Pseudoviren infiziert wurden. (Bild von der Redaktion modifiziert eingefügt aus: Ezzatpour S., et al.,2025, DOI: 10.1126/sciadv.ady3554; Lizenz cc-by-nc.) |
Dass es so schwierig ist ein antivirales Breitbandmedikament zu entwickeln, liegt darin begründet, dass die auf der Oberfläche von Viren lokalisierten Proteine sehr unterschiedlich sind, sich überdies zumeist rasch verändern und daher als Zielstrukturen für breit wirkende antivirale Stoffe nicht geeignet sind. Daher sind die derzeitigen antiviralen Arzneimittel nur eingeschränkt wirksam und lediglich gegen wenige, sehr spezifische Virusinfektionen von Nutzen.
In einer neuen Studie haben Forscher unter der Leitung von Adam Braunschweig von der City University of New York und Hector Aguilar-Carreno von der University of California, Los Angeles, die Idee von der Entwicklung eines Breitband-Antivirenmittels experimentell untersucht. Ihr Fokus lag dabei auf kleinen synthetischen Molekülen, sogenannten Kohlenhydratrezeptoren (SCRs), die Kohlenhydrate binden. Viele Viren, darunter auch solche, die schwere Erkrankungen und zukünftige Pandemien auslösen können, tragen Kohlenhydrate, sogenannte Glykane, auf ihrer Oberfläche.
Bereits frühere Studien hatten darauf hingewiesen, dass SCRs Kohlenhydrate auf bestimmten Viren binden können. Sie könnten daher als aussichtsreiche antivirale Medikamente betrachtet werden.
Die Ergebnisse der neuen Studie wurden am 27. August 2025 in Science Advances veröffentlicht [Ezzatpour S, et al., 2025].
Untersuchungen an Zellkulturen
Um zu prüfen, ob derartige Substanzen gegen ein breiteres Spektrum von Viren wirken könnten, haben die Forscher ein Set von 57 verschiedenen SCRs gegen sechs Hochrisiko-Viren aus drei verschiedenen Virusfamilien geprüft. Dazu gehörten SARS-CoV-1 und -2, MERS-CoV, Nipah-, Hendra- und Ebola-Viren. Abbildung 1.
Dabei stellten die Forscher fest, dass mehrere der SCRs das untersuchte Zellmodell vor einer Infektion mit allen sechs Virenarten schützten. Vier der SCRs erwiesen sich als besonders vielversprechend für die Verhinderung aller getesteten Virusinfektionen.
| Abbildung 2: SCR005 und SCR007 verringern die Morbidität und Mortalität im hACE2-Mausmodell der SARS-CoV-2-Infektion bei minimaler Toxizität. Oben: Die Versuchsführung. Mäuse (n = 8 -10 pro Behandlungsgruppe) wurden nach Infektion mit SCRs behandelt und die Gewichtsänderung, Überlebenswahrscheinlichkeit und Virenbelastung in Lungen-und Hirngewebe im Vergleich zur Kontrollgruppe bestimmt. 2. Reihe: Gewichtsänderung. 3.Reihe: Überlebenswahrscheinlichkeit. Ganz unten: Viruslast in Lunge und Hirn nach 14 Tagen. (Bild von der Redaktion modifiziert und eingefügt aus: Ezzatpour S., et al.,2025, DOI: 10.1126/sciadv.ady3554; Lizenz cc-by-nc.) |
Untersuchungen am Tiermodell
Auf der Grundlage der an Zellkulturen erzielten Ergebnisse wurden zwei SCRs, SCR005 und SCR007, für in-vivo-Untersuchungen an einem schweren humanisierten ACE2 (hACE2)-Mäusemodell der SARS-CoV-2-Erkrankung ausgewählt.
Intranasal verabreicht boten die Verbindungen Schutz vor der SARS-CoV-2-Infektion. Mit einem der SCRs - SCR007 - überlebten etwa 90 % der behandelten Mäuse mindestens zwei Wochen, im Vergleich zu keinem einzigen Tier in der Kontrollgruppe.
Die antivirale Substanz wirkte bereits nach einer einzigen Dosis und, was besonders wichtig ist, bei den antiviral wirksamen Konzentrationen ohne jegliche Anzeichen von Toxizität. Abbildung 2.
| Abbildung 3: Wirkungsmechanismus von SRCs, Schematische Darstellung. Durch ihre Bindung an die Glykane von viralen Glykoproteinen, blockieren SRCs deren Bindung an Rezeptoren der Wirtszelle und in Folge die Fusion des Virus mit der Zelle. (Bild von der Redaktion modifiziert und eingefügt aus: Ezzatpour S., et al.,2025, DOI: 10.1126/sciadv.ady3554; Lizenz cc-by-nc.) |
Untersuchungen zum Wirkungsmechanismus
Das Team untersuchte dann mit einem Set aussagekräftiger Methoden den Mechanismus der antiviralen Aktivität.
Die Ergebnisse bestätigten die Annahme, dass SCRs den Lebenszyklus der Viren hemmen, indem sie an die Glykane auf den Glykoproteinen der Virushülle binden. Dies verhindert das Andocken des Virus an Rezeptoren der Wirtszelle und damit die Membranfusion und den Eintritt des Virus in die Zelle. Abbildung 3 zeigt eine vereinfachte schematische Darstellung.
Fazit
Die Ergebnisse legen nahe, dass es möglich ist Breitband-Antivirenmittel zu entwickeln, indem man virale Glykane anstelle von Proteinen als Zielstrukturen angreift. Solche Medikamente könnten nicht nur Infektionen mit bereits existierenden Viren behandeln, sondern auch zur Prävention von Infektionen mit neu auftretenden Viren eingesetzt werden.
Die Forscher planen nun, die Sicherheit und Wirksamkeit von SCRs bei der Prävention von Virusinfektionen und deren Übertragung auf Tiere und Menschen zu prüfen.
„Das ist genau die Art von antiviralem Mittel, die die Welt dringend braucht“, sagt Braunschweig. „Wenn morgen ein neues Virus auftaucht, haben wir derzeit nichts, was wir einsetzen könnten. Diese Verbindungen bieten das Potenzial, eine solche erste Verteidigungslinie zu bilden.“
----------------------------------------------------------------------------------
Ezzatpour S, et al., Broad-spectrum synthetic carbohydrate receptors (SCRs) inhibit viral entry across multiple virus families. Science Advances. 2025 Aug 29;11(35):eady3554. DOI: 10.1126/sciadv.ady3554 Epub 2025 Aug 27. PMID: 40864723.
*Der von Kendall K. Morgan stammende, am 9. September 2025 auf der NIH-Webseite "NIH Research Matters" erschienene Artikel "Progress toward a broad-spectrum antiviral" (https://www.nih.gov/news-events/nih-research-matters/progress-toward-broad-spectrum-antiviral) wurde von der Redaktion übersetzt und durch Untertitel und 3 Abbildungen aus der zitierten Originalarbeit (Ezzatpour S, et al. 2025) ergänzt. Artikel auf der NIH-Webseite sind generell gemeinfrei.