Sind Cannabis-basierte Arzneimittel bei Neuropathien wirksam?
Sind Cannabis-basierte Arzneimittel bei Neuropathien wirksam?Fr, 30.01.2026— Inge Schuster
Die medikamentöse Behandlung von Neuropathien ist derzeit unbefriedigend. Eine Jahrtausende alte Anwendung von Cannabis in der Volksmedizin aber auch neue wissenschaftliche Erkenntnisse weisen auf ein hohes Potential von Cannabis-basierten Arzneimitteln in der Schmerzbekämpfung hin, da diese Stoffe mit dem für die Regulierung des Schmerzempfindens wichtigen Endocannabinoid-System unseres Körpers interagieren und es modulieren. Es gibt auch Schmerzpatienten, die von positiven Erfahrungen mit Cannabis‐basierten Präparaten berichten und Medien greifen solche Berichte häufig auf. Wie allerdings die aktuelle Cochrane-Analyse zeigt, können klinische Studien bis jetzt keine eindeutige Evidenz für eine schmerzlindernde Wirkung dieser Stoffe bei Neuropathien liefern. Die Aussagekraft der meisten klinischen Studien litt jedoch unter qualitativ schlechter Versuchsführung, einer niedrigen Teilnehmerzahl und zu kurzer Versuchsdauer.
Neuropathien...
Der Begriff Neuropathie steht für ein Spektrum von Erkrankungen, die durch Schädigung der peripheren Nerven (d.i. Nerven außerhalb von Gehirn und Rückenmark) hervorgerufen werden. Deren Symptome umfassen Störungen der sensorischen Nerven (Kribbeln, Schmerzen, Taubheitsgefühle), der motorischen Nerven (Krämpfe, Muskelschwäche bis -atrophie) und der autonomen Nerven, die Verdauung, Atmung, Herztätigkeit steuern. Man kennt mehr als 200 Ursachen, die Neuropathien auslösen können. Neben mechanischen Schädigungen sind dies vor allem Diabetes, Nährstoffmangel (u.a. Vitamin B12, B1), Nebenwirkungen diverser Medikamente (u.a. neurotoxischer Chemotherapeutika), Umweltgifte und Alkoholabusus. Dazu kommen genetische Faktoren, Autoimmune-Neuropathien (Multiple Sklerose, Lupus), in denen direkt Nerven angegriffen werden können und Infektionen (u.a. Varicella Zoster, HIV).
Weltweit leiden 7 bis 10 % der erwachsenen Bevölkerung an Neuropathien, wobei die Inzidenz mit steigendem Alter zunimmt: Laut einer aktuellen Studie (aus Michigan) sind Im Alter von ≥70 Jahren bis zu 42 % der Menschen betroffen, bei den 85 plus-Jährigen könnten es an die 62 % sein [1].
...und ihre bislang unbefriedigende Behandlung
Die Therapie von Neuropathien zielt in erster Linie darauf ab nach Möglichkeit die Ursache zu beheben, etwa durch Einstellung des Blutzuckerspiegels, Substituierung von Nährstoffen oder Vermeidung toxischer Exposition. Allerdings bleibt - insbesondere im hohen Alter - trotz gründlicher Diagnose in bis zu 40 % der Fälle die Ursache von Neuropathien ungeklärt.
Die gängige medikamentöse Behandlung erweist sich bei vielen Patienten als nur mäßig effizient. Dies zeigt die in klinischen Studien ermittelte Responder-Rate - "Number Needed to Treat" (NNT) - auf, das ist die Zahl der Patienten, die behandelt werden müssen, damit einer davon eine Schmerzreduktion von ≥ 50 % hat, die er durch ein Placebo nicht erhalten hätte. Dazu muss angemerkt werden, dass bei der Behandlung von Neuropathien ein signifikanter Placeboeffekt eintritt: Im Mittel berichten rund 21 % der Patienten in Kontrollgruppen ohne Wirkstoff von einer klinisch relevanten Schmerzreduktion, und diese erreicht häufig die gemessene Wirkung des tatsächlichen Medikaments.
Als Erstlinien-Medikamente werden Antikonvulsiva (Gabapentin und Pregabalin (Lyrica)) sowie Antidepressiva wie Duloxetin und Amitriptylin eingesetzt: Die NNT liegt für Gabapentin oder Pregabalin bei 8 bis 10, für Antidepressiva bei 4 bis 6. Zahlreiche unerwünschte Nebenwirkungen - u.a. Verwirrtheit und Sturzgefahr - schränken die Anwendung vor allem bei alten Menschen ein. Der Einsatz von Opioiden wird erst erwogen, wenn die die Erstlinien-Medikamente ungenügend wirken und/oder nicht vertragen werden. Bei all den Risiken von Nebenwirkungen und Abhängigkeit erfährt aber auch hier nur ein kleiner Teil (etwa 14 %) der Behandelten eine Schmerzlinderung von ≥ 50 % [2].
Summa summarum: Systematische Reviews und Metaanalysen qualitativ hochwertiger klinischer Studien zeigen, dass nur eine Minderheit der Patienten ausreichend auf das vorhandene Arsenal an Medikamenten anspricht und dass die meisten davon Dosis-limitierende Nebenwirkungen erfahren. Es besteht also dringender Bedarf für wirksamere und sicherere Arzneimittel zur Behandlung von Neuropathien. Stoffe aus Cannabis oder davon abgeleitete Substanzen könnten diese Anforderungen erfüllen: Seit Urzeiten wird Cannabis weltweit (nicht nur) gegen Schmerzen angewandt und moderne Forschung hat entdeckt, wie isolierte Cannabis-Produkte in die Regulation des Schmerzempfindens unseres Körpers involviert sind.
Cannabis in der Schmerztherapie
Unter dem Begriff Cannabis werden ganz allgemein Produkte subsummiert, die aus Pflanzen der Gattung Hanf (Cannabis sativa) gewonnen werden. Hanf ist seit Jahrtausenden eine Nutzpflanze, von der jeder Teil Verwendung findet: Die Hanffasern zur Herstellung von Textilien, Seilen und Spezialpapier, Hanfsamen als wertvolle Lebens- und Futtermittel, die Blüten und Blätter schließlich als Rauschmittel (getrocknete Blüten und Blätter: Marihuana, Harz der weiblichen Büten: Haschisch) und für medizinische Anwendungen.
Die Anwendung als Heilmittel datiert in China fast 5 000 Jahre zurück; Cannabis wurde u.a. gegen Rheuma, Gicht und Malaria eingesetzt. Im über 3 000 Jahre alten indischen Atharvaveda, das ein Bild der damaligen medizinischen Heilriten gibt, wird Cannabis (Bhang) als eine der fünf heiligsten Pflanzen verehrt und dem Gott Shiva (dem "Herrn des Bhang" - Bhang Raj) zugeordnet. Die Pflanze wurde und wird für rituelle und diverseste medizinische Zwecke genutzt: Vom Mittel gegen Schmerzen (Neuralgien, Kopf- und Zahnschmerzen), über die Behandlung von Krampfanfällen, Entzündungen, Infektionen bis hin zum Beruhigungsmittel und appetitanregenden, verdauungsfördernden Mittel [3]. Auf die weltweite Ausbreitung des Hanfs und seiner Verwendungszwecke soll hier nicht eingegangen werden.
In der westlichen Medizin begann Hanf erst im 19. Jahrhundert eine Rolle zu spielen und führte vorerst zu einem Hype. Da sich aber mit den damals aus unterschiedlichen Chargen von Pflanzenmaterial mit unterschiedlichen Wirkstoffgemischen produzierten Extrakten und Tinkturen keine konsistenten Ergebnisse erzielen ließen, sank das Interesse bald wieder. Es erwachte erst wieder in der zweiten Hälfte des 20. Jahrhunderts, als analytische Methoden es erlaubten die Inhaltstoffe von Cannabis in reiner Form zu isolieren und charakterisieren. Damit war die Grundlage für Untersuchungen zu möglichen Wirkorten und Wirkungsmechanismen dieser Substanzen im Organismus geschaffen und klinische Studien zu Wirkung und Nebenwirkungen konnten nun unter standardisierten Bedingungen begonnen werden.
Isolierung von Cannabinoiden....
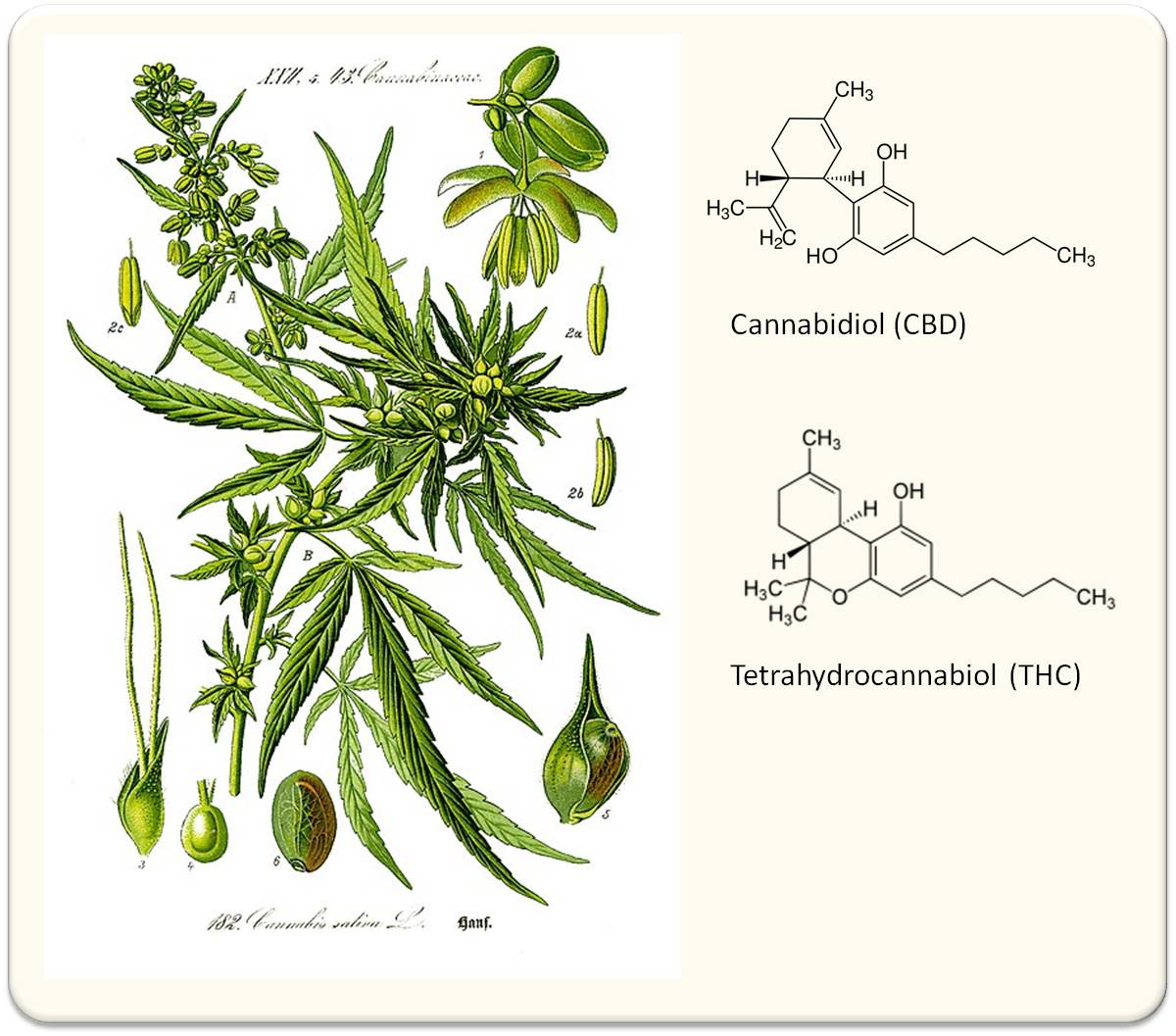
Die Cannabis-Pflanzen enthalten sehr hohe Mengen an sogenannten Cannabinoiden - fast 25 % aller darin identifizierten chemischen Stoffe (u.a eine Fülle an Flavonoiden und Terpenen) werden dieser großen Gruppe an pharmakologisch wirksamen Substanzen zugerechnet und der therapeutische Einsatz beruht (gegenwärtig) im wesentlichen auf dieser Stoffklasse. Von den derzeit mehr als 140 bekannten Strukturen wurden zwei bisher am intensivsten untersucht: Tetrahydocannabinol (Δ9-THC), eine für die euphorisierende, berauschende Wirkung von Cannabis verantwortliche Substanz, die auch schmerzlindernde und anti-emetische Eigenschaften aufweist und Cannabidiol (CBD) eine nicht-psychoaktive Substanz, die angstlösend, krampflösend und entspannend wirkt. Abbildung 1.
|
Abbildung 1. Hanf (Cannabis sativa) Abbildung aus Hermann Adolf Köhler: "Köhlers Medizinal-Pflanzen in naturgetreuen Abbildungen und kurz erläuterndem Texte" 1887 und die beiden pharmakologisch am intensivsten untersuchten Cannabinoide: Cannabidiol (CBD) und Tetrahydrocannabiol (THC). (Bild:gemeinfei aus Wikipedia) |
....Entdeckung des Wirkungsmechanismus...
Untersuchungen mit Hilfe von radioaktiv markiertem CBD und THC haben in den 1990er Jahren zur Entdeckung von zwei Rezeptortypen (nicht nur) im menschlichen Körper geführt: CBD bindet dabei an einen vorwiegend im Immunsystem und peripheren Gewebe lokalisierten Rezeptor (CB2), THC an einen unterschiedlichen, im Gehirn und zentralen Nervensystem lokalisierten Rezeptor (CB1). (Dementsprechend zeigen beide Substanzen deutliche Unterschiede in ihren Wirksamkeits- und Sicherheitsprofilen auf.) In Folge wurden dann natürlich im Körper vorkommende Bindungspartner (Liganden) für diese Rezeptoren identifiziert - sogenannte Endocannabinoide -, deren Bindung Signale zur Freisetzung von Neurotransmittern auslösen. Damit wurde das sogenannte Endocannabinoid-System entdeckt, das eine wesentliche Rolle bei der Regulation von Schmerzempfinden und anderer neurologischer Funktionen (u.a. Schlaf, Appetit, Stress, Gedächtnis) aber auch von Immunabwehr und Entzündungsprozessen spielt.
Mit der Entdeckung des Endocannabinoid-Systems wurden neue Möglichkeiten zur Erforschung und klinischen Untersuchung des therapeutischen Potenzials von Cannabinoiden geschaffen und von diesen abgeleitete Strukturen konnten nun zielgerichtet synthetisiert und entwickelt werden. Das hat in den letzten Jahren zu einem rasanten Anstieg des wissenschaftlichen Interesses geführt: Von insgesamt 40 789 in der medizinischen Datenbank PubMed zum Thema "Cannabis" gelisteten Publikationen sind in den 1990er Jahren 1219 entstanden, 2000 bis 2010 waren es bereits 4032, in der folgende Dekade 12175 und von 2020 bis heute sind es 19516.
Anwendung von Cannabinoiden
Für ein limitiertes Spektrum von Erkrankungen/Zuständen wurden vier auf den Cannabinoiden THC und CBD basierende Präparate bislang als Arzneimittel in zahlreichen Ländern zugelassen:
- Epidyolex (ein hochreines CBD) gegen schwere, seltene Formen von Epilepsie (bei Kindern),
- das Mundspray Sativex (Nabiximols, ein 1:1 Extrakt von THC und CBD) gegen Spastik bei multipler Sklerose,
- Cesamet (Nabilon, ein synthetisches THC-Derivat) gegen Übelkeit, schweres Erbrechen unter Chemotherapie,
- Marinol (Dronabinol, natürliches THC) gegen Übelkeit/Erbrechen und Appetitlosigkeit unter Chemotherapie.
Allerdings werden die THC-enthaltenden Medikamente häufig auch "off-label" bei neuropathischen und anderen Schmerzen verschrieben, das reine CBD-Präparat dagegen bei Schlaf-und Angststörungen. Von der ausgewogenen 1:1 Kombination beider Wirkstoffe erwartet man sich eine Milderung der berauschenden Wirkung und anderen Begleiterscheinungen von THC, therapeutische Synergien bei Neuropathien und insgesamt einen entspannenden Effekt. Bei umfassender ärztlicher Aufklärung ist dieser Einsatz legal.
Klinische Studien
|
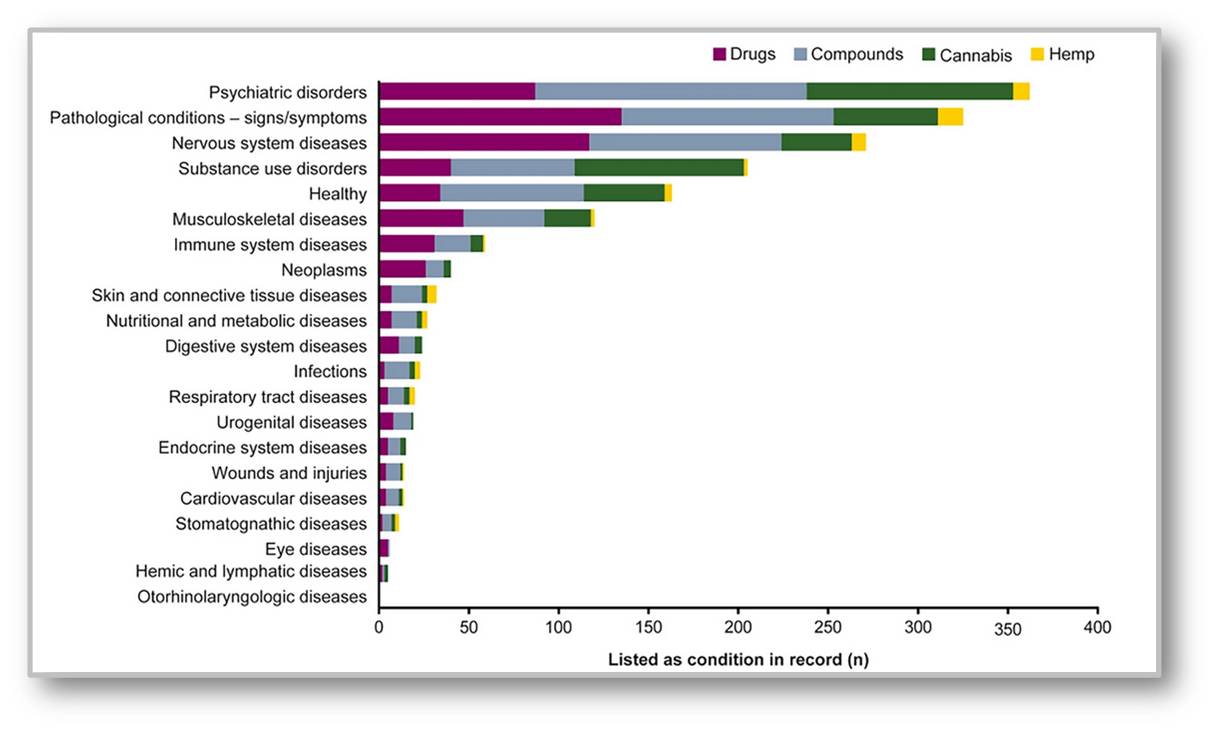
Abbildung 2. Welche klinischen Studien wurden bis jetzt mit welchen Cannabisprodukten und bei welchen Krankheiten/Zuständen durchgeführt? Die Analyse erfasste alle zum Stichtag 1.10.2023 auf ClinicalTrials.gov gelisteten Untersuchungen. Drugs: Registrierte Arzneimittel Epidyolex, Sativex, Cesamet, Marinol . Compounds: Nicht zugelassene Arzneimittel und Extrakte mit definiertem Cannabinoidgehalt.Cannabis: Produkte aus der gesamten Cannabispflanze unabhängig vom Cannabinoidgehalt. Hemp: Haferöl und Haferprodukte ohne definierten Cannabinoidgehalt. (Quelle: Fig.2 in Haney et al., 2026. https://doi.org/10.1007/s40290-025-00591-w-w. Lizenz cc-by- nc.) |
Ebenso wie die gesteigerte Forschung hat auch die Zahl der klinischen Studien enorm zugenommen: Aktuell listet die Plattform ClinicalTrials.gov zum Thema "Cannabis" insgesamt 947 Studien, von denen 241 in der fortgeschrittenen Phase 2 und 93 bereits in Phase 3 sind. 339 dieser Studien wurden zwischen 2010 und 2020 begonnen, 436 in der Zeit zwischen 2020 und heute. Eine kürzlich erschienene Studie hat 825 auf dieser Plattform gelistete Studien in Hinblick auf untersuchte Krankheiten/Zustände und angewandte Cannabis-Produkte analysiert {4]. Abbildung 2 fasst die Ergebnisse zusammen.
Cannabis-Produkte wurden in einer sehr breiten Palette von Krankheiten/Zuständen untersucht; die meisten Studien liefen über neurologische Aspekte:
- psychische Störungen/Erkrankungen (Schizophrenie, Angststörungen, traumatische Belastungsstörungen),
- Begleiterscheinungen von Krankheiten oder unspezifische Zustände (Schmerz, Neuropathien, Übelkeit, Schlafstörungen, Appetitlosigkeit),
- Erkrankungen des Nervensystems (Epilepsie, Multiple Sklerose).
Der überwiegende Teil der Versuche lief mit den oben erwähnten, bereits registrierten Medikamenten ("drugs"; 32,7%) und 14 nicht-registrierten Cannabinoiden oder Extrakten mit definiertem Cannabinoid-Gehalt ("compounds"; 43,6 %), weiters mit Produkten aus ganzen Pflanzenteilen ("Cannabis"; 20,3 %), sowie mit Hanfprodukten wie Hanföl oder Extrakten mit undefiniertem Cannabinoid-Gehalt ("Hemp": 3,5 %). Über 90 % der Versuche waren Interventionsstudien, dh. eine Gruppe von mit Substanz behandelten Patienten wurde mit einer Kontrollgruppe verglichen, und rund 80 % der Kohorten waren randomisiert.
Eine Besonderheit: Im Gegensatz zu üblichen klinischen Studien, die zum weitaus überwiegenden Teil von Pharmafirmen durchgeführt werden, spielten diese bei den Cannabinoid-Untersuchungen eine untergeordnete Rolle; 70,5 % der Studien wurden von akademischen Einrichtungen/Spitälern durchgeführt, 26,8 % von Pharmaunternehmen, 2,5 % von staatlichen Einrichtungen. Dies erklärt wohl auch die niedrige Teilnehmerzahl (weniger als 50 Personen) und kurze Versuchsdauer der meisten Untersuchungen: Ausgedehntere klinische Studien - vor allem in Phase 2 und 3 - sind sehr teuer und mit dem limitierten Budget akademischer Institutionen kaum vereinbar.
Gibt es Evidenz für die Wirksamkeit von Cannabis-basierten Arzneimitteln bei Neuropathien?
Randomisierte kontrollierte klinische Studien werden zur Bewertung von Wirksamkeiten herangezogen und Cochrane-Reviews sind der Goldstandard in der Analyse solcher Studien. Bereits 2018 war ein Cochrane Review auf Basis von 16 Studien mit insgesamt 1750 Teilnehmern zu dem Schluss gelangt:"Es fehlt an qualitativ guter Evidenz, dass von Cannabis abgeleitete Produkte bei chronischen neuropathischen Schmerzen wirksam sind." [5].
Cochrane Review (19.1.2026):
Ein aktualisierter Cochrane Review wurde vergangene Woche veröffentlicht [6]. Mit den seit 2018 neu hinzugekommenen Studien umfasst die Analyse nun 21 randomisierte Placebo-kontrollierte Studien mit insgesamt 2187 Teilnehmern. In sieben Studien wurden Medikamente mit einem hohen Anteil an THC verabreicht, in neun Studien Medikamente mit einem ausgewogenen Verhältnis von THC und CBD und in fünf Studien Medikamente mit einem hohen Anteil an CBD. Nur vier Studien erfüllten die von der EU-Arzneimittelbehörde EMA empfohlene Laufzeit von mindestens 12 Wochen.
Das Ergebnis ist auch dieses Mal enttäuschend: Es gibt weder für die THC-dominierten, noch für die THC/CBD-ausgewogenen oder die CBD-dominierten Medikamente eine qualitativ gute Evidenz für eine Schmerzlinderung von mindestens 50 %. Die THC-dominierten Präparate aber auch die Kombinationspräparate dürften zudem eine Reihe unerwünschter Nebenwirkungen wie Gleichgewichtsstörungen, Schwindel, Konzentrationsstörungen und Schläfrigkeit mit sich bringen.
Die Schlussfolgerung der Autoren [6]:
- Da es an belastbarer Evidenz fehlt, ist unklar, ob Cannabis‐basierte Medikamente mehr nutzen oder schaden.
- Um den möglichen Nutzen und mögliche Schäden Cannabis‐basierter Medikamente verlässlich beurteilen zu können, braucht es größere, methodisch gut durchgeführte Studien. Diese sollten auch Menschen mit schweren körperlichen Begleiterkrankungen (z. B. Herz‐ oder Nierenerkrankungen) sowie mit psychischen Erkrankungen einschließen.
Übersictsartikel in JAMA (26.11.2025)
Kurz vor dem Cochrane Review ist ein Übersichtsartikel in der Fachzeitschrift JAMA erschienen, der den gegenwärtigen Kenntnisstand zur therapeutischen Anwendung von Cannabinoiden zusammenfasst [7]:
- Metaanalysen für die bis jetzt registrierten Cannabinoide zeigen in den vorgesehenen Indikationen minimale bis moderate Wirkungen.
- Für weitere, häufig propagierte Indikationen wie akuter/chronischer Schmerz, Neuropathien, psychische Erkrankungen, Demenz, Depressionen, Angststörungen ist die Evidenz für eine Verwendung von Cannabis oder Cannabinoiden nicht ausreichend.
- Dazu kommen zahlreiche Risiken von Cannabis-Produkten, die von Psychosen bis zu erhöhter Inzidenz von Herz-Kreislauferkrankungen und neurokognitiven Beeinträchtigungen reichen.
Die Schlussfolgerung der Autoren [7]:
"Die Evidenz für die Verwendung von Cannabis oder Cannabinoiden ist bei den meisten medizinischen Indikationen unzureichend. Ärzte sollten die Vorteile gegen die Risiken abwägen, wenn sie mit Patienten informierte Gespräche über die Verwendung von Cannabis oder Cannabinoiden führen."[7]
[1] Wu YHA et al., Prevalence of Peripheral Neuropathy Among Very Old Adults: Evidence From the Michigan Neuropathy Screening Instrument. J Am Geriatr Soc. 2025 Nov;73(11):3530-3538. 10.1111/jgs.70041.. Epub 2025 Sep 1.
[2] Xavier Moisset, Neuropathic pain: Evidence based recommendations. La Presse Médicale.Volume 53, Issue 2, June 2024, 104232. https://doi.org/10.1016/j.lpm.2024.104232.
[3] Antonio Waldo Zuardi, History of cannabis as a medicine: a review. Rev Bras Psiquiatr. 2006;28(2):153-7
[4] Haney, M., Cooper, Z.D., VanLaanen, H. et al. Studies of Cannabinoid-Based Products in ClinicalTrials.gov: A Scoping Review. Pharm Med 40, 33–43 (2026). https://doi.org/10.1007/s40290-025-00591-w.
[5] Mücke M, Phillips T, Radbruch L, Petzke F, Häuser W. Cannabis‐based medicines for chronic neuropathic pain in adults. Cochrane Database of Systematic Reviews 2018, Issue 3. Art. No.: CD012182. https://doi.org/10.1002/14651858.CD012182.pub2
[6] Ateş G, Welsch P, Klose P, Phillips T, Lambers B, Häuser W, Radbruch L. Cannabis‐based medicines for chronic neuropathic pain in adults. Cochrane Database of Systematic Reviews 2026, Issue 1. Art. No.: CD012182. https://doi.org/10.1002/14651858.CD012182.pub3.
[7] Hsu M, Shah A, Jordan A, Gold MS, Hill KP. Therapeutic Use of Cannabis and Cannabinoids: A Review. JAMA. 2026 Jan 27;335(4):345-359. DOI: 10.1001/jama.2025.19433.