Die biomimetische künstliche Nase – wie weit sind wir? Teil 3: Konstruktion einer biomimetischen Nase
Die biomimetische künstliche Nase – wie weit sind wir? Teil 3: Konstruktion einer biomimetischen NaseFr, 09.02.2012- 04:20 — Wolfgang Knoll
![]() Im Teil 2 „Aufbau und Funktion physiologischer Geruchssensoren“ (Science-Blog, 26. Jänner 2012) wurde ein Bild der biologischen Vorgänge bei der Geruchsempfindung beschrieben, vor allem die molekularen Prozesse der Erkennung und Bindung der Geruchsstoffe und Pheromone, sowie die nachgeschalteten enzymatischen Verstärkungskaskaden. Auf dieser Basis definiert sich der Raum, in dem die Ansätze für eine biomimetische Geruchs- (und Geschmacks-) Sensorik angesiedelt werden müssen.
Im Teil 2 „Aufbau und Funktion physiologischer Geruchssensoren“ (Science-Blog, 26. Jänner 2012) wurde ein Bild der biologischen Vorgänge bei der Geruchsempfindung beschrieben, vor allem die molekularen Prozesse der Erkennung und Bindung der Geruchsstoffe und Pheromone, sowie die nachgeschalteten enzymatischen Verstärkungskaskaden. Auf dieser Basis definiert sich der Raum, in dem die Ansätze für eine biomimetische Geruchs- (und Geschmacks-) Sensorik angesiedelt werden müssen.
Komponenten einer biomimetischen Nase
Zentrales Element ist offensichtlich eine Membran nach dem Vorbild der natürlichen Lipid Doppelschicht (lipid bilayer) der Zellmembran. Diese Membran muß
i) für technische Anwendungen robust sein,
ii) durch eine Reihe unterschiedlicher funktioneller Komponenten, also mittels Einbau von Membranproteinen für die verschiedenen Schritte im Reaktionsablauf bei der Geruchserkennung (olfaktorische Sensorik) fit gemacht werden und
iii) es letztendlich erlauben, bei Bindung eines Duftstoffes ein entsprechend ausgelöstes, elektrisches Signal zu detektieren. Auch wenn im Moment kein Labor der Welt in der Lage ist, auch nur annähernd die Komplexität der Riechzellen- Membran, sei es auch nur in der vereinfachten, in Teil 2 (Abb. 4) diskutierten Version, nachzubauen, so sind bereits einzelne Schritte der Reaktionskaskade realisiert worden. Auf Basis dieser im Folgenden beschriebenen Ergebnisse erscheint es durchaus vorstellbar, dass wir das Ziel einer künstlichen biomimetischen Nase erreichen können.
Die einfachste biomimetische Architektur, die als zentrales Matrix-Element die Reaktionskette bei der Geruchsrezeption nachzustellen erlaubt, ist eine immobilisierte Lipid Doppelschicht Membran („tethered Bilayer Lipid Membran“: tBLM). Eine der verschiedenen, in der Literatur beschriebenen Ausführungsformen ist eine auf einem Polymer-Kissen, einem weichen Hydrogel, immobilisierte Lipid-Doppelschicht, welche durch den Einbau eines Geruchsrezeptors für die Erkennung und Bindung eines Geruchsstoffes funktionalisiert wurde (Abbildung 5). (Geruchsrezeptoren sind GPCR-Proteine, die mit 7 durch die Membran reichenden helikalen Peptidsequenzen charakterisiert sind. Beschreibung: ScienceBlog, 5. Jänner 2012, „Wie wir die Welt um uns herum wahrnehmen“)
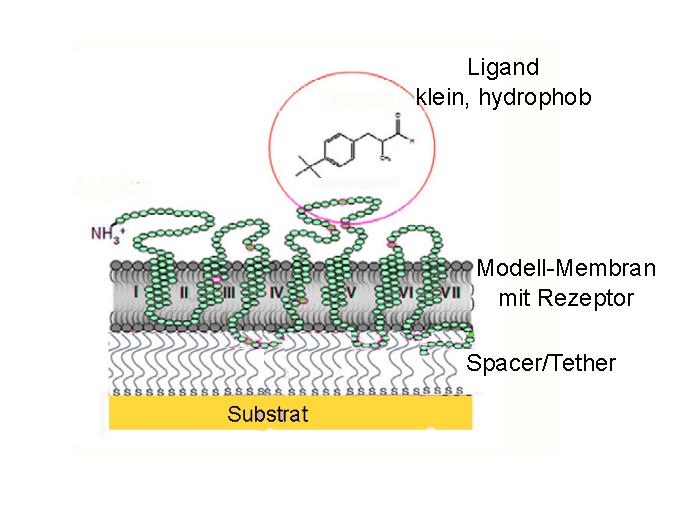 Abbildung 5: Auf einem festen Substrat, welches auch als Transducer/ Elektrode fungiert, wird über einen Abstandshalter/Verknüpfer (Spacer/Tether) eine sog. tethered Lipid Bilayer Membrane (tBLM) immobilisiert und durch den Einbau eines Geruchsrezeptors funktionalisiert, was die Bindung eines Duftstoffes, hier: Lilial, zu detektieren erlauben muß.
Abbildung 5: Auf einem festen Substrat, welches auch als Transducer/ Elektrode fungiert, wird über einen Abstandshalter/Verknüpfer (Spacer/Tether) eine sog. tethered Lipid Bilayer Membrane (tBLM) immobilisiert und durch den Einbau eines Geruchsrezeptors funktionalisiert, was die Bindung eines Duftstoffes, hier: Lilial, zu detektieren erlauben muß.
Diese Grund-Architektur kann tatsächlich sehr einfach, reproduzierbar und robust hergestellt werden (Abbildung 6): Ein fester Träger, in diesem Fall ein mit Gold (Au) beschichtetes Glassubstrat, wird in eine Lösung eines Thiol-Lipid Derivats (siehe Glossar) getaucht, was zur spontanen Bildung einer über einen Abstandshalter immobilisierten Lipid-Monoschicht (Lipid-Monolayer) führt. Taucht man nun diesen mit einer Lipid-Monolage beschichteten Träger in eine wässrige Dispersion von Lipid-Vesikeln (kleine geschlossene Lipid-Doppelschicht-Kugeln), kommt es wieder zu einem spontanen Prozess, nämlich der Fusion einiger Vesikel mit der immobilisierten Lipid Monolayer, der zu einer zuverlässigen Präparation der gewünschten tBLMs führt. 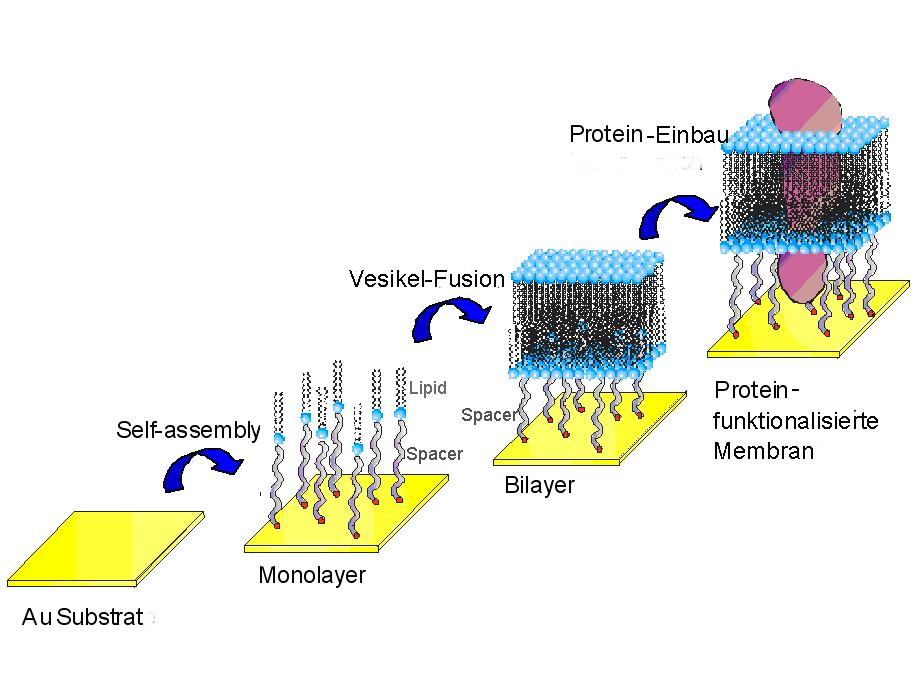
Abbildung 6: Aufbau einer tBLM durch Self-Assembly eines Thiol-Lipid-Derivates, welches spontan zur Bildung einer tethered Lipid-Monoschicht am Gold (Au)-Substrat führt. Diese Monolage wird durch Vesikel Fusion aus einer wässrigen Dispersion zur tethered Lipid-Doppelschicht, einer Festkörper-gestützten Membran erweitert, welche durch den Einbau von Proteinen funktionalisiert werden kann.
Qualitätskriterien der immobilisierten Lipid Doppelschicht Membran
Die erhaltenen Membranen erweisen sich als sehr stabil (in einer Flüssigkeitszelle in wässriger Lösung liegt unser persönlicher Rekord bei einer Stabilität von über 7 Monaten). Wichtige Qualitätskriterien bei der Bewertung ihrer Tauglichkeit für sensorische Anwendungen allgemein, besonders aber für den Einbau und die elektrische Auslesbarkeit von Ionen–Kanälen, sind die Fluidität und die elektrische Dichtigkeit der Membranen.
Fluidität (genauer: die laterale Beweglichkeit der die Membran aufbauenden Lipide): Messungen mit einer aus der Membran-Biophysik bekannten Methode, dem „Fluorescence Recovery after Photobleaching“ (FRAP), zeigten eine fluide Membran an, wenn auch - abhängig von der Dichte an Anker-Lipiden (welche für die Immobilisierung an das Substrat verantwortlich sind) - eine Reduktion der lateralen Beweglichkeit gegenüber der freien lateralen Diffusion der Lipide in einem Vesikel gefunden wurde. Die Fluidität der Membran wurde auch durch Daten mit einem Ionen-Carrier, Valinomycin, bestätigt, dessen molekularer Mechanismus für den Ionentransports über die Membran - als bewegliches Shuttle - eine entsprechende Fluidität der Lipid Matrix voraussetzt.
Elektrische Dichtigkeit (Permeabilität für Ionen). Mindestens ebenso wichtig wie die Beobachtung, dass wir mit unserer Methode eine stabile und fluide Membran aufbauen können, war der Befund, dass diese Festkörper-gestützten Membranen in Hinblick auf die elektrische Dichtigkeit das beste bisher bekannte Modell-Membran System, die Black Lipid Membranes, sogar noch übertreffen. (Man kann spekulieren, dass diese geringe Permeabilität für Ionen direkt mit der Fluidität der Membran korreliert: ein dünner Flüssigkeitsfilm hat per Definition keine Löcher (aber natürlich laterale Dichtefluktuationen…)). Die gefundenen Werte für die elektrische Dichtigkeit der reinen Lipid-Doppelschicht mit einem spezifischen Widerstand besser als 10 Megaohm x cm² erlauben die Beobachtung des Öffnens und Schließens von einzelnen Kanal-Proteinen mit Strom-Inkrementen von 10 pA (s.u.).
Funktionalisieren der immobilisierten Lipid Doppelschicht Membran
Durch den Einbau von Membranproteinen wird eine solche Lipid Matrix für die verschiedenen grundlegenden Untersuchungen im Rahmen biophysikalischer Fragestellungen funktionalisiert und damit auch für praktische Anwendungen in der Bio-Medizin oder eben in der Sensorik fit gemacht. Im Prinzip laufen auch diese Prozesse spontan ab, jedoch gibt es Prozess-bedingte Barrieren. Das manifestiert sich schon bei einfacheren Membran-Proteinen, die im Normalfall aus einer biologischen Membran herausgelöst (solubilisiert) werden müssen, um dann aufgereinigt wieder in die künstliche Membran eingebaut (rekonstituiert) zu werden. Auch wenn man bei diesen Prozessen auf eine jahrzehntelange Erfahrung aus der Membran-Biophysik zurückgreifen kann, ist doch ein Element der Magie oder zumindest eine künstlerische Komponente dabei. Dennoch gelang es im Laufe der Jahre eine ganze Reihe von Proteinen selbst oder in Kooperation mit biologisch arbeitenden Gruppen einzubauen und zu charakterisieren.
Die Quantifizierung der Eigenschaften der Lipid-Protein-Verbundmatrix geht immer dann besonders gut, wenn es sich um elektrogene (elektrische Spannung erzeugende) Prozesse handelt. Neben fast trivialen Experimenten mit Ionen-Carriern, wie z.B. Valinomycin (s.o.), seien hier einige Beispiele von in unserer Gruppe bearbeiteten Systemen angesprochen:
A0A1-ATPase - Membran: in Zusammenarbeit mit Prof. Peter Gräber (Albert-Ludwigs-Universität, Freiburg/Breisgau) konnte gezeigt werden, dass das System in der Lage ist, nach Zugabe von ATP als Energie-Quelle Protonen über die (tethered) Membran zu pumpen. Die enzymatische Aktivität der eingebauten ATPase konnte durch die anschließende elektrochemische Reduktion der transportierten Protonen quantifiziert werden.
Redox-Proteine – Membran: Der Einbau der Cytochrom c Oxidase erlaubte mit Hilfe elektrochemischer Methoden eine äußerst detaillierte Analyse der heterogenen Elektronen-Transfer-Prozesse von der Elektrode (als welche das Gold-beschichtete Substrat eingesetzt werden konnte) zu den vier Redox-Zentren des Proteins (heme a, heme a3, CuA, CuB) durchzuführen, und zwar als Funktion von pH und Temperatur, sowie unter aeroben als auch unter anaeroben Bedingungen. (Cytochrom C Oxidase wurde von den Forschungsgruppen um Prof. Robert B. Gennis, University of Illinois/Urbana und Prof. Shelagh M. Ferguson-Miller, Michigan State University/East Lansing zur Verfügung gestellt.)
Geruchsrezeptor – Membran: Eine Spezialität unserer Gruppe sind spektroskopische Methoden, die es erlauben wichtige Aussagen zur Korrelation von Struktur und Funktion von Membran-integrierten Proteinen zu erarbeiten (die höchst-auflösende sog. surface-enhanced infrared reflection-absorption spectroscopy (SEIRRAS) und die surface-enhanced resonance Raman spectroscopy (SERRS), stationär oder zeitaufgelöst (mit einer Zeitauflösung von besser als 100 µs)). Dies ist vor allem auch bei Systemen und Prozessen, wie z.B. der Bindung eines Geruchsstoffes an einen Membranrezeptor, von Bedeutung, die nicht unmittelbar zu einer elektrogenen Antwort - also dem Transfer von Ladungen über die Membran - führen (welcher elektrochemisch mittels Impedanzspektroskopie beobachtbar wäre). Ein Beispiel ist in Abbildung 7 gezeigt. In Zusammenarbeit mit Prof. Eva Sinner und ihrem Team konnten wir die Bindung des Geruchsstoffes Lilial, einem kleinen hydrophoben Molekül, an seinen Rezeptor, eingebaut in eine tethered Membran verfolgen und quantifizieren (dies durch die Aufnahme der zeitlichen Änderung einiger Banden). 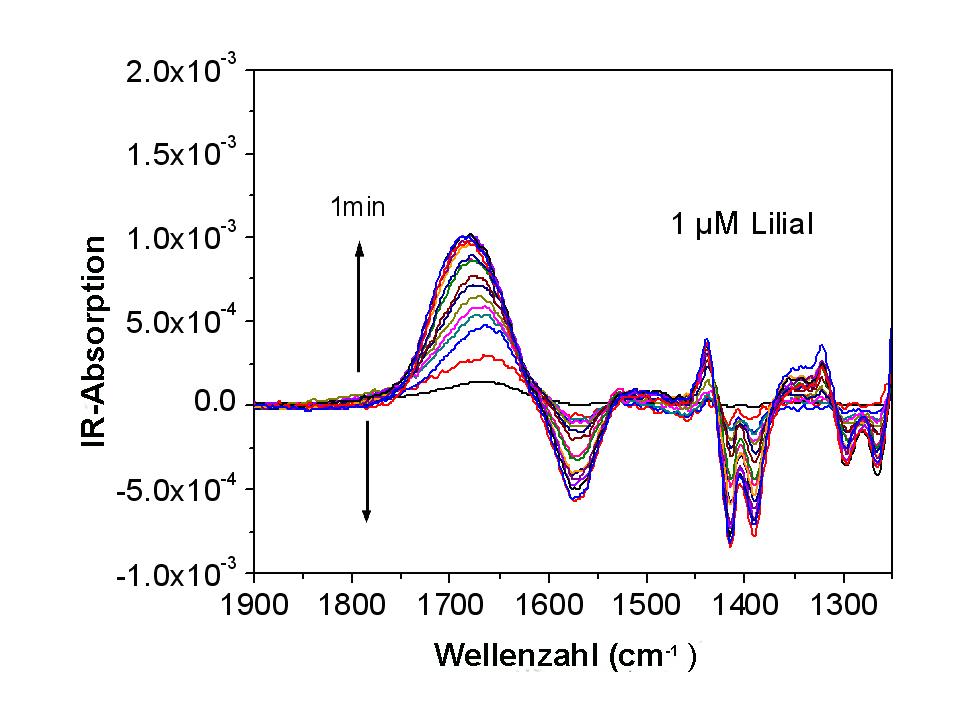 Abbildung 7: Zeitliche Abfolge der Infrarot-Spektren im Spektralbereich der Amide I und Amide II Banden (SEIRRAS Daten), aufgenommen in Abständen von einer Minute nach Zugabe einer 1 µM Lösung des Duftstoffes Lilial zu einer mit einem Geruchsrezeptor (OR5 der Ratte) funktionalisierten tethered membrane (Zusammenarbeit mit Prof. Eva Sinner, Universität für Bodenkultur/Wien, früher MPI für Polymerforschung/Mainz).
Abbildung 7: Zeitliche Abfolge der Infrarot-Spektren im Spektralbereich der Amide I und Amide II Banden (SEIRRAS Daten), aufgenommen in Abständen von einer Minute nach Zugabe einer 1 µM Lösung des Duftstoffes Lilial zu einer mit einem Geruchsrezeptor (OR5 der Ratte) funktionalisierten tethered membrane (Zusammenarbeit mit Prof. Eva Sinner, Universität für Bodenkultur/Wien, früher MPI für Polymerforschung/Mainz).
Mit den beschriebenen Untersuchungen hat man also einen ersten direkten experimentellen Zugang zur Quantifizierung bislang unbekannter Prozess-Parameter von Membranrezeptoren und ihren aus Lösung bindenden Liganden in der Hand, wie der Geschwindigkeit von Bindung und Loslösung (Assoziations- und Dissoziationsraten), der Festigkeit der Bindung (Affinitätskonstante),etc Dies ist ein wichtiger Schritt für die physikalisch-chemische Charakterisierung der Elementarprozesse bei der Geruchsrezeption, es ist aber auch ein Schritt hin zum Design von künstlichen Geruchssensoren auf der Basis biomimetischer Prozesse.
Eine Strukturänderung, aber auch eine bloße Umorientierung des Membranproteins infolge der Bindung des Duftstoffs an seinen Rezeptor kann sowohl zu einer Zunahme als auch zu einer Abnahme der Intensität einzelner Banden führen. Die signifikante Änderung von Infrarot-Banden im Beispiel der Bindung von Lilial an den Geruchs-Rezeptor OR5 (Abb. 7), könnte darauf hinweisen, dass sich bei der Reaktion (auch) einige der transmembranen Helizes des Rezeptors in ihrer Orientierung ändern und damit die gemessene IR- Bandensignatur beeinflussen. (Eine damit einhergehende und experimentell elektrochemisch nachweisbare Änderung der entsprechenden Dipolmomente steht zur Zeit noch aus.)
Ein nächster Schritt zum Design von Geruchssensoren
Die Konstruktion der tBLM und das damit erreichte und dokumentierte Eigenschaftsprofil sollten es erlauben, die Möglichkeit der elektrischen/elektrochemischen Detektion der Bindung von Geruchsstoffen an ihren Membran-Rezeptor im Hinblick auf die Entwicklung von Sensoren auszuloten und zu validieren. Die bereits angesprochene hervorragende elektrische Dichtigkeit der tBLMs - die Grundlage dafür, dass wir nur Hintergrundströme im Bereich von pA vorliegen haben - ermöglicht es alle sonstigen elektrogenen Prozesse mit hoher Empfindlichkeit zu detektieren. Dies ist am Beispiel des muscarinischen Acetylcholin-Rezeptors demonstriert (Abbildungen 8 und 9). 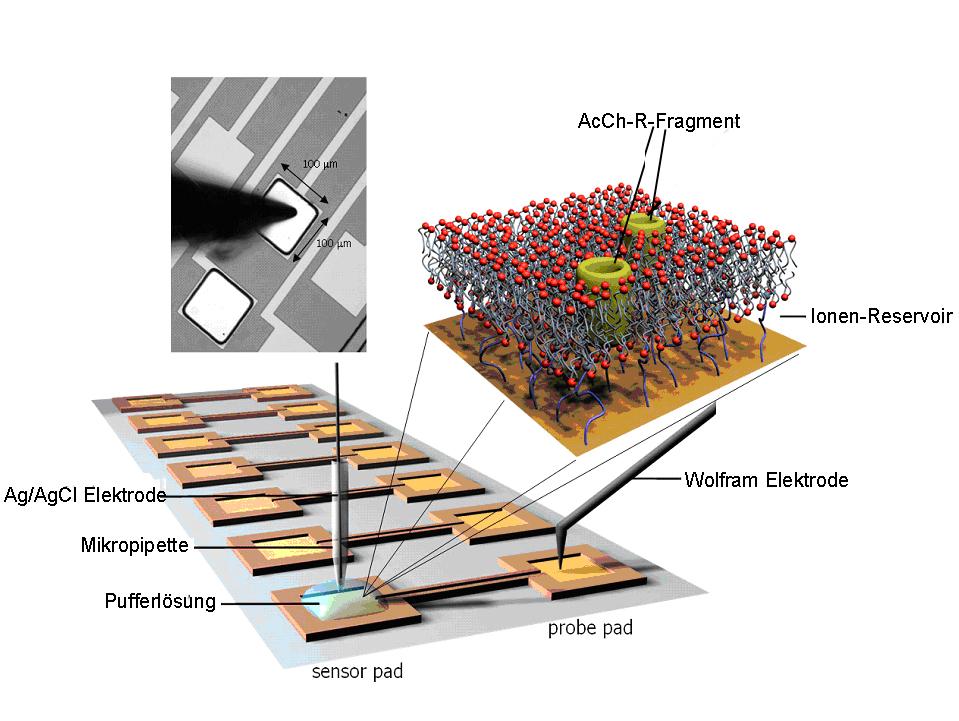 Abbildung 8: Experimenteller Aufbau zur empfindlichen Messung elektrischer/elektrochemischer Prozesse an tBLMs. Die einzelnen Gold- beschichteten Sensor- Pads (100x100 µm²) sind die Basis- (Working-) Elektroden, auf denen die Lipid-Doppelschichten präpariert wurden. Hier sind sie mit einigen wenigen Poren, dem inneren Kanal-Fragment des Acetylcholine-Rezeptors, funktionalisiert worden. In die darüber liegende Elektrolytschicht taucht die Gegen-Elektrode (Ag/AgCl- Silber/Silberchlorid) ein. Diese ist an einen Patch-clamp Verstärker zur rauscharmen Messung der Stromfluktuationen, welche durch die stochastisch öffnenden Kanäle verursacht wird, angeschlossen.
Abbildung 8: Experimenteller Aufbau zur empfindlichen Messung elektrischer/elektrochemischer Prozesse an tBLMs. Die einzelnen Gold- beschichteten Sensor- Pads (100x100 µm²) sind die Basis- (Working-) Elektroden, auf denen die Lipid-Doppelschichten präpariert wurden. Hier sind sie mit einigen wenigen Poren, dem inneren Kanal-Fragment des Acetylcholine-Rezeptors, funktionalisiert worden. In die darüber liegende Elektrolytschicht taucht die Gegen-Elektrode (Ag/AgCl- Silber/Silberchlorid) ein. Diese ist an einen Patch-clamp Verstärker zur rauscharmen Messung der Stromfluktuationen, welche durch die stochastisch öffnenden Kanäle verursacht wird, angeschlossen.
Hier kann das statistische Öffnen und Schließen eines einzelnen Kanal-Protein- Fragmentes des M2 muscarinischen Acetylcholine Rezeptors gezeigt werden (Abbildung 9). Nachdem das an die Gold(Au)-Basiselektrode angelegte Potential von 0 auf + 100 mV geschaltet wurde, zeigt der abnehmende Strom die Umverteilung der positiven und negativen Ionen im räumlich sehr beschränkten wässrigen Spalt zwischen der Elektrode und der Membran (Spacer/Tether Schicht: siehe Abb. 5 und 6): Wie Simulationsrechnungen gezeigt haben, wird dabei z.B die Kaliumionen Konzentration von zunächst 100 mM im Spalt auf 85 mM im stationären Zustand erniedrigt. Das sich dabei aufbauende elektrochemische Gegenpotential reduziert die an der Membran anliegende Spannung von 100 mV bis auf wenige 10 mV, was zu der beobachteten Abnahme des Stromes über die Membran führt. Entscheidend ist aber, dass diesem sehr niedrigen Hintergrund Fluktuationen von spontanen Stromänderungen im Bereich von wenigen pA überlagert sind, die dem stochastischen Öffnen und Schließen einzelner Kanalproteine zugeordnet werden können. Um es noch einmal hervorzuheben: diese Stromfluktuationen können wir nur detektieren, weil wir Membranen präparieren können, die einen so geringen Hintergrundstrom führen und damit die Fluktuationen klar detektierbar sind. 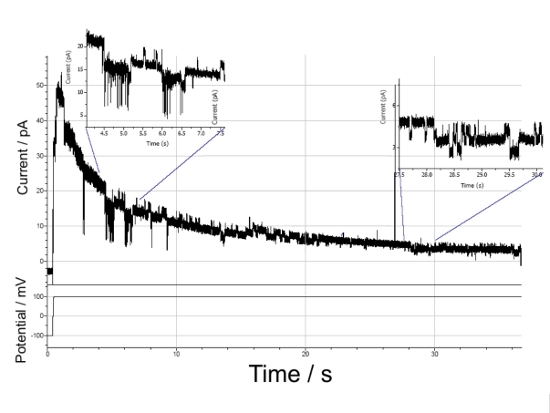 Abbildung 9: Stromverlauf durch eine mit einem Kanal-Protein-Fragment der M2 Isoform des muscarinischen Acetylcholine Rezeptors funktionalisierte tBLM nach Anlegen eines Spannungssprunges von 100 mV. Dem durch Ladungs- Umverteilungsprozesse kontinuierlich abnehmenden Basisstrom überlagert sind die Strom-Fluktuationen, welche durch das stochastische Öffnen und Schließen des Protein- Kanals verursacht werden.
Abbildung 9: Stromverlauf durch eine mit einem Kanal-Protein-Fragment der M2 Isoform des muscarinischen Acetylcholine Rezeptors funktionalisierte tBLM nach Anlegen eines Spannungssprunges von 100 mV. Dem durch Ladungs- Umverteilungsprozesse kontinuierlich abnehmenden Basisstrom überlagert sind die Strom-Fluktuationen, welche durch das stochastische Öffnen und Schließen des Protein- Kanals verursacht werden.
Mit diesem Ergebnis haben wir einen weiteren Meilenstein in Richtung Entwicklung eines biomimetischen Geruchssensor erreicht: Wie in Abb. 4 (Teil 2: science-blog, 26. Jänner 2012) schematisch gezeigt wurde, steht am Ende einer Reaktionskaskade, die mit der Bindung eines Geruchsstoffes an seinen Membran-ständigen Rezeptor beginnt, das Öffnen (und Schließen) von Ionen-Kanälen, die mit ihrem intrinsischen Verstärkungsfaktor (ein einzelner bindender Ligand erlaubt durch das Öffnen des Kanals den Durchtritt von 10 – 100 Millionen Ionen durch die Membran) letztendliche die hohe Empfindlichkeit von Nasen und Insekten-Antennen für Geruchsstoffe bestimmen.
Die biomimetische künstliche Nase – Ausblick
Man sollte das bisher Erreichte auf keinen Fall überbewerten. Auf der einen Seite sind wir noch sehr weit davon entfernt, auch nur annähernd die Komplexität der Reaktionskaskaden in einem Modellsystem nachbilden zu können. Der gesamte Verstärkungsmechanismus, der durch die G-Protein-Fragment-induzierte Aktivierung der Adenylat-Zyklase erreicht wird, hat bislang noch keine modellmäßige, biomimetische Realisierung erfahren. Insofern haben wir keine Ahnung, wie weit wir eigentlich noch vom natürlichen System und seinen unglaublichen Empfindlichkeiten bei unseren künstlichen Nasen entfernt sind.
Aber selbst wenn wir es in absehbarer Zeit schaffen sollten, für einen Rezeptor und damit für einen Geruchsstoff oder eine Klasse von Gerüchen einen Sensor bauen zu können, der den Vergleich mit der Nase eines Hundes nicht zu scheuen braucht, sind wir vom Endziel doch noch sehr, sehr weit entfernt.
Anders als bei der optischen Kommunikation, wo wir die Entstehung eines künstlichen Farb-Bildes auf einem Bildschirm und die Detektion eines Bildes mit einer hochempfindlichen Kamera auf die drei Grundfarben rot, grün, blau als den digitalen Informationsträgern reduzieren können, lebt die Geruchswelt nicht nur von einer Vielzahl von Rezeptoren (der Mensch hat etwa 350 davon, der Hund das Vierfache), die Sinneseindrücke, die wir beim Riechen erleben, werden von einer nahezu unüberschaubaren Vielfalt von Geruchsstoffen als den Informationsträgern bestimmt. Eine kleine Auswahl davon, klassifiziert nach Größe und Gestalt der Moleküle, ist in Abbildung 10 gegeben. 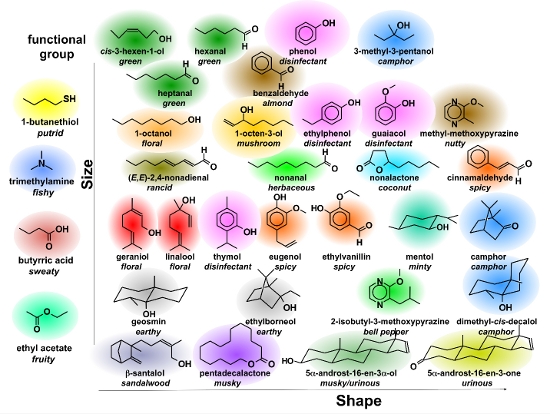 Abbildung 10: Zur Komplexität der Geruchssensorik: Klassifizierung von Gerüchen nach ihren zugrunde liegenden molekularen Strukturen und deren Parameter: Größe und Gestalt.
Abbildung 10: Zur Komplexität der Geruchssensorik: Klassifizierung von Gerüchen nach ihren zugrunde liegenden molekularen Strukturen und deren Parameter: Größe und Gestalt.
Zwar gibt es fast schon „klassische“ Beispiele, welchen Einfluss ein einzelner Geruchsstoff, wie etwa der Maiglöckchenduft (Bourgeonal und Zyklamal) auf uns (bzw. unsere Spermien) haben, aber in der Regel setzt sich unser Geruchseindruck aus vielen (Kombinationen von) Duftstoffen zusammen. Damit haben wir nicht nur das Problem der enormen Empfindlichkeiten, welche die Natur realisieren kann und unsere biomimetischen Nasen mindestens in etwa auch so zeigen müssen, wir werden auch lernen müssen, mit der Kombinatorik von Dufteindrücken umzugehen.
Gemessen an der Komplexität der molekularen Grundprozesse und ihrer biomimetischen Nachbildung im künstlichen Sensor scheint dieses Problem aber eher lösbar zu sein: wenn wir erst das System für einen Rezeptor optimiert haben, sollte es möglich sein auf dem Membran-Chip eine Vielzahl von Rezeptoren mit ihren unterschiedlichen Spezifitäten unterzubringen, parallel auszulesen und über Bioinformatik den kombinatorischen Zugang zu komplexeren Mischungen zu finden. Immerhin war das ja die Basis der - was die Identifikation von Geruchsmischungen angeht - relativ erfolgreichen Versuche, eine elektronische Nase zu realisieren:
eine Reihe von unterschiedlichen Polymeren oder anderen organischen Matrizen, die alle auf einen einzelnen Geruchsstoff relativ unspezifisch reagierten, konnten in der Kombinatorik der Muster-Erkennung tatsächlich einen Bourbon von einem Scotch oder Irish Wiskey unterscheiden. (Nur was die Empfindlichkeiten anlangte, waren die Ergebnisse absolut unbefriedigend und nährten den Wusch, über einen biomimetischen Weg verstärkt nachzudenken). 
Abbildung 11: Die (nicht ganz ernst gemeinte) Vision von der künstlichen Nase auf einem elektronischen Chip.
Es ist also noch ein weiter Weg bis zur künstlichen biomimetischen Nase, aber ein Anfang ist gemacht. Wie dieser Sensor am Ende aussehen wird, weiß heute noch niemand (Abbildung 11 - ein nicht ganz ernst gemeinter Vorschlag). Aber, um mit Goethe, der ja ein ausgewiesener Kenner der (Geruchs-) Welt war (Zitat:“...man möchte zum Maikäfer werden, um im Meer von Wohlgerüchen herumschweben zu können…“) zu enden: „…wer immer strebend sich bemüht…“ wir werden es weiter versuchen - und irgendwann müssen wir dann nicht mehr selbst „unsere Nase in alles stecken“!
Anmerkungen der Redaktion
Glossar
1 µm (mikrometer): 1 millionstel Meter, 1 nm (nanometer): 1 milliardstel Meter Amphiphil: Moleküle besitzen hydrophile (polare) und hydrophobe (lipophile) Bereiche; z.B. Emulgatoren, Tenside; vor allem aber Phospholipide , die essentielle Komponenten von Biomembranen sind
Adenosintriphosphat (ATP): Universeller Energielieferant für zelluläre Prozesse. Bei (enzymatischer) Spaltung der Phosphatbindungen wird Energie freigesetzt, die u.a. zur Synthese von Biomolekülen, zum Stofftransport durch Membranen, zur Muskeltätigkeit,.. benötigt wird. Daneben spielt ATP auch eine bedeutende Rolle im Signaltransfer
Biomembranen: trennen wässrige Kompartments von der Umgebung (Zellmembranen, intrazelluläre Membranen); in die Lipid-Doppelschicht sind verschiedene Arten von Membranproteinen eingelagert, u.a. (im Text erwähnt):
Black Lipid Membrane: über einen kleinen Spalt eines hydrophoben Materials (Teflon) spannt sich eine künstliche Lipid-Doppelschicht
Cytochrom c Oxidase: in der inneren Mitochondrienmembran lokalisiertes essentielles Enzym der „Atmungskette“, welches Sauerstoff zu Wasser reduziert. Die dabei freiwerdende Energie wird zur Synthese von ATP (aus ADP und Phosphat) verwendet.
„Fluorescence Recovery after Photobleaching“ (FRAP): Methode mit der die Geschwindigkeit der Diffusion eines bestimmten Moleküls in der Membran bestimmt wird. Dazu wird das Molekül mit einem fluoreszierenden Marker versehen, seine Fluoreszenzintensität in der Membran (mittle Fluoreszenzmikroskop) gemessen, dann die Fluoreszenz mittels eines kurzen Laserimpulses „gebleicht“ und die Zeit bestimmt mit der fluoreszierende Moleküle aus der Umgebung einwandern (diffundieren).
G-Protein gekoppelte Rezeptoren: Sehr große Familie von Transmembranproteinen (u.a. Geruchsrezeptoren), die mit 7 helikalen Segmenten die Zell-Membran durchqueren und Signale von außerhalb in die Zelle leiten (siehe Beitrag vom 5.1.2012)
Hydrophil: starke Wechselwirkungen mit Wasser („polare“ Wechselwirkungen), häufig wasserlösliche Stoffe.
Hydrophob: wasserabstoßende, fettlösliche (lipophile) Eigenschaften (z.B. Fette, Wachse)
Ionenkanäle: bilden Poren durch die Membran hindurch, durch welche elektrisch geladene Teilchen die Membran durchqueren können
Ionenpumpen: Transmembran-Proteine, die bestimmte Ionen „aktiv“ durch eine Biomembran transportieren. Aktiver Transport erhält seine Energie aus der enzymatischen Spaltung (durch ATPasen) von Adenosintriphosphat (ATP).
Lipid-Doppelschicht: Struktur, die sich aus amphiphilen Lipiden in wässriger (polarer) Lösung ausbildet. Der hydrophile Teil der Lipide ist nach aussen, der wässrigen Lösung zugewandt, der hydrophobe Teil der Lipide (Fettsäureketten) weist ins Innere der Doppelschicht (siehe Abbildungen 6, 8). Die Lipid-Doppelschicht ist rund 5 namometer dünn und für geladene Teilchen praktisch undurchlässig.
Ligand (Biologie): Molekül/Atom, das an ein Ziel-(Target-) Protein bindet; in den meisten Fällen ist die Bindung reversibel, d.h. der Ligand löst sich (dissoziiert) vom Target. Irreversible (kovalente) Bindung kann erfolgen, wenn der Ligand durch eine chemische Reaktion mit dem Target verknüpft wird.
Patch-clamp Technik: Methode nach dem Prinzip der Spannungsklemme mit der sich der durch einzelne Ionenkanäle in der Zellmembran fließende Strom messen lässt.
pH-Wert: Maß für den sauren oder basischen Charakter einer wässrigen Lösung; definiert durch den negativen (dekadischen) Logarithmus der Wasserstoffionenkonzentration (-aktivität). Wasser mit üblicherweise neutralem Charakter hat einen pH-Wert um etwa 7.0. Lösungen mit pH-Werten unter 7 werden als sauer bezeichnet, über 7 als basisch.
Thiol-Lipid Derivat: Lipide mit einer Thioalkohol (-SH)-Gruppe, die zur sehr festen Bindung des (Tether-)Lipids an das Gold-Substrat führt
Weiterführende Links
In diesem Video (7½ min.) des Max-Planck-Institut für Polymerforschung erläutert Professor Eva-Kathrin Sinner (siehe SB-Beitrag vom 15. Dezember 2011), wie es gelang, einen Sensor für den Duftstoff Lilial herzustellen:
